МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ВЫПОЛНЕНИЮ КОНТРОЛЬНЫХ РАБОТ ПО ФИЗИКЕ ДЛЯ СТУДЕНТОВ ЗАОЧНОЙ ФОРМЫ ОБУЧЕНИЯ
За время изучения курса общей физики студент-заочник должен выполнить 6 контрольных работ (по 2 в семестре).
2. Номер варианта - это последняя цифра номера зачетной книжки.
Контрольные работы нужно выполнить в отдельной тетради, на обложке которой приводятся сведения: фамилия, имя, отчество; факультет; номер зачетной книжки; домашний адрес; номер контрольной работы.
Условия задач надо переписать полностью.
В конце контрольной работы указать, каким учебником студент пользовался при выполнении работы.
Решение задач следует сопровождать пояснениями, если необходимо дать чертеж.
Решать задачу надо в общем виде. Числовые значения величин при подстановке их в расчетную формулу следует выражать в единицах СИ.
Для замечаний преподавателя на страницах тетради следует оставлять поля.
Ф И З И К А
(четвертый семестр)
Варианты контрольной работы № 2
| № варианта | НОМЕРА ЗАДАЧ | |||||||
 Раздел I Раздел I | Раздел II | |||||||
Р А З Д Е Л I
Задача 1. Определите число N молекул водорода, содержащихся в объеме 3 л при нормальных условиях, и массу m0молекулы водорода.
(7×1022; ~ 3×10-27 кг)
Задача 2. Два баллона соединены тонкой трубкой с краном. Объем первого баллона 3 л, второго - 8 л. В первом баллоне находится газ под давлением 750 мм рт.ст., а во втором - под давлением 300 мм рт.ст. Какое давление установится в баллонах при открытом соединительном кране? (Температура газа не изменяется).
(0,06 МПа)
Задача 3. Из сосуда откачивают воздух. Объем сосуда V0= 3 л, объем цилиндра насоса V = 0,5 л. Каким будет давление воздуха в сосуде после пяти рабочих ходов поршня (Р5), если в начале сосуд содержал воздух при атмосферном давлении Ро= 1,013×105Па?
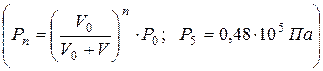 .
.
 Задача 4. Аэростат, наполненный газом при нормальном атмосферном давлении, поднялся в слой воздуха, где давление равно 500 мм рт.ст. Во сколько раз увеличился его объем? Изменение температуры не учитывать, влиянием упругости оболочки пренебречь.
Задача 4. Аэростат, наполненный газом при нормальном атмосферном давлении, поднялся в слой воздуха, где давление равно 500 мм рт.ст. Во сколько раз увеличился его объем? Изменение температуры не учитывать, влиянием упругости оболочки пренебречь.
(В 1,5 раза).
Задача 5. В вентиляционную трубу жилого дома поступает наружный воздух при температуре 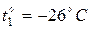 . Какой объем займет каждый кубический метр наружного воздуха, когда он поступит в комнату и нагреется до
. Какой объем займет каждый кубический метр наружного воздуха, когда он поступит в комнату и нагреется до 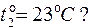
(1,2 м3).
Задача 6. Манометр на баллоне с кислородом показывает давление 98 атм. в помещении с температурой 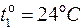 . Когда баллон вынесли на улицу, где температура была
. Когда баллон вынесли на улицу, где температура была 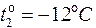 , манометр показал 86 атм. Не произошла ли утечка газа за время, прошедшее между двумя измерениями температуры?
, манометр показал 86 атм. Не произошла ли утечка газа за время, прошедшее между двумя измерениями температуры?
(Нет).
Задача 7. Какова максимальная разница зимой и летом в массе и в весе воздуха, заполняющего помещение объемом 100 м3, если летом температура в помещении повышается до 30° С, а зимой падает до 5°С? Атмосферное давление нормальное (Р0= 1,0×105Па).
(10,4 кг; 102 Н).
Задача 8. В колбе вместимостью 100 см3содержится некоторый газ, молекулы которого обладают средней кинетической энергией 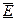 , равной 8,310-21Дж. На сколько понизится давление газа в колбе, если, вследствие утечки, из колбы выйдет N=1020молекул?
, равной 8,310-21Дж. На сколько понизится давление газа в колбе, если, вследствие утечки, из колбы выйдет N=1020молекул?
(5,55 кПа)
Задача 9. Давление газа равно 1 мПа, концентрация n его молекул равна 1010 см-3. Определите: 1) температуру Т газа; 2) среднюю кинетическую энергию 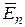 поступательного движения молекул газа.
поступательного движения молекул газа.
(7250К; 1,5×10-19 Дж).
Задача 10. Колба вместимостью 4л содержит 0,6 г кислорода под давлением 200 кПа. Определите среднюю кинетическую энергию 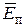 поступательного движения молекул.
поступательного движения молекул.
(10-19 Дж).
Задача 11. Определите среднее значение полной кинетической энергии 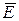 одной молекулы гелия (Не) и водяного пара (Н2О) при температуре Т = 400 К.
одной молекулы гелия (Не) и водяного пара (Н2О) при температуре Т = 400 К.
(8,28×10-21 Дж; 16,6×10-21 Дж).
Задача 12. Определите кинетическую энергию 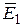 , приходящуюся в среднем на одну степень свободы молекулы азота, при температуре
, приходящуюся в среднем на одну степень свободы молекулы азота, при температуре
Т = 1 кК, а также среднюю кинетическую энергию 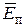 поступательного движения, среднюю кинетическую энергию
поступательного движения, среднюю кинетическую энергию 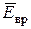 вращательного движения и среднее значение полной кинетической энергии
вращательного движения и среднее значение полной кинетической энергии 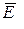 молекулы.
молекулы.
(6,910-21Дж; 20,710-21Дж; 13,810-21Дж; 34,510-21Дж).
Задача 13. Определите суммарную кинетическую энергию Еппоступательного движения всех молекул газа, находящегося в сосуде вместимостью 3 л под давлением 540 кПа.
(2,43 кДж).
Задача 14. Количество вещества гелия = 1,5 моля, температура газа Т=120 К. Определите суммарную кинетическую энергию Еппоступательного движения всех молекул этого газа.
(2,24 кДж)
Задача 15. Какова внутренняя энергия 1 моля кислорода при температуре 300К?
(»6,23 кДж)
Задача 16. Водород массой 10г нагрели на DТ = 200 К. Найдите изменение внутренней энергии водорода.
(12,5 кДж)
Задача 17. Какова внутренняя энергия водяного пара массой 10-3 кг, молекулы которого имеют среднюю кинетическую энергию, равную 1,5×10-20 Дж?
(502 Дж)
Задача 18. Определите среднюю арифметическую скорость молекул газа, если их средняя квадратичная скорость равна 1 км/с.
(0,92 км/c).
Задача 19. Определите среднюю квадратичную скорость 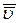 молекул газа, заключенного в сосуде вместимостью 2 л под давлением 200 кПа. Масса газа 0,3 г.
молекул газа, заключенного в сосуде вместимостью 2 л под давлением 200 кПа. Масса газа 0,3 г.
(2103м/c).
Задача 20. Колба вместимостью 4 л содержит некоторый газ массой 0,6 г под давлением 200 кПа. Определите среднюю квадратичную 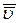 и среднюю арифметическую
и среднюю арифметическую 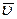 скорости молекул газа.
скорости молекул газа.
(2×103 м/c; 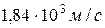 ).
).
Задача 21. Определите выражение для импульса молекул идеального газа, энергии которых равны наиболее вероятному значению энергии.
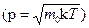 .
.
Задача 22. Используя функцию распределения молекул по скоростям, дайте вывод формулы, определяющей наиболее вероятную скорость v в молекул.
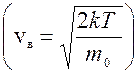 .
.
Задача 23. Получите выражение, определяющее долю молекул, энергия Е которых много меньше kТ. Функцию распределения молекул по энергиям считать известной.
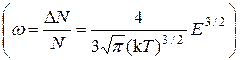 .
.
Задача 24. Считая функцию распределения молекул по энергиям известной, получите формулу, определяющую долю молекул, энергия Е которых много больше энергии теплового движения молекул.
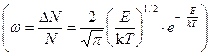 .
.
Задача 25. Во сколько раз изменится значение максимума функции распределения молекул идеального газа по энергиям F(E)max, если температура Т газа увеличится в 2 раза? Решение поясните графически.
(Уменьшится в 2 раза).
Задача 26. На какой высоте над поверхностью Земли атмосферное давление вдвое меньше, чем на ее поверхности? Считайте, что температура воздуха Т = 290 К и не изменяется с высотой.
(5,88 км).
Задача 27. Найдите изменение высоты h, соответствующее изменению давления на величину Р = 100 Па вблизи поверхности Земли, где температура Т = 290 К, а давление Р0= 100 кПа.
(8,78 м).
Задача 28. Барометр в кабине летящего самолета все время показывает одинаковое давление 80 кПа, благодаря чему летчик считает высоту полета неизменной. Однако, температура воздуха изменилась на Т = 1 К. Какую ошибку h в определении высоты допустил летчик? Считайте, что температура не зависит от высоты и что у поверхности Земли давление Р0= 100 кПа.
(6,5 м).
Задача 29. В центрифуге находится некоторый газ при температуре Т = 271 К. Ротор центрифуги радиусом а = 0,4 м вращается с угловой скоростью = 500 рад/c. Определите относительную молекулярную массу Мrгаза, если давление Р у стенки ротора в 2,1 раза больше давления Р0 в его центре?
(84, криптон).
Задача 30. Баллон вместимостью 10 л содержит водород массой 1 г. Определите среднюю длину свободного пробега молекул.
(1,55 нм).
Задача 31. Определите число соударений, которые происходят в течение 1 c между всеми молекулами водорода, занимающего при нормальных условиях объем 1 мм3.
(1,571021).
Задача 32. Вычислите теплопроводность К гелия при нормальных условиях.
(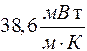 ).
).
Задача 33. Диффузия D кислорода при температуре 0C равна 0,19 см2/c. Определите среднюю длину свободного пробега молекул кислорода.
(135 нм).
Задача 34. Найдите динамическую вязкость гелия при нормальных условиях, если диффузия D, при тех же условиях, равна 1,0610-4 м2/c.
(19 мкПас).
Задача 35. Вычислите динамическую вязкость кислорода при нормальных условиях.
(13 мкПа×с).
Задача 36. В сосуде емкостью V = 0,3 л находится один моль углекислого газа при температуре Т = 300 К. Определите давление Р газа: 1) по уравнению Менделеева-Клапейрона; 2) по уравнению Ван-дер-Ваальса. (Для углекислого газа: 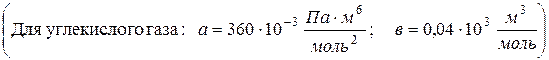
(8,31МПа; 5,67МПа).
Задача 37. Определите внутреннюю энергию U углекислого газа массой m=132г при нормальном давлении Р0 и температуре Т=300 К, рассматривая газ: 1) как идеальный; 2) как реальный.
(22,4 кДж; 9,2 кДж).
Задача 38. В сосуде вместимостью 10л находится азот массой 0,25 кг. Определите: 1) внутреннее давление Р¢ газа; 2) собственный объем V¢ молекул. (Замечание: постоянная «в» Ван-дер-Ваальса равна учетверенному объему всех молекул, содержащихся в одном моле газа).
(108 кПа; 86,2 см3).
Задача 39. В баллоне вместимостью 8л находится кислород массой 0,3 кг при температуре 300 К. Определите, какую часть объема сосуда составляет собственный объем молекул газа. Определите отношение внутреннего давления Р¢ к давлению газа на стенки сосуда (используйте «замечание» к задаче №38).
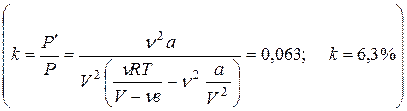 .
.
Задача 40. В сосуде вместимостью V1= 1 л содержится 10г азота. Определите изменение температуры азота (используя модель: газ Ван-дер-Ваальса), если газ расширяется в пустоту до объема V2 = 10л.
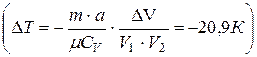 .
.
 2015-09-07
2015-09-07 1037
1037








