Эти анализы выполняют для определения уровня загрязнения сточных вод, выпускаемых рыбообрабатывающим предприятием; а также для оценки эффективности каких-либо способов очистки.
1. Азотистые вещества
В сточной воде рыбообрабатывающих предприятий азотистые вещества находятся частично в виде мельчайших кусочков рыбы и имеют белковую природу, частично в виде продуктов распада белков – экстрактивных веществ. Содержание в сточной воде первых можно определить по общему азоту, вторых – по аммонийному азоту.
В сточной воде рыбообрабатывающих предприятий содержание общего азота может составлять от следов до 250 мг/дм3 и более.
1.1 Общее содержание азота (по Къельдалю)
Оборудование, реактивы, материалы
Аппарат Широкого;
Колба Къельдаля:
Коническая колба на 100; 250 см3;
Пипетка на 1, 10 см3;
Цилиндр на 100 см3;
Дистиллированная вода, не содержащая аммонийных солей и аммиака (т.е. бидистиллят);
Серная кислота, пл. 1,84 г/см3 и 0,02 н. стандартный раствор,0,1 н раствор;
Едкий натр, 50%-ный раствор и 0,02 н. стандартный раствор;
Сульфат меди CuSO4× 5Н2О, 10%-ный раствор;
Индикатор метиловый красный (0,1 г метилового красного растворяют в 7,4мл 0,05 н раствора едкого натра и разбавляют раствор до 100 мл дистиллированной водой);
Фенолфталеин, 1%-ный спиртовой раствор;
Сульфат калия или сульфат натрия, безводный;
Сульфид натрия Nа2S×9H2О, 4%-ный раствор;
Пемза;
Кусочки пемзы предварительно кипятят несколько раз в дистиллированной воде, воду сливают и высушивают.
Сущность метода. При нагревании органических веществ со смесью концентрированной серной кислоты и сульфата калия (температура кипения 370°С) в присутствии катализатора происходит их разложение с образованием сульфата аммония (NH4)2SO4. Раствор подщелачивают, отгоняют аммиак и определяют его в отгоне.
Ход определения. Берут такой объем анализируемой сточной воды, чтобы в ней содержалось 2 - 6 мг азота (в виде органических соединений и солеи аммония), переносят в колбу Кьельдаля, прибавляют 10 см3 Н2S04 (плотностью 1,84 г/см3), 5 г сульфата калия или натрия, 1 см3 раствора сульфата меди и всыпают несколько кусочков пемзы. Содержимое колбы кипятят под тягой; сначала удаляется вода, потом начинается разложение органических веществ, и жидкость в колбе становится темной. Кипячение продолжают до тех пор, пока раствор в колбе не станет вполне прозрачным и бесцветным. Аналогичным образом обрабатывается холостая проба (без введения сточной воды). Колбу охлаждают, прибавляют 2,5 см3 раствора сульфида натрия, 3-5 капель раствора фенолфталеина и затем осторожно по стенке колбы, чтобы жидкости не смешивались, наливают 50 см3 раствора едкого натра. Колбу немедленно подключают в установку для отгонки, в приемник наливают 25 см3 0,02 н. раствора серной кислоты и 2-3 капли индикатора метилового красного и начинают нагревать. Конец трубки холодильника должен быть погружен в раствор серной кислоты, находящейся в приемнике. Отгонку ведут в течение 20-30 минут (до нейтральной реакция конденсата – проба на универсальную индикаторную бумагу). Затем отъединяют приемник и избыток серной кислоты в приемной колбе оттитровывают 0,02 н. раствором едкого натра, 1 мл которого соответствует 0,28 мг азота.
Общее содержание азота в мг/дм3 вычисляют по формуле 1:
X = 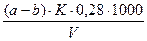 , (1)
, (1)
где а, b - объемы 0,02 н. раствора серной кислоты, израсходованные на титрование холостого опыта и пробы, см3;
К - поправочный коэффициент для приведения концентрации раствора серной кислоты к точно 0,02 н;
0,28 - количество азота, эквивалентное 1 см3 точно 0,02 н. раствора Н2SО4, см3;
V - объем СВ, взятой для анализа, см3.
1.2 Азот аммонийный
Аммиак в СВ рыбной отрасли определяют после предварительной отгонки из щелочной среды. В дистилляте большие количества аммиака определяют объемным методом, а малые – колориметрическим, с реактивом Несслера.
1.2.1 Объемный метод определения
Ход определения. Предварительную отгонку аммиака рекомендуется проводить при рН 9,5. СВ в количестве 100 - 250 см3 (в зависимости от содержания аммиака) вносят в колбу аппарата Широкого, прибавляют 1г окиси магния и перегоняют с водяным паром в приемник, в который предварительно наливают 25 см3 0,1 н. раствора Н2SО4 для поглощения аммиака. По окончании отгонки оттитровывают избыток кислоты 0,1 н. раствором NаОН в присутствии метилового красного.
Расчет производят по формуле 2:
X =14×(25 - a) × N × K × 1000 / V, (2)
где Х- содержание аммонийного азота, мг/дм3;
14 - эквивалент азота;
а - количество едкого натра, пошедшего на титрование избытка кислоты, см3;
N - нормальность раствора NаОН;
V - объем СВ, взятой для отгонки, см3;
К - поправочный коэффициент к нормальности титрованного раствора едкого натра.
1.2.2 Колориметрический метод определения (с реактивом Несслера)
Сущность метода. Аммиак реагирует в щелочной среде с йодомеркуриатом калия, образуя осадок желто-коричневого цвета. При низкой концентрации аммиака получается коллоидный раствор, пригодный для колориметрического определения. Нижний предел определения равен 0,05 мг NН 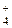 в 1г. Без разбавления можно определить не более 4 мг NH
в 1г. Без разбавления можно определить не более 4 мг NH 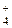 в 1г.
в 1г.
Оборудование, реактивы, материалы
Фотоколориметр;
Электроплитка;
Мерные колбы на 50,100 см3;
Пипетки на 1,10 см3;
Бидистиллят безаммиачный;
Реактив Несслера;
Тартрат натрия и калия (сегнетова соль), 50%-ннй раствор: растворяют 50 г KNаС4H4О6×4H2O в 100 см3 бидистиллята, прибавляют 0,2-0,5 см3 реактива Несслера. Раствор можно применять после осветления.
Едкий натр, чда, 15%-ный раствор.
Раствор А. Растворяют 0,2965 г NН4 Сl чда в бидистилляте и разбавляют до 1 дм3. В 1 см3 раствора содержится 0,1 мг NН4+. Раствор должен быть свежеприготовленный,
Раствор Б. 50 см3 раствора А разбавляют бидистиллятом до 1 дм3; в 1 см3 раствора содержится 0,005 мг NН4+. Раствор должен быть свежеприготовленным.
Реактивы не должны содержать аммиак, что контролируется холостым опытом.
Ход определения. К 50 см3 пробы или к меньшему ее объему, доведенному до 50 см3 бидистиллятом, прибавляют 1-2 капли сегнетовой соли и смесь тщательно перемешивают. Затем приливают 1 см3 реактива Несслера и через 15 минут измеряют оптическую плотность с фиолетовым светофильтром (400 - 420 нм) в кюветах с толщиной слоя 1-5 см. Из величины оптической плотности рабочего опыта (Д1) вычитают оптическую плотность холостого опыта (Д2) и по калибровочной кривой находят соответствующее ей значение величины NН4+ (a).
 2015-10-16
2015-10-16 856
856








