В химическом отношении простые эфиры характеризуются высокой инертностью по отношению ко многим реагентам, особенно основной природы. Они не расщепляются металлоорганическими соединениями, гидридами и амидами щелочных металлов, а также комплексными гидридами бора и алюминия. Простые эфиры практически незаменимы в качестве растворителей при получении магнийорганических и других металлоорганических соединений, а также для реакций восстановления алюмогидридами и его производными. Сольватирующая способность эфиров как растворителей основана на их свойствах жестких оснований Льюиса. Эфиры образуют очень прочные комплексы с жесткими кислотами Льюиса - BF3, AlBr3, AlR3, SbCl5, SbF5, SnCl4, ZnCl2 и т.д. состава 1:1 или 2:1.
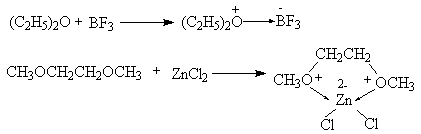
Как основания Льюиса простые эфиры образуют комплексы с галогенами, в которых эфир играет роль донора, а галоген акцептора. Раствор иода в эфире окрашен в коричневый цвет в отличие от фиолетовой окраски иода в растворах в алканах.
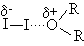
Сдвиг максимума поглощения при комплексообразовании позволяет оценить прочность комплекса. Кроме того в ультрафиолетовой области появляется новая полоса поглощения, называемой полосой переноса заряда. Такие комплексы получили название комплексов с переносом заряда (КПЗ). Эфиры образуют соли триалкилоксония при взаимодействии с очень сильными алкилирующими агентами.
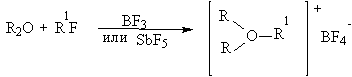
Триэтилоксонийборфторид легко получается при взаимодействии эфирата трехфтористого бора с эпихлоргидрином в абсолютном эфире.
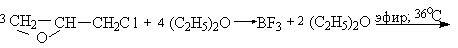
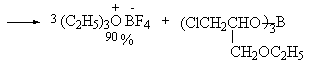
В настоящее время соли триалкилоксония получают при взаимодействии простых эфиров с алкилтрифлатами или алкилфторсульфонатами. Катион триалкилоксония - сильнейший алкилирующий агент почти для любого, даже слабого нуклеофильного агента.
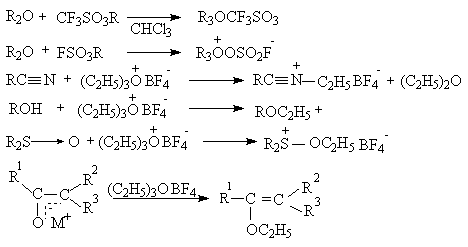
На способности простых эфиров давать соли оксония основаны способы расщепления простых эфиров под действием бромистоводородной или иодистоводородной кислот, а также тригалогенидов бора.
Тиоспирты (тиолы) — соединения, содержащие группу — SH, соединенную с углеводородным радикалом, напр. C2H5SH
Химические свойства. Тиоспирты можно рассматривать как производные сероводорода, имеющего в водных растворах свойства слабой кислоты. Соответственно тиоспирты обладают заметными кислотными свойствами. Так, например, при действии щелочей образуются соединения, аналогичные алкоголятам и получившие название меркаптидов:
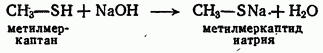
Следует напомнить, что алкоголяты спиртов в отличие от меркаптидов получаются только при действии щелочных металлов, на спирты.
Способы получения. 1. Тиоспирты получаются действием гидросульфида натрия на галоидные алкилы:
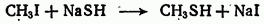
2. Тиоэфиры образуются:
а) при взаимодействии двух молекул галоидпроизводного с сернистым натрием:
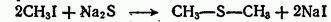
б) при действии галоидных алкилов на меркаптиды:
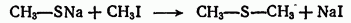
Метилмеркаптан  Газ с темп. кип. +6°С, образующийся при гниении белковых веществ. Содержится в человеческих испражнениях, чем объясняется их неприятный запах.
Газ с темп. кип. +6°С, образующийся при гниении белковых веществ. Содержится в человеческих испражнениях, чем объясняется их неприятный запах.
2. Гомологи бензола. Номенклатура и изомерия
Гомологи бензола – соединения, образованные заменой одного или нескольких атомов водорода в молекуле бензола на углеводородные радикалы (R):
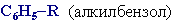
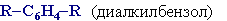
Общая формула гомологического ряда бензола 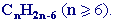
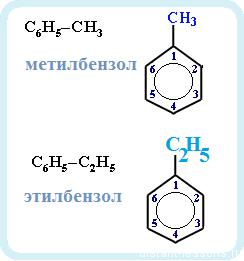
Номенклатура. Широко используются тривиальные названия (толуол, ксилол, кумол и т.п.). Систематические названия строят из названия углеводородного радикала (приставка) и слова бензол (корень):
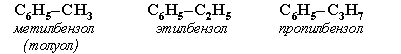
Если радикалов два или более, их положение указывается номерами атомов углерода в кольце, с которыми они связаны. Нумерацию кольца проводят так, чтобы номера радикалов были наименьшими. Например:
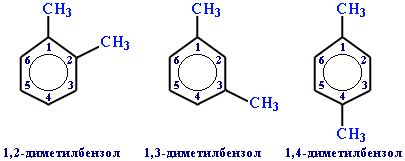
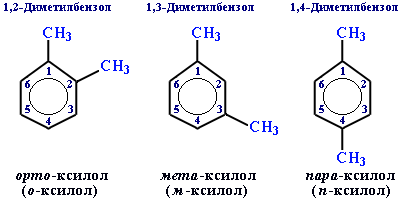
Для дизамещенных бензолов R-C6H4-R используется также и другой способ построения названий, при котором положение заместителей указывают перед тривиальным названием соединения приставками:
орто - (о -) заместители у соседних атомов углерода кольца, т.е. 1,2-;
мета - (м -) заместители через один атом углерода (1,3-);
пара - (п -) заместители на противоположных сторонах кольца (1,4-).
Ароматические одновалентные радикалы имеют общее название " арил ".
Из них наиболее распространены в номенклатуре органических соединений два: C6H5- (фенил) и C6H5CH2 - (бензил).
Изомерия (структурная):
1) положения заместителей для ди -, три - и тетра -замещенных бензолов (например, о -, м - и п -ксилолы);
2) углеродного скелета в боковой цепи, содержащей не менее 3-х атомов углерода:
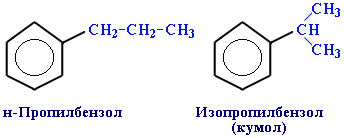
3) изомерия заместителей R, начиная с R = С2Н5.
Например, молекулярной формуле С8Н10 соответствует 4 изомера:
три ксилола CH3-C6H4-CH3 (о-, м-, п-) и этилбензол C6H5-C2H5.
Пространственная изомерия относительно бензольного кольНоменклатура гомологов бензола:
Название углеводорода складывается из двух частей:
(количество и указание места прикрепления) и название радикала + «бензол»
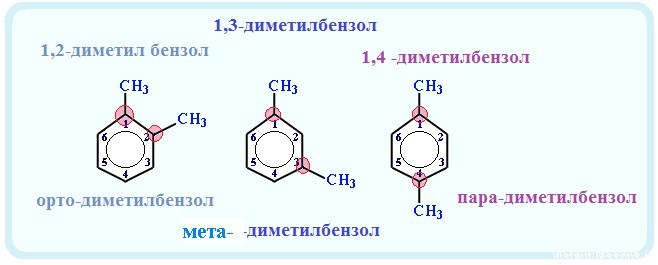
Если в молекуле арена есть несколько одинаковых радикала, то применяются приставки: орто-, мета — и пара-
· орто- (о-) — два радикала находятся рядом — при соседних атомах углерода (1,2-ди «радикал» бензол);
· мета- (м-) — два радикала находятся через один атом углерода (1,3 — ди «радикал» бензол)
· пара- (п-) — два радикала находятся друг против друга — через 2 атома углерода (1,4- ди «радикал» бензол)
Все эти вещества изомерны друг другу. У бензола и его гомологов довольно много изомеров — это обусловлено как количеством атомов, так и геометрией молекулы.
ца в алкилбензолах отсутствует.
· Получение гомологов бензола: алкилирование бензола:
реакция проводится в присутствии катализатора — галогенидов алюминия, например, AlCl3:
C6H6 + CH3Cl → C6H5CH3 + HCl

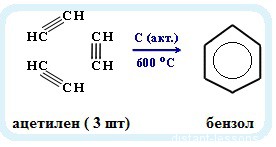
· Именная реакция — реакция Зелинского. Получение бензола из ацетилена:
3С2H2 → C6H6
 Это основные, «классические» способы получения бензола и его гомологов, теперь рассмотрим варианты из заданий ЕГЭ
Это основные, «классические» способы получения бензола и его гомологов, теперь рассмотрим варианты из заданий ЕГЭ
1. Получение бензола из неорганических веществ:
· 1вариант:
Исходное вещество — карбид кальция СaC2:
CaC2 + 2H2O → Ca(OH)2 + C2H2 — ацетилен
дальше — реакция Зелинского: 3С2H2 → C6H6 Это самый короткий путь получения.
· 2 вариант:
Исходное вещество — карбид алюминия Al4C3:
Al4C3 + 12H2O → 4Al(OH)3 + 3CH4 — метан
2СH4 (1500 °C) → C2H2 + 3H2
дальше — реакция Зелинского
2. Получение бензола и его гомологов из других неорганических веществ:
1) получение бензола из алканов:
СH4 (1500 °C) → C2H2 (С, 600ºС) → С6H6
2) получение бензола и его гомологов из алкенов:
С2H4 → C2H2 →C6H6
Толуо́л (от исп. Tolu, толуанский бальзам) — метилбензол, бесцветная жидкость с характерным запахом, относится к аренам.
Толуол получен впервые П. Пельтье в 1835 при перегонке сосновой смолы. В 1838 выделен А. Девилем из бальзама, привезенного из города Толу в Колумбии, в честь которого получил своё название[1].
Получение и очистка[править | править вики-текст]
Продукт каталитического риформинга бензиновых фракций нефти. Выделяется селективной экстракцией и последующей ректификацией.Также хорошие выходы достигаются при каталитическом дегидрировании гептана через метилциклогексан.
Очищают толуол аналогично бензолу, только в случае применения концентрированной серной кислоты следует учитывать, что толуол сульфируется легче бензола, а, значит, необходимо поддерживать более низкую температуру реакционной смеси (практически — менее 30 °C).
Толуол также образует с водой азеотропную смесь[2][3].
Толуол можно получить из бензола по реакции Фриделя — Крафтса с использованием трибромида железа в качестве катализатора:
{\displaystyle {\mathsf {C_{6}H_{6}+CH_{3}Br{\xrightarrow[{}]{FeBr_{3}}}C_{6}H_{5}CH_{3}+HBr}}} 
Билет 12
АЛЬДЕГИДЫ И КЕТОНЫ – органические соединения, содержащие фрагмент >C=O (углерод, связанный двойной связью с кислородом, его называют карбонильным). У альдегидов карбонильный углерод соединен с атомом Н и органической группой R (общая формула RHC=O), а в кетонах – с двумя органическими группами (общая формула R2С=О).
Номенклатура альдегидов и кетонов. Группу –(Н)С=О называют альдегидной, для связывания с органическими группами у нее есть всего одна свободная валентность, это позволяет ей находится только на конце углеводородной цепи (но не в середине). При составлении названия альдегида указывается название соответствующего углеводорода, к которому добавляется суффикс «аль», например, метаналь Н2С=О, этаналь Н3СС(Н)=О, пропаналь Н3ССН2С(Н)=О. В более сложных случаях углеродную цепь группы R нумеруют, начиная с карбонильного углерода, затем с помощью числовых индексов указывают положение функциональных групп и различных заместителей.
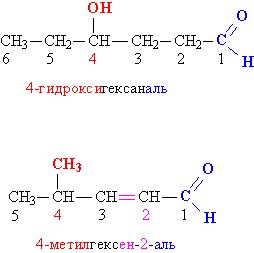
Рис. 1. НОМЕНКЛАТУРА АЛЬДЕГИДОВ. Замещающие и функциональные группы, а также соответствующие им цифровые индексы выделены различающимися цветами.
Для некоторых альдегидов часто используют тривиальные (упрощенные) названия, сложившиеся исторически, например, формальдегид Н2С=О, ацетальдегид Н3СС(Н)=О, кротоновый альдегид СН3СН=CHC(H)=O.
В отличие от альдегидной, кетонная группа >C=O может находиться также в середине углеводородной цепи, поэтому в простых случаях указывают названия органических групп (упоминая их в порядке увеличения) и добавляют слово «кетон»: диметилкетон CH3–CO–CH3, метилэтилкетон CH3CH2–CO–CH3. В более сложных случаях положение кетонной группы в углеводородной цепи указывают цифровым индексом, добавляя суффикс «он». Нумерацию углеводородной цепи начинают с того конца, который находится ближе к кетонной группе (рис. 2).
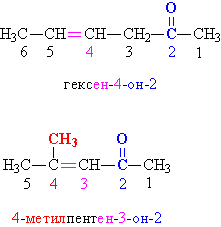
Рис. 2. НОМЕНКЛАТУРА КЕТОНОВ. Замещающие и функциональные группы и соответствующие им цифровые индексы выделены различными цветами.
Для простейшего кетона CH3–CO–CH3 принято тривиальное название – ацетон.
 2018-01-21
2018-01-21 949
949








