Например для реакции:
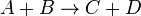
выражение для скорости будет выглядеть так:
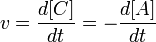 .
.
закон действующих масс:
Скорость химической реакции в каждый момент времени пропорциональна концентрациям реагентов, возведенным в некоторые степени.
Для элементарных реакций показатель степени при значении концентрации каждого вещества часто равен его стехиометрическому коэффициенту, для сложных реакций это правило не соблюдается. Кроме концентрации на скорость химической реакции оказывают влияние следующие факторы:
§ природа реагирующих веществ,
§ наличие катализатора,
§ температура (правило Вант-Гоффа),
§ давление,
§ площадь поверхности реагирующих веществ.
Если мы рассмотрим самую простую химическую реакцию A + B → C, то мы заметим, что мгновенная скорость химической реакции величина непостоянная.
КИНЕТИЧЕСКОЕ УРАВНЕНИЕ, выражает зависимость скорости хим. р-ции от концентраций компонентов реакц. смеси. Для простой (одностадийной) гомог. р-ции скорость v пропорциональна произведению концентраций реагирующих в-в и кинетическое уравнение записывается в виде:
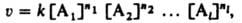
где [Ai] (i=1,2,...,l) - концентрация i-го в-ва, ni-порядок реакции по i-му в-ву, k-константа скорости р-ции.
 2018-01-21
2018-01-21 945
945








