10.1 Синтез через шикимову кислоту
Гексозомонофосфатний шлях асиміляції вуглеводів веде до синтезу циклічних структур, включно деяких гетероциклічних сполук. Початковою реакцією, що лежить в основі синтезу циклічних структур, є взаємодія між фосфоенолпіруватом і Д-еритрозо-4-фосфатом. Дякуючи приєднанню карбонільної групи цукру до подвійного зв’язку енолпірувату з них спочатку утворюється 3-дезокси-Д-арабіно-гептулозо-7-фосфат, причому фосфатна група фосфоенол-піровиноградної кислоти втрачається. 3-дезокси-Д-арабіно-гептулозонат-7-фосфат циклізується в 5-дегідрохінну кислоту. На цьому етапі можливі проміжні реакції за участю НАД+ і НАД-Н
Шляхом відщеплення води з 5-дегідрохінної кислоти утворюється 3-дегідрошикимова кислота, яка потім відновлюється в шикимову кислоту. Після фосфорилювання в 3-му положенні шикимова кислота реагує з фосфоенолпіруватом, в результаті утворюється шикимат-5-енол-піруват-3-фосфат. При відщепленні залишку фосфорної кислоти ця сполука переходить в харизмову кислоту (рис.10-1). Остання є вихідним продуктом для синтезу антранілової, н-амінобензойної, о- і н-оксибензойної кислот, рівно як і амінокислот фенілаланіну, тирозину, триптофану (рис.10-2).





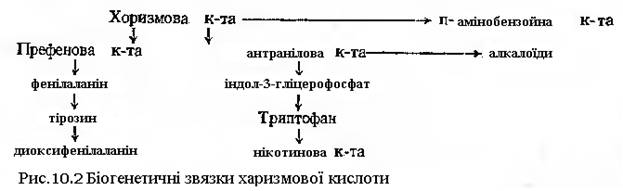
Харизмова кислота є вихідним продуктом синтезу убіхінонів. Відомо, що убіхінони приймають участь в переносі електронів у дихальному ланцюзі. По хімічній природі є бензохінонами, які мають гідрофобні ізопренові бокові ланцюги.
В результаті ферментативного відщеплення піровиноградної кислоти від харизмової утворюється п-оксибензойна кислота. Остання вступає у реакцію з пренілпірофосфатом, при цьому втрачається карбоксильна група п-оксибензойної кислоти. Утворений пренілгідрохенон гідроксилюється, метилюється і т. і. в інших реакціях. Всі метильні і метоксильні групи походять з метіоніну. Синтез пренілпірофосфату здійснюється шляхом, який властивий каротиноїдам, через мевалонова кислоту (рис.10-3).

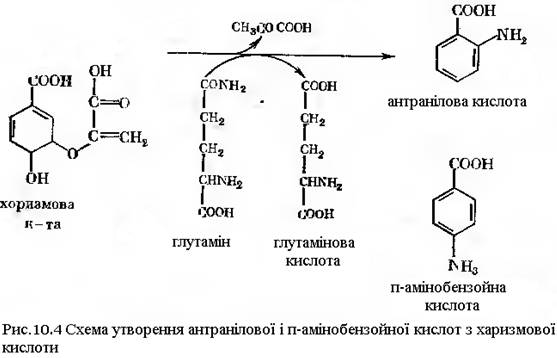
Однією з важливих метаболічних функцій харизмової кислоти є її властивість до амінування, в результаті чого з’являються продукти, що містять у своїй структурі азот. До них в першу чергу відносять антранілова і п-амінобензойна кислота. Як при синтезі антранілової, так і при синтезі п-амінобензойної кислоти донорами аміногруп є глютамін, що віддає свою амідну групу або іон амонію. Однак, вирішальну роль відіграє глютамін як більш специфічний донор. Для обох реакцій потрібний магній, а при синтезі п-амінобензойної кислоти потрібен гуанозин. Вважають, що між вихідною речовиною, харизмовою кислотою і кінцевими продуктами є проміжні метаболіти, які не були виділені, тому зображені на рис.10-4 реакції не дають уявлення про всі деталі процесу.
Вихідною речовиною для біосинтезу феноксазинових похідних також є харизмова кислота. У даному випадку в результаті ряду реакцій проходить формування гетероциклічної структури. В якості одного з найбільш відомих речовин, в основі якої лежить феноксазинова структура, може бути названий актиноміцин Д. він добре відомий як інгібітор активності РНК-полімерази. Після амінування харизмової кислоти утворена антранілова кислота гідроксилюється, в результаті утворюється 3-оксиантранілова кислота. Після її метилювання відбувається приєднання пептидної групи з утворенням пептидлактона-3-окси-4-метилантранілової кислоти. Дві молекули пептидного лактону конденсуються з утворенням феноксизону, похідними якого є актиноміцини (рис.10.5).


З антранілової кислоти відбувається синтез хінолінових похідних, зокрема алкалоїдів, що відносяться до псевданів, названі так за родовою назвою культур-продуцентів Pseudomonas. В реакцію вступає антранілова кислота у вигляді своєї КоА-похідної. Другим компонентом реакції слугує також КоА-похідна β-кетокислоти, число вуглецевих атомів якої залежить від їх кількості у боковому ланцюзі псевдана (рис.10.6).

При розгляданні шляхів синтезу продуктів, утворених через антранілову кислоту, особливо вторинних метаболітів, необхідно мати на увазі, що можливим метаболічним попередником для них може бути триптофан. У цьому випадку антранілова кислота також приймає участь в синтезі, але вона походить з триптофану в результаті його ферментативного розкладу.
Одним з метаболітів актиноміцетів є антибіотик новобіоцин. Дивлячись на механізм біогенезу, новобіоцин відомий тим, що у формуванні його молекули приймають участь продукти, які виникають в результаті функціонування гексозомонофосфатного шляху, і похідна глюкози – новіоза. З шикимата утворюються проміжні метаболіти синтезу 3-аміно-4,7-диокси-8-метилкумарин і 4-окси-3(3-метил-2-бутеніл)-бензойна кислота (рис.10.7).

10.2 Введення функціональних груп в циклічні структури
По ходу формування циклічних структур або після завершення їх синтезу можуть відбуватись різні ензиматичні реакції, що забезпечують введення нових функціональних груп. Декілька таких реакцій було показано при розгляданні механізму біогенезу молекули тетрацикліну. Важливим етапом в процесі біосинтезу є введення замісників шляхом утворення С-С зв’язків. Найбільш часто в якості таких замісників зустрічається метильна група і алкільні радикали, зокрема поліізопренових убіхінонів, вітаміну К і ряду інших продуктів, які мають походження з шикимової кислоти.
Метилювання. Рекція метилювання може проходити в процесі формування циклічної структури. Вважають, що при синтезі продуктів, які мають полікетиди в якості проміжних метаболітів, С-метилювання проходить перед замиканням кільця, до вивільнення ароматичного продукту від зв’язаного з ним ферменту. Можливо, на цьому рівні відбувається приєднання будь-якого іншого радикалу, хоча допускають, алкілування може проходити і на сформованих ароматичних сполуках, де в реакцію вступають вуглеводні атоми, які мають нуклеофільний характер. Акцепторами метильних груп можуть бути сполуки, які мають аміногрупи або заміщенні аміногрупи (-NH2, -NHR, -NR-R1), гідроксильні (-ОН) або сульфгідрильні (-SH) групи.
Основним джерелом метильних груп слугує метіонін у своїй активній формі у вигляді S-аденозинметіоніну.

За рахунок активності метилтрансферази відбувається перенесення метильної групи S-аденозилметіоніну до відповідного акцептору, в результаті чого S-аденозилметіонін перетворюється перетворюється в S- аденозилгомоцистеїн. Метилтрансферази відрізняються за своєю специфічністю до певних акцепторів. Коферментом при переносі одно- вуглецевих сполук, зокрема метильної групи, є відновлена форма фолієвої кислоти – тетрагідрофолієва кислота.

Тут слід звернути увагу на те, що у склад фолієвої кислоти і відповідно тетрагідрофолату входить п-амінобензойнга кислота. Її антиметаболітом є сульфаніламід, який має структурну подібність з цією кислотою. Якщо виникає необхідність обмежити або повністю призупинити реакції метилювання, то у сферу реакції, у даному випадку в середовище, вводять сульфаніламід. Внаслідок структурної подібності з п-амінобензойною кислотою, він входить замість неї у реакцію, змінюючи структуру коферменту і перетворюючи його в неактивну сполуку. Саме таким шляхом можна користуватися, якщо потрібно отримати диметильну похідну тетрацикліну.

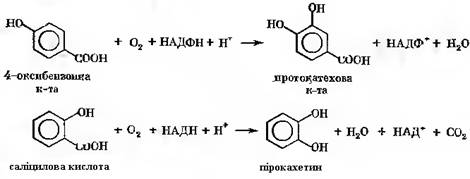
Гідроксилювання. На сформованій ароматичній структурі можуть проходити реакції введення гідроксильних замісників. Ензиматичний процес гідроксилювання здійснюють монооксигенази, які включають один атом кисню з молекули О2 на молекулу субстрату, а другий атом вивільняють через воду. В якості переносника водню, простетичної групи, вони мають птеридин і флавін. Вони каталізують речовини, в яких –Н або –СООН заміщується на –ОН. Прикладом можуть служити реакції гідроксилювання 4-оксибензойної кислоти, в результаті утворюється протокатехова кислота і саліцилова кислота, яка перетворюється в пірокахетин. В першому випадку реакцію здійснює п-оксибензоатгідроксилаза, у другому – саліцилат гідроксилаза.
Іншим прикладом подібних реакцій служить синтез м-оксибензойної кислоти і антибіотику патуліну (рис.18-8). Механізм синтезу 6-метилсаліцилової кислоти приведений вище. В цих реакціях приймають участь 6-метилсаліцилатдекарбоксилаза; м-крезолгідроксилаза; дегідрогеназа, каталізуюча обернене перетворення м-оксибензолу у відповідний альдегід, м-оксибензол гідроксилаза. Обом названим гідроксилазам потрібен кисень і НАДФН для прояву активності.

Хлорування і дехлорування. В молекулах антибіотику хлор- тетрацикліну і гризеофульвіну міститься атом хлору. В зв’язку з цим для синтезу названих сполук повинна бути присутньою мінеральна хлормістка сполука. Звичайно вводять солі калію і натрію. Хлорування відбувається тоді, коли циклічна структура уже сформована. Ензиматична система, здійснююча цей процес, невідома.
Більш складною є задача отримання сполуки, без хлору, зокрема тетрацикліну. Необхідність отримання такої речовини обумовлена її терапевтичними властивостями, відмінними від хлортетрацикліну. Оскільки іон хлору майже завжди присутній в компонентах середовища для ферментації, виникає задача блокувати його включення в молекулу. Цього досягають шляхом введення в склад середовища конкурентного хлору іону брому. Іон брому перешкоджає включенню хлору в тетрациклінове ядро. Звичайно використовують бромисті солі натрію і калію. Вводити броміди слід у строго визначених концентраціях, оскільки високий вміст їх у середовищі може призвести до включення брому в молекулу тетрацикліну і утворення бромтетрацикліна. Введення у середовище фториду натрію і йодиду калію – менш ефективне, ніж введення бромної солі. Інтенсивність кокурентного припинення відмічалось у такій послідовності: Br>F>J.
При введенні в середовище бромідів все ж таки не вдається отримати 100% вихід тетрацикліну. Близько 10% приходиться на хлортетрациклін. Для отримання 98-100% виходу тетрацикліну в середовище, що містить бромід натрію, рекомендовано вносити 2-меркаптобензотіазол, тіосечовину або 2-тіоурацил. Вважають, що інгібіторами хлорування є в основному речовини, які мають загальну формулу

Тут X-S, -SH, SR, -NH2, -NHR, -NRR (R-метил, -феніл, -бензил та ін. ефіри), У-S, або N. Механізм дії цих сполук не встановлений. Можливо, наявність у них сульфгідрильної групи забезпечує включення іону хлору в реакцію до формування молекули антибіотику. Можливо також, що тіосполуки зв’язують мідь, яка є складовою частиною поліфенолоксидазних ферментів, що приймають участь в процесі хлорування.
Отримані мутанти, у яких спадково порушений механізм хлорування. Вони здатні виробляти значні кількості тетрацикліну в присутності іону хлору.
При біосинтезі гризеофульвіну шляхом введення в середовище бромідів, йодидів, фторидів або тіосечовини також не відбувається включення хлору в молекулу. При цьому утворюється дехлоргризеофульвін.
 2018-01-21
2018-01-21 1305
1305
