6.1. Цель работы
Ознакомление с методикой опытного определения показателя адиабаты реальных газов, получение навыков в проведении теплотехнического эксперимента.
6.2. Задачи работы
Экспериментальное определение численного значения показателя адиабаты воздуха и обработка результатов эксперимента.
Адиабатный процесс – это процесс изменения состояния идеального газа, протекающий без теплообмена с окружающей средой:
Δq=0 (6.1)
Адиабатный процесс является одним из наиболее часто встречающихся на практике термодинамическим процессом изменения состояния рабочего тела.
Уравнение адиабатного процесса имеет вид [1]:
 (6.2)
(6.2)
где k – показатель адиабаты, равный отношению изобарной теплоемкости CP к изохорной CV:
 >1 (6.3)
>1 (6.3)
Численное значение показателя адиабаты для идеального газа можно получить исходя из молекулярно-кинетической теории газов:
для одноатомного газа k = 1,66;
для двухатомного газа k = 1,4;
для многоатомного газа k = 1,33.
Для идеальных газов величина k является постоянной, не зависящей от параметров состояния газа.
Связь между изобарной и изохорной теплоемкостями устанавливает уравнение Майера:
СP – СV = R (6.4)
Выразив CP из формулы (6.4), формулу (6.3) можно привести к виду:
 (6.5)
(6.5)
Поскольку для реальных газов теплоемкость СV возрастает с увеличением температуры интенсивнее, чем СР, то значение k с увеличением температуры уменьшается. Величина k для реальных газов одной атомности при прочих равных условиях имеет отличия. Так, например, для двухатомных газов: водород k = 1,41; азот k = 1,404; воздух k = 1,4.
Допустим, что условия опыта с достаточной степенью точности удовлетворяют уравнению состояния идеального газа:
p v = M∙R∙T (6.6)
Представим сосуд, заполненный газом, имеющим параметры: давление p1 и температуру Т1, превышающие параметры окружающей среды. За счет охлаждения стенок сосуда окружающей средой и отвода некого количества теплоты q1, температура газа станет равной температуре окружающей среды – Т2, а давление снизится до некого значения р2 (процесс 1-2 рис. 6.1). Затем быстро выпустим газ из резервуара, соблюдая тем самым условия адиабатного расширения – отсутствие теплообмена с окружающей средой.

Рис. 6.1. К определению показателя адиабаты
В конце процесса 2-3 давление в сосуде станет равным давлению окружающей среды р3, а температура понизится до Т3, меньше Т2. Закроем сосуд и выждем некоторое время, в течение которого от окружающей среды к более холодному телу будет подведена теплота q2 (процесс 3-4).
В результате температура возрастет до температуры окружающей среды (Т4 = Т2), а давление повысится до некоторого значения Р4.
Учитывая уравнение адиабатного процесса (6.2) можно записать:
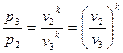 (6.7)
(6.7)
Логарифмируя выражение (6.11) запишем:
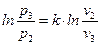 (6.8)
(6.8)
Выведем отсюда k:
 (6.9)
(6.9)
Так как Т2 = Т4, можно предположить, что по линии 2-4 протекает условный изотермический процесс (Т = const), которому соответствует выражение:
 (6.10)
(6.10)
С учетом выражения (6.10) уравнение (6.9) примет вид:
 (6.11)
(6.11)
6.4. Описание экспериментальной установки
Экспериментальная установка (рис. 6.2.) состоит из ресивера 6, в котором с помощью компрессора 3 создается избыточное давление, измеряемое чашечным манометром 7.
На линии нагнетания от компрессора к ресиверу расположен трехходовой кран 4. Выпуск сжатого воздуха из ресивера производится через кран 5. Привод компрессора осуществляется от электродвигателя 2, питающегося трехфазным током.
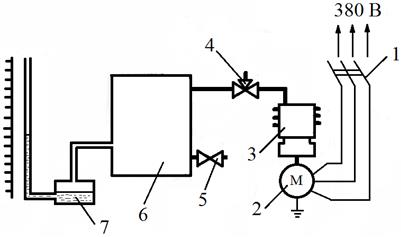
Рис. 6.2. Схема экспериментальной установки: 1 – рубильник;
2 – электродвигатель; 3 – компрессор; 4 – трехходовой кран;
5 – быстродействующий кран; 6 – ресивер; 7 – жидкостный чашечный манометр
Силовая сеть имеет рубильник 1. Трехходовой кран в работе занимает два положения. В одном из них производится нагнетание воздуха в ресивер, во втором – сжатый воздух из компрессора уходит в атмосферу, при этом ресивер отключается от нагнетательной линии.
6.5. Порядок проведения работы.
1) Убедиться по показанию манометра, что в ресивере нет избыточного давления. В противном случае выпустить из ресивера воздух через кран 5.
2) Перекрыть кран 5. Кран 4 поставить в положение, при котором сжатый воздух из компрессора будет поступать в ресивер.
3) Включить электродвигатель компрессора и, наблюдая за показанием чашечного манометра, закачать воздух в ресивер до давления, требуемого в опыте рИЗБ.1. Каждая серия опытов производится 3 раза для различных начальных давлений. Общее количество опытов равно 9. Численные значения начальных давлений принять равными 800, 700 и 600 мм вод.ст. (примерно 8, 7 и 6 кПа соответственно)
4) По достижении заданного давления рИЗБ.1 поворотом крана 4 направить воздушный поток от компрессора в атмосферу. Отключить электродвигатель.
5) Выждав 5…7 минут, необходимых для охлаждения сжатого воздуха до температуры окружающей среды (о наступлении этого момента будет свидетельствовать установившееся показание манометра рИЗБ.2). Записать значение давления РИЗБ.2 в протокол.
6) Открыть кран 5 на время не более 2 секунд и выпустить сжатый воздух из ресивера в атмосферу. При этом рИЗБ.3 станет равным нулю (рИЗБ.3 =0). Закрыть кран.
7) После 5…7 минут охладившийся при адиабатном расширении воздух прогреется до температуры окружающей среды и давление повысится до РИЗБ.4, значение которого занести в протокол.
6.6. Обработка полученных данных и оформление отчета
1) Для каждого опыта определить абсолютное давление воздуха в начале изохорного процесса снижения давления с отводом теплоты (РАБС.1), в начале адиабатного расширения РАБС.2, в конце адиабатного расширения рАБС.3, в конце изохорного повышения давления с подводом теплоты РАБС.4 по следующей формуле:
 , Па (6.12)
, Па (6.12)
где рБАР – атмосферное давление, Па;
рИЗБ.i – избыточное давление по манометру, мм вод. ст.
2) Используя выражение (6.11) вычислить значение показателя адиабаты k:
 (6.13)
(6.13)
3) Определить среднее значение показателя адиабаты воздуха для серии проводимых опытов:
 (6.14)
(6.14)
где n – количество опытов.
6.7. Оформление отчета
Отчет по работе должен включать цель работы, задачи работы, схему установки, данные замеров, расчеты. Данные экспериментов свести в таблицу опытных данных (табл. 6.1.)
Таблица 6.1.
Опытные данные
| № опыта | Давление в ресивере | Показатель адиабаты ki | |||||||
| по манометру, мм вод. ст. | абсолютное давление, Па | ||||||||
| рИЗБ.1 | рИЗБ.2 | рИЗБ.4 | рАБС.1 | рАБС.2 | рАБС.3 | рАБС.4 | рБАР | ||
| … | |||||||||
6.8. Контрольные вопросы
1. Что представляет собой адиабатный процесс идеального изменения состояния газа?
2. Как зависят между собой k, CР, CV.
3. От каких параметров состояния идеального и реального газов зависит k?
4. Как влияет температура на значение k идеального и реального газов?
 2017-10-25
2017-10-25 6696
6696








