Определение массовых долей ионов кальция и магния при совместном присутствии в растворе
Краткое теоретическое вступление: Определение основано на титровании раствора, содержащего ионы кальция и магния, стандартным раствором ЭДТА с двумя индикаторами - эриохромом черным Т и мурексидом. С эриохромом черным Т титруется сумма кальция и магния; затем с мурексидом в щелочной среде - только кальций. Разность объемов, затраченных на титрование смеси с разными индикаторами,, соответствует содержанию магния в растворе.
Цель: определить содержание кальция и магния.
Реактивы: Этилендиаминтетраацетат натрия двузамещенный - 0,05н раствор;
Аммиачный буферный раствор;
Гидроксид натрия NaOH - 20%-й раствор;
Эриохром черный Т (кр.). Мурексид (кр.).
Ход выполнение. Анализируемый раствор в мерной колбе вместимостью 100 мл разбавляют водой до метки, перемешивают и отбирают пипеткой 10 мл раствора для титрования.
В первой пробе определяют сумму кальция и магния. Для этого разбавляют раствор в колбе для титрования 70-80 мл дистиллированной воды, добавляют 5 мл аммиачного буферного раствора и индикатора эриохрома черного Т до образования винно-красной окраски. После этого медленно титруют 0,05 н раствором ЭДТА до изменения окраски из винно-красной в синюю (V1).
К другой пробе прибавляют 70-80 мл воды, 2 мл 20%-го раствора NaOH и индикатора мурексида до образования красной окраски. Затем титруют 0,05 н раствором ЭДТА до появления фиолетовой окраски. Затраченный объем ЭДТА соответствует содержанию кальция (V2).
Обработка результатов:
| V1(ЭДТА) при титровании с эриохромом | V2(ЭДТА) при титровании с мурексидом |
| … | … |
| … | … |
| … | … |
Массу кальция и магния в растворе рассчитывают по формулам:
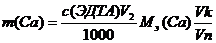
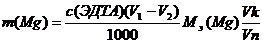
Где: с(ЭДТА) – нормальная концентрация раствора комплексона -3;
V1(ЭДТА) – средний объем комплексона – 3, пошедший на титрования кальция и
магния;
V2(ЭДТА) – средний объем комплексона – 3, пошедший на титрования кальция;
Vк – объем колбы;
Vп – объем аликвоты.
Выводы:
 2018-01-21
2018-01-21 1058
1058








