Кафедра химии
По дисциплине «Аналитическая химия»
по теме:
ОПТИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
Специальность 1 - 49 01 02«Технология хранения и переработки животного сырья»
Специализация: 1 - 49 01 02 02 Технология молока и молочных продуктов
Проверил Выполнили
Автушенко В.В. студенты группы ТЖМ – 101
___________________________ _______________________________
«_____» ______________ 2011 г. _______________________________
_______________________________
«_____» ____________________ 2011 г.
Могилев 2011
Лабораторная работа № 1
Фотоэлектроколориметрическое определение ионов Fe3+ в виде роданидного комплекса
Теоретические основы метода
Фотоэлектроколориметрия основана на поглощении света определяемым веществом в видимой части спектра (400–760 нм). Интенсивность светового потока при его прохождении через исследуемую среду уменьшается вследствие превращения энергии излучения в различные формы внутренней энергии вещества и (или) в энергию вторичного излучения. Поглощательная способность вещества зависит от электронного строения атомов и молекул, а также от длины волны и поляризации падающего света, толщины слоя, концентрации вещества, температуры. Для измерения поглощательной способности в данном методе используют фотоэлектроколориметры – оптические приборы, состоящие из источника света, камеры для образцов, монохроматора (призма или дифракционная решетка) и детектора.
Применение фотоэлектроколориметрии основано на основном законе светопоглощения, или законе Бугера-Ламберта-Бера, который связывает уменьшение интенсивности света с концентрацией раствора и толщиной слоя. Согласно закону Бугера-Ламберта-Бера, растворы одного и того же окрашенного вещества при одинаковой концентрации этого вещества и одинаковой толщине слоя раствора поглощают равное количество световой энергии, т.е. светопоглощение таких растворов одинаково.
Этот закон выражается уравнением:
 1
1
где I – интенсивность света прошедшего через раствор; I 0 – интенсивность падающего на раствор света; ε – молярный коэффициент поглощения; С – молярная концентрация окрашенного вещества в растворе, моль/л; l – толщина слоя светопоглощающего раствора, см.
После логарифмирования и смены знаков на обратные, уравнение (1) принимает следующий вид:
 2
2
Величина lg I 0/ I является важной характеристикой окрашенного раствора; ее называют оптической плотностью и обозначают буквой D или А, тогда:
 3
3
Из этого уравнения следует, что оптическая плотность раствора прямо пропорциональна концентрации окрашенного вещества и толщине слоя раствора.
Для определения концентрации анализируемого иона обычно используют следующие методы: метод добавок и метод калибровочного графика.
Метод добавок основан на сравнении оптической плотности исследуемого раствора и того же раствора с добавкой известного количества стандартного раствора определяемого вещества. Для определения неизвестной концентрации используют два способа.
1. Расчет по уравнению:
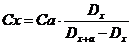 4
4
где С а – концентрация добавки в фотометрируемом растворе; D х – оптическая плотность исследуемого раствора без добавки стандартного раствора; D х+а – оптическая плотность исследуемого раствора с добавкой стандартного раствора.
2. Графический способ
При определении неизвестной концентрации графическим способом на оси ординат откладывают значения оптической плотности исследуемого раствора D х (без добавки) и оптические плотности исследуемого раствора с двумя добавками D х+а1 и D х+а2, а на оси абсцисс – концентрации добавленного вещества С а1 и С а2 в анализируемом растворе.
Через полученные точки проводят прямую (рисунок 1) до пересечения с осью абсцисс в точке С х. Абсолютное значение отрезка 0Сх выражает неизвестную концентрацию исследуемого раствора.
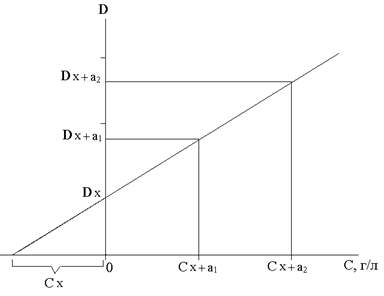 |
| Рисунок 1 – Графическое определение концентрации анализируемого иона методом добавок |
Метод добавок применяют для определения малых количеств различных элементов в присутствии больших количеств посторонних.
Метод калибровочного графика. При использовании метода калибровочного графика готовят серию стандартных растворов с различной концентрацией определяемого иона и измеряют их оптическую плотность. Согласно основному закону светопоглощения между концентрацией C и оптической плотностью D существует прямолинейная зависимость, причем, если С = 0, то и D = 0 (рисунок 2):
 |
| Рисунок 2 – Калибровочный график для определения концентрации анализируемого иона методом фотоэлектроколориметрии |
Измерив оптическую плотность исследуемого раствора D х, находят ее значение на оси ординат, а затем на оси абсцисс соответствующее значение С х.
Метод калибровочного графика применяют при выполнении серийных анализов. Этот метод позволяет определить концентрацию растворов даже в том случае, когда основной закон светопоглощения не соблюдается.
1.2 Цель работы: определить содержание Fe3+ в виде роданидного комплекса в растворе методом калибровочного графика.
1.3 Приборы и реактивы:
Фотоэлектроколориметр ФЭК–56 с набором кювет или фотометр КФК–3; стандартный раствор хлорида железа (III) с концентрацией 1 г/л; раствор соляной кислоты (1:1); 5% раствор роданида аммония (NH4CNS) или роданида калия (KCNS); мерные колбы объемом 50 мл; градуированная пипетка объемом 1 мл; мерный цилиндр.
 2018-02-14
2018-02-14 1219
1219







