Вода – весьма распространенное на Земле вещество. Почти ¾ поверхности земного шара покрыты водой, образующей океаны, моря, реки и озера. Много воды находится в газообразном состоянии в виде паров в атмосфере; в виде огромных масс снега и льда лежит она круглый год на вершинах высоких гор и в полярных странах. В недрах земли также находится вода, пропитывающая почву и горные породы.
Вода обладает рядом специфических свойств по сравнению с другими жидкостями. Эти свойства, известные под названием аномалии воды, определяются строением ее молекул и характером молекулярного взаимодействия.
Приведем главнейшие из этих аномалий.
Плотность дистиллированной воды при увеличении температуры от 0 до 100°С имеет максимум (при температуре 4°С), в то время как у других жидкостей она постоянно уменьшается. В соответствии с плотностью при температуре от 0 до 4°С объем воды уменьшается, а затем, при повышении температуры, увеличивается.
При замерзании вода расширяется, а не сжимается, как все другие жидкости. Плотность льда при 0°С примерно на 10% меньше плотности воды при этой температуре.
Примечание. Если бы при понижении температуры и при переходе из жидкого состояния в твердое плотность воды изменялась так же, как это происходит у подавляющего большинства веществ, то при приближении зимы поверхностные слои природных вод охлаждались бы до 0°С и опускались на дно, освобождая место более теплым слоям, и так продолжалось бы до тех пор, пока вся масса водоема не приобрела бы температуру 0°С. Далее вода начинала бы замерзать, образующиеся льдины погружались бы на дно, и водоем промерзал бы на всю глубину. При этом многие формы жизни в воде были бы невозможны. Но так как наибольшей плотности вода достигает при 4°С, то перемещение ее слоев, вызываемое охлаждением, заканчивается при достижении этой температуры. При дальнейшем понижении температуры охлажденный слой, обладающий меньшей плотностью, остается не поверхности, замерзает и тем самым защищает лежащие ниже слои от дальнейшего охлаждения и замерзания.
Температура замерзания воды с увеличением давления понижается, а не повышается, как это следовало бы ожидать.
Примечание. Этой аномалией можно объяснить существование жидкой воды на больших глубинах в морях при температуре, значительно ниже 0°С.
Температура замерзания (0°С) и кипения (100°С) дистиллированной воды аномальна по сравнению с температурой гидридов, входящих в одну с кислородом группу Периодической системы Д.И.Менделеева: серы — H2S, селена — H2Se, теллура — H2Te. В соответствии с температурой замерзания и кипения этих гидридов следовало бы ожидать замерзание воды при - 90°С, а кипение при - 70°С.
Вода способна к значительному переохлаждению, т. е. может оставаться в жидком состоянии при температуре значительно ниже температуры плавления льда.
Удельная теплоемкость воды (4,18 Дж/(г×К)) в 5 — 10 раз больше удельной теплоемкости других природных веществ. Укажем для сравнения значения удельной теплоемкости некоторых веществ (Дж/(г×К)): песок 0,79; известняк 0,88; хлорид натрия 0,88; глицерин 2,43; этиловый спирт 2,85. Лишь у немногих веществ (литий, древесина) она несколько приближается к удельной теплоемкости воды.
Примечание. Благодаря высокой теплоемкости вода является мощнейшим энергоносителем на нашей планете. Поэтому в ночное время, а также при переходе от лета к зиме вода остывает медленно, а днем или при переходе от зимы к лету так же медленно нагревается, являясь, таким образом, регулятором температуры на земном шаре.
Удельная теплоемкость воды уменьшается при повышении температуры, тогда как у других веществ (кроме ртути) она увеличивается. При этом уменьшение удельной теплоемкости воды происходит при температуре от 0 до 37°С, а затем она увеличивается (у ртути она непрерывно уменьшается).
Удельная теплота плавления льда необыкновенно высокая и в среднем равна 333·103 Дж/кг. Вода и лед при 0°С различаются между собой по содержанию скрытой энергии на 333·103 Дж. С понижением температуры удельная теплота плавления не увеличивается, а уменьшается примерно на 2,1 Дж на 1°С.
Примечание. При плавлении льда объем, занимаемый водой, уменьшается, следовательно, давление понижает температуру плавления льда. Это вытекает из принципа Ле Шателье. Действительно, пусть лед и жидкая вода находятся в равновесии при 0°С. При увеличении давления равновесие, согласно принципу Ле Шателье, сместится в сторону образования той фазы, которая при той же температуре занимает меньший объем. Этой фазой является в данном случае жидкость. Таким образом, возрастание давления при 0°С вызывает превращение льда в жидкость, а это и означает, что температура плавления льда снижается.
Вязкость воды с ростом давления уменьшается, а не увеличивается, как следовало бы ожидать по аналогии с другими жидкостями.
Диэлектрическая проницаемость ε у воды чрезвычайно велика и равна 81 (у льда при t = -5°С εл = 73), тогда как у большинства других веществ она составляет 2—8 и лишь у некоторых достигает 27—35 (спирты).
Примечание. Вследствие этого вода обладает большей растворяющей и диссоциирующей способностью, чем другие жидкости.
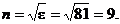 Коэффициент преломления света водой n = 1,333 для длины волны λ=580 нм и при t = 20°С, вместо требуемого теорией значения
Коэффициент преломления света водой n = 1,333 для длины волны λ=580 нм и при t = 20°С, вместо требуемого теорией значения
Удельная теплоемкость водяного пара до температуры t = 500°C отрицательна, т. е. пар при сжатии остается прозрачным, а при разрежении превращается в туман (сгущается).
Удельная теплота парообразования воды при понижении температуры увеличивается, достигая при 0°С очень высокого значения (25,0·105 Дж/кг).
Вода обладает самым высоким поверхностным натяжением среди жидкостей (0,0727 H/м при 20°С), за исключением ртути (0,465 H/м).
 2018-02-20
2018-02-20 2044
2044







