ВЫСШИЕ ПОЛИСАХАРИДЫ.
ГИДРОЛИЗ КРАХМАЛА.
Реактивы и оборудование: 1% раствор крахмала, 10% раствор серной кислоты, раствор Люголя, 10% раствор гидроксида натрия, реактив Фелинга; универсальная индикаторная бумага, конические колбы на 100 мл, пипетки, мерные цилиндры, спиртовки, пробирки.
Ход работы: В коническую колбу на 100 мл вносят 20-30 мл 1% раствор крахмала и 5-7 мл 10% раствора серной кислоты. В восемь пробирок наливают по 1% мл очень разбавленного раствора Люголя. В первую пробирку вносят одну каплю исходного раствора крахмала. Отмечают образовывавшуюся окраску. Затем колбу с реакционной смесью нагревают над небольшим пламенем. Через каждые 3 мин отбирают пипеткой пробу раствора и вносят в пробирку с раствором Люголя. Отмечают постепенное изменение окраски проб при реакции с йодом. Вначале окраска раствора будет интенсивно синей, затем фиолетовой (амилодекстрины), далее от красно-бурой (эритродекстрины) до оранжево-желтой и, наконец, желтой (в дальнейшем эта окраска изменяться не будет). Декстрины расщепляются до дисахарида мальтозы, которая гидролизуется с образованием конечного продукта – D-глюкозы.
Схема гидролиза крахмала:
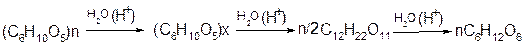
крахмал декстрины D-мальтоза D-глюкоза
После того как реакционная смесь перестанет изменять окраску с йодом, ее кипятят еще несколько минут, охлаждают и нейтрализуют 10% раствором гидроксида натрия (контроль по универсальному индикатору). Отливают в пробирку 2 мл гидролизата и добавляют 2 мл реактива Фелинга. Верхнюю часть жидкости нагревают на пламени горелки до начинающегося кипения. Выпадает красный осадок оксида меди (I), что свидетельствует о наличии в растворе продуктов глубокого гидролиза крахмала – глюкозы и мальтозы.
Лабораторная работа №13.
ВЫДЕЛЕНИЕ ГЛИКОГЕНА ИЗ ПЕЧЕНИ.
Реактивы и оборудование: свежая печень животного, 5% раствор ТХУ (трихлоруксусная кислота), 1% раствор крахмала, раствор Люголя; ступка, пестик, стеклянный порошок, пробирки.
Ход работы: 0,5 г печени помещают в ступку, насыпают в ступку немного стеклянного песка и растирают пестиком. Затем добавляют 3 мл 5% раствора ТХУ и растирают еще 10 мин. После этого в ступку наливают 5 мл дистиллированной воды, суспензию перемешивают и фильтруют.
Фильтрат переливают в пробирку, во вторую пробирку наливают равный объем раствора крахмала. В обе пробирки добавляют по несколько капель раствора Люголя.
Пробирки с крахмалом и гликогеном нагревают и наблюдают изменение окраски. Затем обе пробирки охлаждают и наблюдают возвращение исходной окраски.
Синюю окраску с йодом дает амилоза – одна из фракций крахмала. Амилоза – полисахарид линейного строения, состоящий из остатков a, D-глюкопиранозы. Ее молекулы имеют структуру спирали, внутри которой есть свободный канал диаметром около 5 мкм, в него внедряются молекулы йода, образуя окрашенные комплексы («соединения включения») за счет взаимодействия с гидроксильными группами моносахаридных остатков. При нагревании молекулы амилозы теряют свою спиралевидную структуру, и окрашенные комплексы разрушаются. При охлаждении спиральная структура амилозы и, следовательно, окрашенные комплексы восстанавливаются. Гликоген относится к полисахаридам с разветвленными цепями. Для них большое значение имеет процесс адсорбции йода на поверхности боковых цепей. Если боковые цепи короткие, то развивается бурая окраска, если длинные, то темно-красная.
КАРБОНОВЫЕ КИСЛОТЫ.
Лабораторная работа №9.
НЕПРЕДЕЛЬНЫЕ КАРБОНОВЫЕ КИСЛОТЫ.
 2020-07-01
2020-07-01 1153
1153








