Естественное и антропогенное загрязнение окружающей среды
Под загрязнением окружающей среды понимают любое внесение в ту или иную экологическую систему несвойственных ей живых или неживых компонентов, физических или структурных изменений, прерывающих или нарушающих процессы круговорота или обмена веществ, потоки энергии со снижением продуктивности или разрушением данной экосистемы.
Загрязнения биосферы подразделяют на локальные, региональные и глобальные. Локальные загрязнения характерны для городов, крупных промышленных предприятий, районов добычи полезных ископаемых.
Региональные загрязнения охватывают значительные территории и акватории, подверженные влиянию крупных промышленных районов.
Глобальные загрязнения распространяются на большие расстояния от места своего возникновения и оказывают неблагоприятное воздействие на крупные регионы, иногда на всю планету.
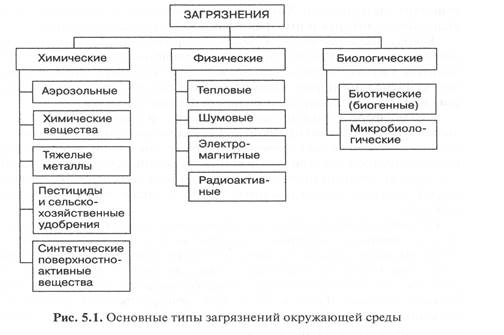
По происхождению выделяют естественное загрязнение, возникшее в результате мощных природных процессов (извержения вулканов, лесных пожаров, выветривания и пр.) и антропогенное, являющееся результатом деятельности человека. Загрязнения также подразделяются на три основных типа:
· химическое,
· физическое и
· биологическое (рис. 5.1).
Загрязнители, поступающие в окружающую среду, подвергаются воздействию естественных физико-химических процессов, в результате чего могут рассеиваться на большие расстояния от их источника, образовывать соединения с другими компонентами среды, активировать процессы в биосфере. Антропогенное воздействие на биосферу вызывает не только ее загрязнение, но и разрушение из-за несбалансированности биохимических процессов. Масштабы антропогенных воздействий напрямую связаны с развитием цивилизации. Из биосферы ежегодно извлекаются миллиарды тонн ископаемых ресурсов для производства 1,3 млрд т стали и других металлов. Ежегодно в биосферу поступает:
| Загрязнения биосферы | млрд т |
| твердых отходов, | 17,4 |
| минеральных удобрений, | 500 |
| пестицидов, | 5 |
| синтетических материалов | 60 |
| жидких стоков, | 500 млн м3 |
| СО2, | 20 млрд м3 |
| SО2 | 150 млн м3 |
| и других химических веществ, число которых составляет более 100 тыс. наименований | |
Создание искусственной среды обитания с развитием инфраструктуры крупных городов (урбанизация) усиливает масштабы антропогенного воздействия.
Химическое загрязнение
Химическое загрязнение связано с увеличением количества химических компонентов определенной среды, а также проникновение (введение) в нее химических веществ в концентрациях, превышающих норму или свойственных ей. Наиболее опасны для природных экосистем и человека именно химические загрязнения, поставляющие в окружающую среду различные токсиканты —
| · аэрозоли, |
| · химические вещества, |
| · тяжелые металлы, |
| · пестициды, |
| · пластмассы, |
| · поверхностно-активныевещества (ПАВы, детергенты). |
Химические загрязнения в настоящее время являются лимитирующими факторами развития цивилизации.
| Аэрозольные загрязнения. Аэрозоли — аэродисперсные (коллоидные) системы, в которых долгое время во взвешенном состоянии могут находиться твердые частицы (пыль), капельки жидкости, образующиеся при конденсации паров, взаимодействии газовых сред или попадающие в воздушную среду без изменения фазового состава |
.
В атмосфере аэрозольные загрязнения воспринимаются в виде дыма, тумана. По своему происхождению аэрозоли подразделяются на естественные и искусственные. Первые поступают в тропосферу, реже в стратосферу при извержении вулканов, сгорании метеоритов, возникновении пылевых бурь, поднимающих с земных поверхностей частицы почвы и горных пород, а также лесных и степных пожарах.
Основными источниками искусственных аэрозольных загрязнений воздуха являются тепловые электростанции, которые потребляют уголь высокой зольности, обогатительные фабрики, металлургические, цементные, магнезитовые и сажевые заводы. Аэрозольные частицы от этих источников отличаются большим разнообразием химического состава. Чаще всего в них обнаруживаются соединения кремния, кальция и углерода (несгоревший уголь, сажа, смола); реже — оксиды металлов, а также асбест.
Еще большее разнообразие свойственно органической пыли, включающей алифатические и ароматические углеводороды, соли кислот. Она образуется при сжигании остаточных нефтепродуктов, в процессе пиролиза на нефтеперерабатывающих и других подобных предприятиях.
Для сравнительной характеристики участия естественных и искусственных источников загрязнения воздуха твердыми частицами в табл. 5.1 приведены данные о поступлении в атмосферу первичных загрязнителей. Там же представлены сведения о вторичных загрязнителях, связанных с новообразованиями в атмосфере.
Независимо от происхождения и условий образования аэрозоль, содержащий твердые частицы размером менее 5,0 мкм, называется дымом, а содержащий мельчайшие частицы жидкости — туманом.
Время пребывания частиц в атмосфере зависит как от их размеров и плотности, так и от состояния атмосферы (скорости ветра, состава, температуры). Мелкие частицы (размер частицы меньше 1 мкм) имеют время пребывания в нижних слоях атмосферы 10—20 суток, что достаточно для их распространения на большие расстояния от источников образования.
Атмосферная пыль и аэрозоли ослабляют солнечное излучение в результате рассеяния, отражения и поглощения лучистой энергии, При достаточно длительном сохранении интенсивных загрязнений атмосферы это приводит к понижению температур и локальным изменениям климатических условий, что наиболее заметно в крупных городах и промышленных центрах.
Пыль и аэрозоли играют негативную роль в процессах коррозии металлических и силикатных материалов из-за образования на поверхностях отложений,
Пылевые и аэрозольные загрязнения атмосферы оказывают заметное влияние на здоровье человека, состояние флоры и фауны. Снижение потока солнечного излучения уменьшает образование под действием УФ-лучей витамина D3. В зонах интенсивных пылевых загрязнений возникает ряд специфических заболеваний (силикоз и асбестоз, приводящие к изменению тканей легких).
| Твердые частицы, поступающие в атмосферу | Таблица 1 |
| Загрязнители | Масса, млн т/год |
| Естественные источники | |
| Первичные загрязнители | |
| Частицы почвы и горных пород (ветровая эрозия) | 100—500 |
| Зола от лесных пожаров и сжигания сельскохозяйственных отходов | 3—150 |
| Морская пыль | 300 |
| Вулканическая пыль | 20—150 |
| Вторичные загрязнители | |
| Сульфаты | 130—200 |
| Соли аммиака | 80—270 |
| Нитраты | 60—430 |
| Углеродные соединения растительного происхождения | 75—200 |
| ИТОГО по естественным источникам | 768— 1 900 |
| Искусственные источники | |
| Первичные загрязнители | |
| Частицы в составе промышленных выбросов | 10—90 |
| Вторичные загрязнители | |
| Сульфаты | 130-200 |
| Нитраты | 30—35 |
| Углеводородные соединения | 15—90 |
| ИТОГО по искусственным источникам | 185—415 |
| ВСЕГО по естественным и искусственным источникам | 953—2315 |
Мельчайшие частицы металлов, или ионы металлов, вызывают образование в крови токсических продуктов биохимических реакций. Особенно распространенными заболеваниями являются токсичные отравления свинцом, кадмием, алюминием, бериллием и их соединениями.
Гигроскопические пыли могут обезвоживать поверхности листьев растений, образуя на них корку, что нарушает естественные процессы обмена. Наоборот, пыли, типичные для городов, поглощают инфракрасное излучение, способствуя этим перегреву листьев растений. Все это нарушает нормальный водный и температурный режим и, в конечном счете, снижает активность ферментов фотосинтеза.
Вследствие деятельности человека в атмосферу поступают:
| · углекислый газ СО2, |
| · угарный газ СО, |
| · диоксид серы SО2, |
| · метан СН4, |
| · оксиды азота NO2, NO и N2О, |
| · хлорфторуглероды (при использовании аэрозолей в быту), |
| · углеводороды, бензапирен и др. (в результате работы транспорта). |
Наиболее массовые загрязнители, выбрасываемые всеми техногенными источниками в атмосферу, представлены в табл. 5.2.
Кислотные осадки (дожди) формируются при растворении в воде диоксидов серы и азота. Такие осадки, выпадая на поверхность Земли, имеют показатель кислотности рН < 5,6.
| В целом вода с pH меньше 7 считается кислой, а с рН больше 7 – щелочной. Нормальный диапазон pH для поверхностных водных систем лежит в пределах от 6,5 до 8,5, а для подземных систем – от 6 до 8,5. Читайте подробнее на FB.ru: http://fb.ru/article/153987/zachem-nam-nujno-znat-ph-vodyi |
Основным источником таких выбросов являются продукты сгорания топлива (уголь, мазут, бензин и т.д.) в энергетических установках предприятий, наземного и воздушного транспорта, выбросы химических и металлургических предприятий.
Время пребывания SО2 в атмосфере в среднем составляет около 15 дней. Благодаря своей активности SО2 в атмосфере претерпевает ряд химических превращений, главное из них — окисление и образование Н2SО4. При этом кислотные пары могут разноситься с облаками на сотни километров (до 1500 км) до мест выпадения их с осадками.
Кислотные соединения азота (N0, NO2) от антропогенных источников:
| · энергетики (57,0%), |
| · транспорта (38,5%), |
| · промышленности (4,5%) |
— служат источниками образования атмосферной азотной кислоты.
Кислотные осадки антропогенного происхождения заметно изменили рН окружающей среды. Около 150 тыс. лет назад при образовании ледяного покрова Гренландии рН осадков составляла 6,0—7,6 (по результатам анализов полярных льдов и горных глетчеров). Во второй трети XX в. рН атмосферных осадков составляла:
· 4,0—4,5 в Германии и странах Бенилюкса,
· 2,4—2,7 в Шотландии и Норвегии,
· 4,0— 4,5 в США и Японии.
По оценкам специалистов, заметных изменений во вкладе в кислотные осадки со стороны природных процессов в последние сотни лет не происходило.
Показатель кислотности среды чрезвычайно важен для жизнедеятельности практически всех организмов. Негативные последствия проявляются при значениях рН < 5,5. Все нормальные формы жизни прекращаются при значениях рН < 5. Кислотные осадки вызывают деградацию лесов, особенно хвойных. При взаимодействии с почвенным покровом усиливаются процессы выщелачивания биогенов. При рН < 4 резко снижается активность редуцентов и азотфиксаторов, обостряется дефицит питательных веществ, почвы становятся неплодородными. Под действием кислотных осадков существенно ускоряется:
· коррозия металлов, нарушается
· целостность лакокрасочных покрытий,
· стекол,
· разрушаются здания,
· памятники архитектуры.
Среди вредных веществ, содержащихся в воздухе городов, имеется большая группа, обладающая канцерогенной активностью. Это в первую очередь бензапирен и другие ароматические углеводороды, поступающие от котельных промышленных предприятий и с выхлопными газами автотранспорта.
Быстрыми темпами нарастает в атмосфере содержание:
· двухатомных газов с несимметричной молекулой (СО, НСI и др.),
· трехатомных газов (Н2О, СО2, SО2) и
· газов с числом атомов больше трех (NН3, СН4 и др.).
Эти газы обусловливают парниковый эффект.
Солнечная радиация, падающая на Землю, частично поглощается поверхностью суши и океана, 30% ее отражается в космическое пространство. Поглощенная энергия солнечной радиации преобразуется в теплоту и излучается в космос в диапазоне длин волн инфракрасного излучения (ИК-излучение). Чистая атмосфера прозрачна для ИК-излучения, а атмосфера, содержащая пары парниковых газов, поглощает инфракрасные лучи, благодаря чему происходит ее разогрев. Поэтому парниковые газы можно уподобить стеклянному покрытию в обычных садовых парниках.
| Загрязнители, выбрасываемые всеми техногенными источниками в атмосферу Земли (90-е гг. XX столетия) | Табл.2 |
| Загрязнитель | Масса, млн т/год |
| Твердые частицы дыма и промышленная пыль | 580 |
| Оксиды углерода | 360 |
| Летучие углеводороды и другая органика | 320 |
| Оксиды серы | 160 |
| Оксиды азота | 110 |
| Соединения фосфора | 18 |
| Сероводород | 10 |
| Аммиак | 8 |
| Хлор | 1 |
| Фтористый водород | 1 |
Начиная с XVIII в. природное равновесие содержания парниковых газов в атмосфере, претерпело серьезные нарушения. За 250 лет содержание метана в атмосфере увеличилось в 3 раза вследствие антропогенного влияния.
Рост концентрации СО2 сначала происходил из-за массовой вырубки лесов, потреблявших углекислый газ на синтез биомассы растений. С начала XIX в. определяющую роль приобретают выбросы СO2 с продуктами сжигания ископаемого топлива, технологических и попутных газов.
Из антропогенных источников поступления СО2 в атмосферу наибольшую долю составляют предприятия энергетики и металлургии, транспорт, использующий двигатели внутреннего сгорания.
Рост населения планеты и интенсивное разведение домашних животных привели к тому, что биологический вклад (аэробное дыхание, разложение органических остатков) в увеличение концентрации СO2 в атмосфере стал соизмеримым с промышленными выбросами.
Увеличение содержания СО2 в атмосфере на 60% по сравнению с современным уровнем приведет к повышению температуры земной поверхности на 1,2-2 °С; это значит, что если до 2050 г. потребление ископаемого топлива не сократится, то концентрация СО2 в атмосфере возрастет вдвое, а температура поверхности Земли увеличится на 3°С.
К сожалению, возрастает дополнительный вклад в парниковый эффект таких газов, как N02, SО2, NH3, СН4, фреонов и других органических веществ. Опережающими темпами растет содержание в атмосфере СН4 и NН3. Установлено, что если темпы роста концентрации в атмосфере газов, дающих дополнительный вклад в парниковый эффект, сохранятся на сегодняшнем уровне, то к 2020 г. их действие будет эквивалентно удвоению концентрации СО2 в атмосфере.
Потепление на Земле, по мнению климатологов, за счет роста температуры на 0,1 °С считается значительным, а увеличение температуры на 3,5 °С — критическим.
Развитие процессов в биосфере во многом зависит от состояния озонового экрана. Верхние слои атмосферы в значительной степени определяют условия жизни на Земле. Они являются защитным барьером на пути излучений и частиц высоких энергий из космоса. Особую опасность для биосферы представляет жесткое ультрафиолетовое излучение Солнца в диапазоне длин волн λ < 310 нм.
Известно, что более 99% ультрафиолетового излучения Солнца поглощается слоем озона (О3) на высоте 25 км (в среднем) от поверхности Земли.
Основные источники NО Х антропогенного происхождения — двигатели внутреннего сгорания, высокотемпературные энергетические установки, в которых сжигается топливо, ракеты и сверхзвуковые самолеты.
Атомарный хлор образуется в результате фотохимического разрушения фреонов (фторхлорметанов): СF2СI2 и СFСI3. Эти вещества чисто антропогенного происхождения летучи и устойчивы в тропосфере. Их источником являются холодильные установки и аэрозольные баллоны. С момента промышленного применения в 50-е гг. XX в. содержание фреонов в атмосфере увеличивалось на 5—10% в год.
В настоящее время учеными обнаружены зоны стратосферы с существенно сниженным содержанием озона. Такая озоновая «дыра» зафиксирована над Антарктидой в весенние месяцы года.
Уменьшение озонового слоя, средняя толщина которого составляет 2,5—3,5 мм, может привести к изменениям облачного покрова Земли, нарушению теплового баланса атмосферы. Рост мощности ультрафиолетового излучения, достигающего поверхности Земли, может оказать существенное влияние на биологические и геохимические процессы.
Среди химических загрязнителей воды наибольшую опасность представляют:
| · фенолы, |
| · нефть, |
| · нефтепродукты, |
| · тяжелые металлы, |
| · пестициды. |
Загрязнение Мирового океана связано главным образом с поступлением огромного количества вредных антропогенных веществ на его акватории.
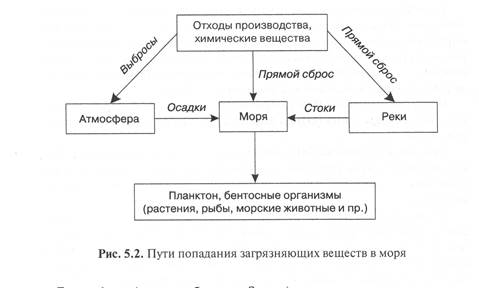
В настоящее время в водные объекты ежегодно поступает более 30 тыс. различных химических соединений в количестве до 1,2 млрд т, а всего на поверхность океанов, морей и рек в результате аварий и сбросов поступают нефть и нефтепродукты в количестве, превышающем 12 млн т в год. Каждая тонна нефти образует на воде пленку до 12 км2. Основные пути попадания загрязняющих веществ моря показаны на рис. 5.2.
Гидросфера (водная оболочка Земли) включает ресурсы океанов, морей, рек, озер, прудов, болот и подземных вод. Общее количество воды на Земле достигает 1386 млн км3, а площадь океанов и морей в 2,5 раза больше площади суши. Из общего количества воды на Земле доля пресных вод немногим более 2,5%, т.е. на каждого жителя Земли приходится около 5,8 млн м3. Однако для человека доступно менее 30% этих вод, так как основная их часть сосредоточена в ледниковых покровах (около 27 млн км3), скрыта в подземных образованиях (объем подземных пресных вод примерно в 100 раз больше объема поверхностных вод в озерах, реках, болотах).
Деятельность человека охватывает практически всю акваторию Мирового океана:
| · поверхность служит для мореплавания и рыболовства; |
| · прибрежная зона — для извлечения биологических, минеральных, энергетических ресурсов, интенсивного промышленного и жилищного строительства; |
| · дно — для добычи полезных ископаемых и захоронения отходов. |
В водные объекты поступают загрязненные сточные воды бытового, промышленного происхождения, ядохимикаты и удобрения, смываемые с полей при паводках, загрязненные атмосферные осадки. В результате речных течений и циркуляционных процессов такие загрязнения распределяются на большие пространства и переносятся на сотни и даже тысячи километров.
Человек в своей деятельности расходует воду не только для удовлетворения естественных физиологических потребностей. Вода используется промышленностью и сельским хозяйством во все больших масштабах. При этом значительная ее часть связывается в технологических процессах и безвозвратно теряется. По оценкам ученых такие потери составляют около 150 км3 в год, т.е. более % устойчивого стока пресных вод.
В промышленности вода используется для приготовления растворов, проведения различных реакций нагрева и охлаждения, транспорта сырья, промывки изделий и многих других целей.
| Производство 1 тонны продукта | Расход воды (в м3) |
| Чугуна или стали расходуется | 15—20м3 |
| Кальцинированной соды | 10, |
| серной кислоты | 25—80, |
| вискозного шелка | 300—400, |
| меди — 500, пластических масс | 100—500, |
| синтетического каучука | 2000-3000 м3 |
Тепловая электростанция мощностью 300 МВт потребляет 300 тыс. м3 воды в год, химический комбинат средней мощности имеет суточный водооборот до 2 млн м3 воды. Во все больших масштабах потребляется вода в крупных городах. Так, средний расход воды для города с населением 3 млн человек составляет 2 млн м3 в сутки (соотношение 3:2, т.е. на 1 человека 0,67 млн м3 в сутки). Часть потребляемой воды химически и физически связывается, а часть возвращается в водные объекты в загрязненном агрессивными химическими примесями состоянии.
| Учебно-экспериментальная теплоэлектроцентральМосковского Энергетического ин-та (МЭИ). Запущена в 1950 г. Аналога подобной станции нет ни в одном другом вузе России Единственным топливом для ТЭЦ является природный газ. Единственным топливом для ТЭЦ является природный газ. В 2007 году началась реконструкция ТЭЦ которая должна завершиться до конца 2015 года. Реконструкция ТЭЦ МЭИ предполагает не только увеличение установленной мощности, но и существенно более высокие характеристики их экологической безопасности. После реконструкции установленная мощность ТЭЦ МЭИ будет доведена до 14,5-15,3 МВт; максимальная тепловая нагрузка 20 МВт (потребляет 20 тыс. м3 воды). Реконструкция ТЭЦ МЭИ предполагает не только увеличение установленной мощности, но и существенно более высокие характеристики их экологической безопасности. |  |
Продуктами жизнедеятельности человека и отходами ряда производств являются органические соединения, которые поступают в водные объекты со сточными водами или в результате фильтрации через грунты. Их разложение осуществляется в результате деятельности аэробных микроорганизмов. В процессах брожения при интенсивном потреблении кислорода, растворенного в воде, образуются СО2, Н2О, а также нитраты, фосфаты, сульфаты и кислородсодержащие соединения других элементов. Это, с одной стороны, приводит к интенсивному разложению водорослей и растений, что стимулирует рост зоопланктона и внешней фауны, потребляющей кислород для дыхания. С другой стороны, возникающий дефицит кислорода вызывает массовую гибель аэробных организмов и размножение анаэробных микроорганизмов, разрушающих биомассу путем брожения.
Другими органическими загрязнителями являются фенолы, их галогенсодержащие соединения, которые попадают в водные объекты со стоками предприятий по производству клеев, пластмасс, кокса, весьма опасны органические растворители, широко применяемые в Различных химических технологиях (например, хлорированные углеводороды).
Нефть и нефтепродукты попадают в водные объекты при бурении скважин, потерях при транспортировке, авариях танкеров, в результате сливов при промывании емкостей. На воде нефть образует тонкие пленки, создающие со временем эмульсионный слой нефть-вода, покрывающий до 20-30% поверхности Мирового океана. Этот слой препятствует газообмену между водой и воздухом, что приводит к повышению в клетках водных организмов содержания СО2 и их гибели. Микробиологический распад нефти идет неделями и даже месяцами. Нефтепродукты отрицательно воздействуют на гидробиоценозы, так как аккумулируются в морской биоте, передаваясь по трофическим цепям. Потребление таких морепродуктов создает угрозу здоровью людей. В морскую среду ориентировочно поступает около 12 млн т нефти и нефтепродуктов, которые распространяются по акватории весьма неравномерно (табл. 5.3).
Таблица 5.3 Концентрация нефтепродуктов в районах Мирового океана
| Акватория | Концентрация,мкг/л |
| Тихий океан, северо-западная часть | 0-200 |
| Атлантический океан, северо-восточная часть | 0-160 |
| Северное море | 0-350 |
| Средиземное море | 0-950 |
| Балтийское море | 800-8000 |
Тяжелые металлы. Особое значение приобрело загрязнение биосферы группой загрязнителей (поллютантов), получивших общее название «тяжелые металлы». К ним относится более 40 химических элементов периодической системы Д.И, Менделеева (хром, марганец, железо, кобальт, никель, медь, цинк, галлий, германий, молибден, кадмий, олово, сурьма, теллур, вольфрам, ртуть, таллий, свинец, висмут и т.д.).
Поступление тяжелых металлов в биосферу вследствие техногенного рассеивания осуществляется разнообразными путями. Важнейшим является их выброс при высокотемпературных процессах в черной и цветной металлургии, при обжиге цементного сырья, сжигании минерального топлива.
Часть техногенных выбросов тяжелых металлов, поступающих в атмосферу в виде аэрозолей, переносится на значительное расстояние и вызывает глобальное загрязнение. Другая часть с гидрохимическим стоком попадает в бессточные водоемы, где накапливается в водах и донных отложениях и может стать источником вторичного загрязнения.
Значительное загрязнение тяжелыми металлами, особенно свинцом, а также цинком и кадмием обнаружено вблизи автострад. Ширина придорожных аномалий свинца в почве достигает 100 м и более.
Растения могут поглощать из почвы микроэлементы, в том числе тяжелые металлы, аккумулируя их в тканях или на поверхности листьев, являясь, таким образом, промежуточным звеном в цепи «почва — растение — животное — человек».
Пестициды. Пестициды (pestis — «зараза», caedo — «убивать») — средства защиты растений от вредителей и болезней. В настоящее время используется около 700 химических веществ, из которых создается несколько тысяч препаратов пестицидов. Пестициды — единственный загрязнитель, который сознательно вносится человеком в окружающую среду.
Хлорорганические инсектициды (гексахлоран, ДДТ) обычно слабо растворимы в воде, очень устойчивы ко всем видам разложения и могут сохраняться в почве десятилетиями, аккумулируясь при систематическом применении.
Фосфорорганические инсектициды (карбофос, фосфамид, амифос) в почве и других природных средах распадаются довольно быстро. При этом они отличаются эффективностью действия и их применение перспективно. Широко используются карбамидные инсектициды. Отличаясь высокой токсичностью для определенных видов насекомых, эти препараты почти полностью безвредны для человека.
Почва является основным приемником и аккумулятором пестицидов, которые накапливаются в ней в результате адсорбции их молекул почвенными коллоидами. Очень важно создавать и применять только препараты с небольшой продолжительностью жизни, измеряемой неделями или месяцами. В этом деле уже достигнуты определенные успехи, испытываются и внедряются в практику новые быстрорастворимые препараты с большой скоростью метаболической Деструкции.
Сельскохозяйственные удобрения — вещества, компенсирующие потери элементов почвы, связанные с ростом растений. Для сохранения Почвенной экосистемы на поля следует вносить эквивалентное количество соответствующих элементов. Отсюда успехи сельского хозяйства связаны с минеральными удобрениями и ежегодно увеличивают их количество, вносимое в почву. При этом не все удобрения достигают растений, много их теряется, в частности при вымывании из почвы (Это опасно!).
Например, 5-кратное увеличение количества применяемых азотных удобрений позволило повысить урожайность зерновых культур только на 20%, а содержание нитратов в почве и растениях резко возросло. Сельскохозяйственная продукция, содержащая повышенное количество нитратов, имеет пониженную питательную ценность, теряет устойчивость к длительному хранению.
Другой вид удобрений — фосфорные. Их избыток в почве обогащает фтором и мышьяком растения, что весьма вредно для питающихся ими животных. Значительная доля фосфорных удобрений не усваивается растениями, не вовлекается в биохимический круговорот, а около 5% выносится в водные объекты.
Калийные удобрения (КМО3, К25О4, КСI) в силу высокой растворимости в воде в значительной степени вымываются в сопредельные водоемы в периоды, когда заканчивается начальная стадия развития растений, т.е. потребность их в калии уменьшается.
Наряду с минеральными удобрениями в сельском хозяйстве широко используют органические удобрения (навоз, торф, компост). При большом количестве в почвах таких удобрений, содержащих много патогенных микроорганизмов, и при обогащении водной среды ими создаются условия для возникновения очагов болезнетворных организмов.
Поверхностно-активные вещества. Широкое применение синтетических поверхностно-активных веществ (СПАВ), или детергентов, особенно в составе моющих средств, обусловливают поступление их со сточными водами во многие водоемы, в том числе и в источники хозяйственно-питьевого водоснабжения. В настоящее время эти вещества — одни из самых распространенных химических загрязнителей водоемов.
СПАВ поступают в водоемы с бытовыми, промышленными и сельскохозяйственными стоками (в сельском хозяйстве поверхностно-активные вещества используют для эмульгирования пестицидов).
Поверхностно-активные вещества относятся к экологически жестким веществам. Они очень трудно ассимилируются природной средой и крайне отрицательно влияют на состояние водоемов. Дело в том, что на их окисление расходуется слишком много растворенного кислорода, который таким образом отвлекается от процессов биологического окисления.
Детергенты очень вредны для гидробионтов. У рыб они вызывают жаберные кровотечения и удушье. У теплокровных животных нарушают функции биомембран, усиливая этим токсическое и канцерогенное влияние других токсикантов водной среды.
 2020-07-01
2020-07-01 5628
5628