При нагревании спирта в присутствии концентрированной серной кислоты или хлорида цинка, а также при пропускании паров спирта при 350 – 500 0С через трубку с оксидом алюминия происходит реакция дегидратации (отщепление воды) и образуются алкены.
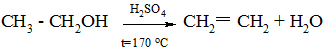
Легче всего дегидратируются третичные, потом вторичные и затем уже первичные спирты. В спиртах сложного строения преимущественно отщепляется от соседнего атома углерода третичный водородный атом, гораздо в меньшей степени – вторичный, и практически не отщепляется первичный (правило Зайцева):
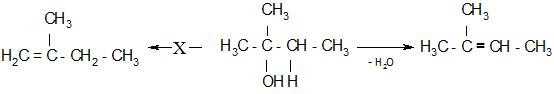 |
Межмолекулярная дегидратация спиртов. Образование простых эфиров
При нагревании избытка спирта с серной кислотой (t = 140 ºС) или при пропускании паров спирта через порошкообразный безводный сульфат алюминия при 200 0С наряду с этиленовыми углеводородами образуются и простые эфиры:
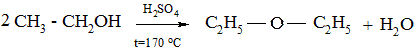
А.Е. Фаворский показал, что при нагревании этиленгликоля с небольшим количеством серной кислоты образуется циклический простой эфир – диоксан, обладащий высокой растворяющей способностью.
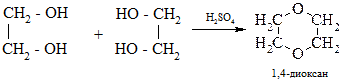
Сложные эфиры, имеющие арильные заместители рядом с атомом кислорода, получают из фенолятов и галогенопроизводных углеводородов.
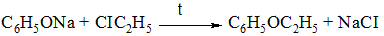
Замена гидроксила на аминогруппу
Гидроксильная группа спиртов в жестких условиях (t = 300 °С, AI2O3) может замещаться на аминогруппу с образованием первичных аминов:
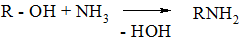
Реакции окисления
Отщепление водорода (дегидрогенизация, дегидрирование). При пропускании паров спирта при 200-300 °С над мелко раздробленной медью или серебром первичные спирты превращаются в альдегиды, а вторичные – в кетоны. При этом наблюдается выделение водорода:
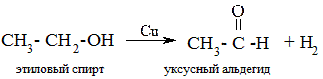
Окисление спиртов. Спирты устойчивы к действию окислителей. Поэтому окисление обычно проводят сильными окислителями, например К2Сr2O7 + H2SO4 или КMnO4 + H2SO4. При окислении спиртов действие окислителя направляется на тот углеродный атом, который уже связан с гидроксильной группой. В зависимости от характера получают различные продукты окисления.
Первичные спирты окисляются до альдегидов.
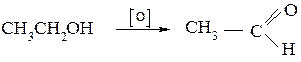
При окислении вторичных спиртов образуются кетоны:
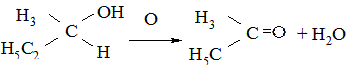
Третичные спирты окисляются только в жестких условиях с разрывом
С–С связей.
Окисление фенолов Легкость окисления фенолов связана с сильным электронодонорным действием гидроксильных групп. Даже при действии кислорода воздуха фенол окисляется и приобретает розовую окраску.
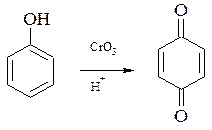 |
Под действием хромовой кислоты фенолы окисляются в хиноны.
 2020-09-24
2020-09-24 154
154








