В 1957 г Ф.Сэнгеру за определение первичной структуры инсулина была присуждена Нобелевская премия по химии. Это был первый белок, для которого удалось установить аминокислотную последовательность, этой работе Сэнгер посвятил 10 лет. В основе его подхода лежал частичный гидролиз пептидных цепей, предварительно помеченных в ходе реакции свободной аминогруппы с фтординитробензолом.
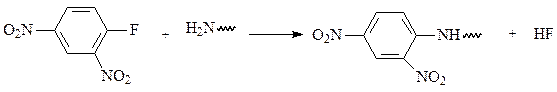
Связь с динитрофенильной группой устойчива к кислоте, и поэтому после полного кислотного гидролиза меченного пептида высвобождалась динитрофенилированная аминокислота желтого цвета, которая находилась на N-конце пептида. Частичный кислотный гидролиз меченных пептидов приводил в этом случае к образованию небольших фрагментов, для которых затем определяли аминокислотный состав. В конце концов Сэнгер сложил фрагменты полученной аминокислотной мозаики и установил последовательность двух цепей молекулы инсулина, содержащий 21 и 30 остатков и связанных между собой в цельной молекуле двумя дисульфидными мостиками.
Анализ чередования аминокислот в белках открыл закономерность – в белках реализуются далеко не все возможные первичные структуры, часто встречаются идентичные пептидные группировки, чаще всего трехпептидные. Кроме того, значительные совпадения первичной структуры характерны для белков, выполняющих сходные биологические функции.
В последние годы вместо фтординитробензола чаще применяют дансил хлорид. Получающиеся в результате пептидные производные сильно флуоресцируют, что позволяет проводить анализ концевых групп со значительно меньшим количеством пептидов.
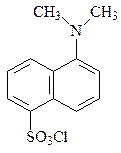
В случае углеводов классическим методом идентификации концевых групп служит исчерпывающее метилирование. Многократная обработка метилирующим агентом, например диметилсульфатом, превращает все свободные ОН-группы в ОСН3-группы. Полный кислотный гидролиз с последующим разделением метилированных сахаров и их количественным определением позволяет оценить число концевых звеньев (содержащих четыре метоксигруппы), число звеньев в неразветвленных участках цепи (содержащих по три метоксигруппы) и число точек ветвления (содержащих по две метоксигруппы).
Сравнительно новым методом маркировки редуцирующих концов углеводных цепей является восстановление альдегидных групп бортритидом натрия (NaB3H4). Введенная таким образом радиоактивная метка дает возможность по радиоавтографам хроматограмм определять положение фрагментов, отщепленных от редуцирующих концов.
Одним из наиболее ценных реагентов, используемых для установления структуры углеводов, является иодная кислота. Под действием иодной кислоты расщепляются С-С-связи, по обе стороны от которых расположены ОН-группы, с образованием диальдегидов. Метод позволяет проводить количественные определения. Через несколько часов после начала реакции избыток периодата удаляют этиленгликолем; можно также определить количество периодата, затраченное в процессе окисления. Если ОН-группы связаны с тремя идущими подряд атомами углерода, то центральный атом отщепляется в составе муравьиной кислоты, количество которой тоже можно точно определить. Помимо этого, после удаления избытка периодата диальдегид можно восстановить добавлением твердого боргидрида натрия с образованием устойчивых СН2ОН-групп и далее с помощью мягкого кислотного гидролиза расщепить ациклические ацетальные связи, разделить полученные фрагменты и провести их модификацию. Эту последовательность реакций называют деградацией по Смиту.
Концевые группы полирибонуклеотидов тоже отщепляют периодатом, предварительно удалив с помощью фосфомоноэстеразы фосфатные группы на 3’-гидроксилах. Образующиеся диальдегиды восстанавливают далее бортритидом натрия. Другой метод включения в полинуклеотиды радиоактивной концевой группы основан на переносе фосфорильной группы с молекул АТФ под действием неспецифической полинуклеотидкиназы с образованием свободной 5’-гидроксильной группы полирибо- или полидезоксирибонуклеотида.
 2014-02-04
2014-02-04 731
731








