1. Люминесценция (от лат. lumen – свет и … escent – суффикс, означающий слабое действие) – излучение, избыточное над тепловым и продолжающееся в течение времени, которое много больше световых колебаний.
Первая часть определения отделяет люминесценцию от теплового равновесного излучения. Тепловое излучение в видимой области спектра заметно только при температуре около тысячи и более градусов. В то время как люминесценция может наблюдаться при любой температуре вплоть до абсолютного нуля. Поэтому люминесценцию называют часто холодным свечением.
Вторую часть определения – признак длительности свечения – ввел Сергей Вавилов, чтобы отделить люминесценцию от разных видов рассеяния и отражения света, а также от тормозного излучения и излучения Черенкова. В отличие от рассеяния света при люминесценции между поглощением и испусканием света происходят промежуточные процессы, длительность которых больше периода световой волны.
Первоначально понятие люминесценция относилось только к видимому свету. В настоящее время оно применяется к излучению в ИК, видимом, УФ и рентгеновском диапазонах. Исторически явление люминесценции сыграло важную роль в развитии физики. Интерес к свечению разных веществ под действием катодных лучей привел К. Рентгена к открытию в 1895 году рентгеновских лучей. В 1896 году А. Беккерель, в продолжение семейной традиции занимавшийся изучением люминофоров, открыл естественную радиоактивность.
Многие формы природной люминесценции были известны людям очень давно. Например, свечение насекомых (светлячки), свечение морских рыб и планктона, полярные сияния, свечение минералов, гниющего дерева и других разлагающихся органических веществ. Однако систематическое изучение люминесценции началось с конца XIX века. В настоящее время к природным формам прибавилось много искусственных способов возбуждения люминесценции. Твердые и жидкие вещества, способные люминесцировать, называют люминофорами (от лат. lumen – свет и греч. phoros - несущий).
Чтобы вещество было способно люминесцировать, его спектры должны иметь дискретный характер, то есть его энергетические уровни должны быть разделены зонами запрещенных энергий. Поэтому металлы в твёрдом и жидком состоянии, обладающие непрерывным энергетическим спектром, не дают люминесценции. Энергия возбуждения в металлах непрерывным образом переходит в тепло. И лишь в коротковолновом диапазоне металлы могут испытывать рентгеновскую флуоресценцию, т.е. под действием рентгеновского излучения испускать вторичные Х -лучи.
2. Способы возбуждения люминесценции. Их много. Перечислим основные:
а. Фотолюминесценция возбуждается светом. В зависимости от того, как быстро атом, поглотивший фотон hn 0, возвращается в стационарное состояние, испуская фотон hn, различают флуоресценцию (время релаксации t» 10-8 с) и фосфоресценцию (t >> 10-8 с). Деление это условно и носит практический характер. Вещества, с длительным послесвечением называют фосфорами.
б. Радиолюминесценция возбуждается проникающей радиацией. Например, при движении частицы в кристалле сернистого цинка ZnSвозникает локальная вспышка – сцинтилляция. Это явление лежит в основе сцинтилляционных счётчиков. Исторически первым таким счётчиком был построеный в 1903 году спинтарископ Крукса.
Сцинтилляционные счётчики позволяют регистрировать и сосчитывать ионизирующие частицы поштучно. В качестве радиолюминофоров в них используются кристаллы антрацена C14H10, а также ZnS, NaI, CsI, органические растворы и пластики.
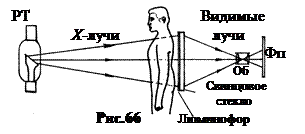 К радиолюминесценции относится также свечение кристаллов под действием Х -лучей. Это делает возможной рентгеновскую диагностику на основе флюорографии – фотографирования на плёнку люминесцентного изображения просвечиваемого Х -лучами объекта (рис.66).
К радиолюминесценции относится также свечение кристаллов под действием Х -лучей. Это делает возможной рентгеновскую диагностику на основе флюорографии – фотографирования на плёнку люминесцентного изображения просвечиваемого Х -лучами объекта (рис.66).
В рентгеноскопии применяют люминофоры на основе (ZnCd)S·Ag и CaWO4, дающие свечение в области максимальной чувствительности глаза и позволяющие максимально использовать чувствительность фотоплёнки, уменьшая тем самым дозу облучения.
в. Катодолюминесценция возбуждается быстрыми электронами. Формально она может быть отнесена к радиолюминесценции, но благодаря её большому техническому значению обычно выделяется в отдельную группу.
Катодолюминесценция применяется в экранах кинескопов телевизоров, осциллографов, мониторов ЭВМ. Для цветных кинескопов разработаны люминофоры, дающие три основные цвета свечения: синий (ZnS·Ag), зелёный (ZnSe·Ag), красный [Zn3(PO4)2·Mn].
г. Из других способов возбуждения люминесценции назовём триболюминесценцию – возбуждение свечения под действием механических деформаций (при раскалывании куска сахара в темноте наблюдается голубоватая вспышка), хемилюминесценцию – возбуждение за счёт энергии химических реакций. Хемилюминесценция в живых организмах, сопровождающаяся видимым свечением, называется биолюминесценций. Последняя наблюдается у некоторых бактерий, грибов, насекомых и рыб. Биолюминесценция связана с процессами жизнедеятельности организмов. Она распространена среди обитателей морей и океанов.
3. Фотолюминесценция. Резонансное излучение. Рассмотрим подробнее свечение тел, возникающее под действием света. В 1904 году Роберт Вуд освещал пары натрия светом от горелки, в пламя которой вводилась поваренная соль NaCl. Благодаря этому в свете горелки присутствовали интенсивные D – линии натрия c l 1 = 589,6 нм и l 2 = 589,0 нм. Оказалось, что освещаемые пары натрия начинали светиться, испуская эти же D – линии с длиной волны l 1 и l 2. Такое же излучение Вуд наблюдал и в парах ртути Hg, освещаемых ртутной лампой. Как в свете лампы, так и в излучении паров Hg наблюдалась линия с l = 253,7 нм, расположенная в УФ области. Этот эффект назвали резонансным излучением. Название вытекает из классического толкования эффекта. Атом возбуждается частотой, равной частоте собственных колебаний, и испускает линию этой частоты.
Резонансное излучение представляет собой частный и наиболее простой случай фотолюминесценции без энергетических потерь. Атом поглощает фотон hn, переходит в возбуждённое состояние и, спустя какое-то время, излучает это же фотон hn.
4. Закон Стокса. Ещё в 1852 году Джордж Стокс, исследуя явление фотолюминесценции установил правило: длина волны фотолюминесценции больше длины волны возбуждающего света.
Закон Стокса можно объяснить тем, что каждый испущенный при люминесценции фотон получается за счёт поглощённого фотона, часть энергии которого А растрачивается на какие-то внутримолекулярные процессы. Так что hn = hn 0 - A. (10.1)
Величина А в большинстве случаев положительна (А > 0, стоксовская область). Но иногда бывает отрицательной (А < 0, антистоксовская область). В последнем случае к энергии возбуждающего фотона hn 0 добавляется тепловая энергия А колебательного движения молекул. В результате энергия hn излучённого фотона получается больше энергии hn 0 поглощённого фотона. С ростом температуры антистоксовская область возрастает.
Закон Стокса был открыт на заре спектрального анализа, когда призменные и дифракционные спектральные аппараты имели малое разрешение. В результате не только свет возбуждения, но и свет люминесценции представлялся в виде широких цветных полос. Поэтому закон Стокса имел, в основном, такой смысл: фиолетовый свет может возбуждать, например, зелёное свечение, но зелёный свет не может возбуждать фиолетовое свечение.
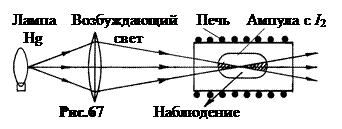 5. Молекулярные спектры. В 1905 году Вуд провёл опыты с парами йода по той же схеме, что и опыты с парами натрия и ртути. Выбор элементов для исследования объяснялся тем, что натрий, ртуть, йод легко испаряются при относительно слабом нагревании. Небольшое количество этого вещества помещалось в эвакуированную кварцевою ампулу, находившуюся в нагревательной печи (рис.67). Меняя температуру в печи, можно изменять давление паров вещества в кварцевом сосуде. Наблюдение люминесцентного излучения велось обычно в направлении, перпендикулярном к возбуждающему пучку.
5. Молекулярные спектры. В 1905 году Вуд провёл опыты с парами йода по той же схеме, что и опыты с парами натрия и ртути. Выбор элементов для исследования объяснялся тем, что натрий, ртуть, йод легко испаряются при относительно слабом нагревании. Небольшое количество этого вещества помещалось в эвакуированную кварцевою ампулу, находившуюся в нагревательной печи (рис.67). Меняя температуру в печи, можно изменять давление паров вещества в кварцевом сосуде. Наблюдение люминесцентного излучения велось обычно в направлении, перпендикулярном к возбуждающему пучку.
В отличие от ртути и натрия, пары йода находятся в молекулярном состоянии I 2. Как уже говорилось в §7, число уровней энергии в молекулах много больше, чем в атомах. Исследование спектра люминесценции паров I 2 показало, что при освещении I 2 узкой линией спектра ртути с l = 253,7 нм спектр паров I 2 представляет собой группы полос из тесно расположенных линий. Расстояние между линиями примерно 0,2 нм. Если длину волны возбуждающего света изменить на 0,4 – 0,8 нм, то вся система линий смещается в одну сторону, оставаясь в основном подобной. Это можно объяснить тем, что при изменении энергии поглощаемого фотона с hn 1 до hn 2 молекулы йода переходят на другой возбуждённый уровень.
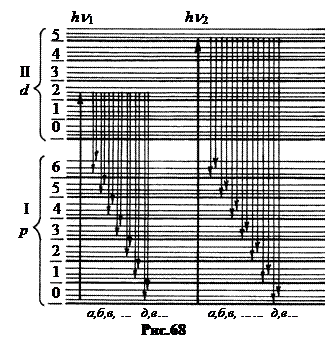 На рис.68 римской цифрой I обозначен нижний невозбуждённый электронный уровень в атоме йода (p - подуровень), цифрой II – ближайший возбуждённый электронный уровень атома йода (d - подуровень). Система пронумерованных уровней 0,1,2… показывает расщепление электронных уровней в молекуле йода, обусловленное колебательным движением молекулы. Линии без номеров между колебательными уровнями обозначают расщепление, обусловленное вращательным движением молекулы.
На рис.68 римской цифрой I обозначен нижний невозбуждённый электронный уровень в атоме йода (p - подуровень), цифрой II – ближайший возбуждённый электронный уровень атома йода (d - подуровень). Система пронумерованных уровней 0,1,2… показывает расщепление электронных уровней в молекуле йода, обусловленное колебательным движением молекулы. Линии без номеров между колебательными уровнями обозначают расщепление, обусловленное вращательным движением молекулы.
Уровни расположены очень тесно, энергетические ступеньки между ними малы. Поэтому даже незначительное изменение энергии поглощённого фотона с hn 1 до hn 2 переводит молекулу на другой возбуждённый уровень. Поскольку возвращается молекула в основное состояние в соответствии с правилами отбора, то “идёт” она по другим ступенькам, испуская хотя и похожую, но другую комбинацию спектральных линий.
Чем уже линия возбуждающего света, тем лучше разрешается молекулярный люминесцентный спектр. Если возбуждающая линия становится шире, охватывая спектр частот от n 1 до n 2, то могут испускаться и первая и вторая (по рис.68) и другие системы полос. В результате спектр паров даже двуатомных молекул чрезвычайно усложняется и во многих местах становится малодоступным для разрешения. Спектры многоатомных молекул отличаются ещё большей сложностью, и потому их ещё труднее интерпретировать.
Из рисунка 68 становится понятным закон Стокса. Если молекула не вносит энергию в излучение, то фотоны испускаемого света имеют меньшую энергию (большую длину волны) по сравнению с фотонами поглощаемого света (переходы а, б, в, г). Остальная энергия превращается в тепло и лишь при резонансном излучении, когда нет потерь, энергия поглощённого и излучённого фотонов одинакова (переходы д).
Если фотон поглощается уже возбуждённой за счёт теплового движения молекулой, то может излучаться фотон с большей энергией. Чем выше температура газа, тем больше таких возбуждённых молекул, тем больше вероятность антистоксовского излучения.
Линии люминесцентных спектров уже линий теплового излучения, поскольку температура газа ниже, и потому доплеровское уширение, обусловленное тепловым поступательным движением молекул, меньше. При сжатии газов расстояние между молекулами уменьшается. Их взаимодействие усиливается. Это ведёт к дополнительному расщеплению энергетических уровней молекул и, соответственно, к увеличению числа спектральных линий.
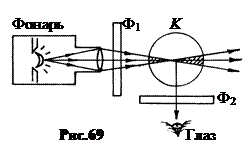 6. Люминесценция конденсированных сред. Её исследование затрудняется тем, что наряду с люминесцентным излучением в жидкости и газах становится весьма заметным рассеяние возбуждающего люминесценцию света. Чтобы устранить рассеянный свет, наблюдение ведётся обычно по схеме скрещённых светофильтров, показанной на рис.69. Источник возбуждающего света, например, электрическая дуга, заключён в светонепроницаемый кожух. Перед выходным объективом фонаря помещается светофильтр, максимум пропускания которого приходится на длину волны l 1, находящуюся в пределах полосы поглощения люминофора.
6. Люминесценция конденсированных сред. Её исследование затрудняется тем, что наряду с люминесцентным излучением в жидкости и газах становится весьма заметным рассеяние возбуждающего люминесценцию света. Чтобы устранить рассеянный свет, наблюдение ведётся обычно по схеме скрещённых светофильтров, показанной на рис.69. Источник возбуждающего света, например, электрическая дуга, заключён в светонепроницаемый кожух. Перед выходным объективом фонаря помещается светофильтр, максимум пропускания которого приходится на длину волны l 1, находящуюся в пределах полосы поглощения люминофора.
Чтобы отсечь рассеянный в кювете К (или в кристалле) свет l 1, между глазом и кюветой помещается второй светофильтр Ф2, длина волны l 2 максимума пропускания которого приходится на полосы люминесценции.
Расстояние между спектральными линиями в полосах люминесценции конденсированных тел ещё меньше, чем в полосах молекулярных газов. Поэтому спектры люминесценции жидких и твёрдых тел обычно характеризуют кривой люминесценции.
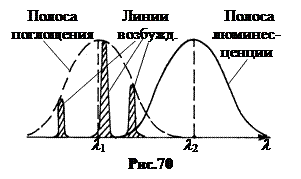 Опыт показывает, что кривые поглощения и люминесценции всегда сдвинуты друг относительно друга в соответствии с правилом Стокса и частично перекрываются (Рис.70). При возбуждении люминесценции узкой линией спектр люминесценции один и тот же, если линия находится в пределах полосы поглощения.
Опыт показывает, что кривые поглощения и люминесценции всегда сдвинуты друг относительно друга в соответствии с правилом Стокса и частично перекрываются (Рис.70). При возбуждении люминесценции узкой линией спектр люминесценции один и тот же, если линия находится в пределах полосы поглощения.
Введение посторонних веществ в люминофор, ослабляющих свечение, называют примесным тушением люминесценции. Оно обусловлено тем, что возбуждённые атомы люминофора, сталкиваясь с атомами примеси, отдают им свою энергию. При концентрационном тушении свечение ослабляется из-за увеличения взаимодействия между самими излучающими атомами. В результате увеличивается доля безызлучательных переходов.
Люминесценцию характеризуют коэффициентом полезного действия h = Е люм çЕ погл, где Е люм – энергия люминесцентного излучения, а Е погл – энергия поглощённого излучения, квантовым выходом k = n люм çn погл, где n люм и n погл– число испущенных и поглощённых, соответственно, фотонов, средней длительностью t возбуждённого состояния молекул и др.
Время t изменяется от 10-8с (пары йода) до 10-4с (урановые стёкла) и даже до нескольких часов. Из закона сохранения энергии следует, что чем больше t, тем меньше интенсивность свечения. С ростом температуры время t уменьшается. Кристаллофосфоры с t порядка нескольких часов могут высвечиваться при нагревании за доли секунды. Яркость свечения при этом сильно возрастает.
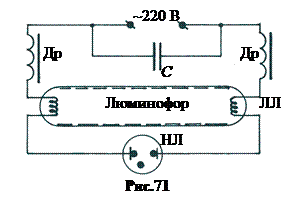
7. Люминесцентные лампы – это самая широкая область практического применения люминесценции. Схема включения самой распространённой газоразрядной ртутной люминесцентной лампы (ЛЛ) низкого давления показана на рис.71.
Лампа ЛЛ представляет собой стеклянную трубку, на внутренней поверхности которой напылён мелкий порошок кристаллического люминофора. В торцах лампы впаяны вольфрамовые оксидированные спирали, облегчающие запуск лампы.
 Внутри лампы ЛЛ находится смесь ртутных паров Hgи инертных газов (Ne, Ar) под давлением 10-3 ÷ 10-2мм рт.ст. Возникающее в электрическом разряде лампы свечение ртутных паров около 50% по энергии находится в УФ области с интенсивными линиями l 1 = 184,9 нм и l 2 = 253,7 нм, которые и обеспечивают свечение люминофора.
Внутри лампы ЛЛ находится смесь ртутных паров Hgи инертных газов (Ne, Ar) под давлением 10-3 ÷ 10-2мм рт.ст. Возникающее в электрическом разряде лампы свечение ртутных паров около 50% по энергии находится в УФ области с интенсивными линиями l 1 = 184,9 нм и l 2 = 253,7 нм, которые и обеспечивают свечение люминофора.
При включении лампы ЛЛ в сеть 220 В ток через неё вначале не идёт. В результате на неоновой лампе – стартёре НЛ возникает напряжение, достаточное для её зажигания. При горении стартёра через него идёт ток десятки миллиампер, вольфрамовые спирали в торцах лампы ЛЛ разогреваются, обеспечивая высокую эмиссию электронов. В результате лампа ЛЛ зажигается, через неё идёт ток в сотни миллиампер. Напряжение на лампе ЛЛ и в стартёре падает и становится меньше напряжения гашения стартёра. Стартёр гаснет, вольфрамовые спирали в лампе ЛЛ остывают, разряд в лампе поддерживается за счёт ионизации атомов ртути и инертного газа.
В качестве люминофоров в таких лампах наиболее часто используют галлофосфат кальция, активированный сурьмой и марганцем, или смесь MgWO4 и (ZnBe)2SiO4·Mn. Состав люминофора подбирается таким, чтобы спектр люминесценции был ближе к спектру дневного света. Световая отдача люминесцентных ламп достигает 80 лм ç Вт, а срок службы – свыше 10000 часов, что в несколько раз больше, чем у ламп накаливания.
8. Комбинационное рассеяния света. В 1928 году Леонид Мандельштам и Григорий Ландсберг, изучая рассеяние монохроматического света в кристаллах, обнаружили, что у спектральных линий в рассеянном свете появляются линии – спутники. Спутники расположены с двух сторон на определённых по частоте расстояниях D n (Рис.72).
В том же году этот эффект обнаружил в жидкостях индийский физик Чандрасекхара Раман. Явление назвали комбинационным рассеянием или, в западной литературе, эффектом Рамана. Основные закономерности эффекта следующие.
а. Спутники сопровождают каждую линию первичного спектра
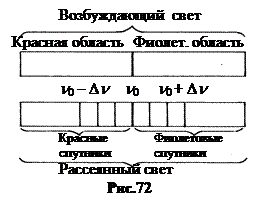 б. Различие в частотах D n возбуждающей первичной линии n 0 и линий каждого из спутников n 1, n 2, n 3… характерно для рассеивающего вещества. Оно равно частотам собственных ИК колебаний его молекул.
б. Различие в частотах D n возбуждающей первичной линии n 0 и линий каждого из спутников n 1, n 2, n 3… характерно для рассеивающего вещества. Оно равно частотам собственных ИК колебаний его молекул.
в. Спутники представляют собой системы линий, лежащие симметрично (по частоте) по обе стороны возбуждающей линии.
г. Спутники в длиноволновой области (“красные”) много интенсивнее коротковолновых (“фиолетовые”).
д. С повышением температуры интенсивность “фиолетовых” спутников растёт.
Суть явления в следующем. Если атом или молекула испытывают собственные колебания с частотой n, то при взаимодействии со световым квантом они могут отдать ему энергию hn и тем самым изменить частоту рассеянного света. Энергия кванта в этом случае увеличивается, hn 0 + hn = h (n 0 + n). Получается “фиолетовый” спутник.
Если же квант сталкивается с “неподвижной” молекулой, то он может отдать ей энергию, энергия и частота рассеянного кванта уменьшатся и станут равными hn 0 - hn и n 0 - n. Получается “красный” спутник. У холодных тел энергия колебания молекул невелика. Поэтому интенсивность “красных” спутников больше, чем “фиолетовых”. С нагреванием энергия колебания молекул растёт, а значит, растёт и интенсивность “фиолетовых” спутников.
Как и люминесценция, комбинационное рассеяние света позволяет исследовать внутреннюю структуру вещества. Это оптический аналог эффекта Комптона.
 2014-02-02
2014-02-02 8296
8296
