РАЗЛИЧНЫЕ АГРЕГАТНЫЕ СОСТОЯНИЯ ВЕЩЕСТВА
Тема 1. ФИЗИЧЕСКИЕ СВОЙСТВА КАПЕЛЬНЫХ ЖИДКОСТЕЙ КАК СРЕДЫ ДВИЖЕНИЯ
ВВЕДЕНИЕ
Прикладная гидромеханика».
Московский Авиационный Институт
(Государственный технический университет) «МАИ»
Кафедра «Проектирование аэрогидрокосмических систем»
Акимов Е.Н., Керин Н.В.
Конспект лекций по дисциплине:
Утверждено
на заседании кафедры 608
__________________
Москва 2011
Настоящее пособие предназначено для студентов, изучающих дисциплину «Прикладная гидромеханика» для специальности 1306 (160801) и специализаций (03, 04, 15).
Пособие написано с использованием материалов учебника «Гидромеханика», автор Шашин В.М. Учитывая, что на изучение данной дисциплины отводится крайне ограниченное время, а изучаемая дисциплина является одной из определяющих, с большим объёмом курса, возникла необходимость изложить указанный курс в конспективном виде.
В данном пособии изложены вопросы силового взаимодействия тел с жидкостью при их движении, методы оценки сил различной природы; рассмотрены кавитационные течения, глиссирование, погружение тел в воду. Наряду с численными решениями задач изложена приближённая инженерная методика.
(Лекций 1 ч.)
Предмет прикладной гидромеханики. Некоторые сведения из истории развития прикладной гидромеханики. Внешняя и внутренняя задача прикладной гидромеханики. Прямые, обратные и смешанные типы задач гидромеханики. Место и роль гидромеханики в практике проектирования аэрогидрокосмических систем.
(Лекций 3 ч., СРС 2 ч.)
Различные агрегатные состояния вещества.
Существование поверхности раздела. Поверхностное натяжение.
Плотность жидкостей.
Уравнение состояния воды.
Вязкость воды. Жидкости ньютоновские и неньютоновские.
Количественная оценка сжимаемости жидкостей.
Теплопроводность и диффузия жидкостей.
Характерное свойство твердых тел — способность сохранять неизменной форму. Газы и жидкости объединяет свойство текучести, т. е. способность свободно деформироваться под воздействием малых внешних сил и принимать форму заданного ограниченного пространства. Следует, однако, выделить понятие капельной жидкости. В отличие от газов, капельные жидкости обладают малой сжимаемостью, так, что будучи помещенными в сосуд, они занимают не весь объем (как это происходит у газов), а только тот, который свойствен данной массе жидкости. Таким образом капельные жидкости могут образовывать поверхности раздела, а в отдельных случаях - в буквальном смысле формировать капли.
С термодинамической точки зрения состояние жидкости или пара характеризуется тремя параметрами; давлением p, плотностью ρ и температурой Т, связанными между собой уравнением состояния. Поэтому для выяснения, в какой фазе находится вещество – в жидкой или паровой (газовой), достаточно знать какие-либо два параметра (скажем, давление p и температурy T).
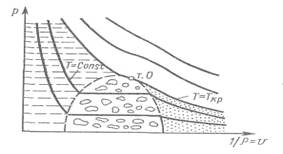 |
Диаграмму состояния бинарной системы «жидкость – пар» можно представить в системе координат p -
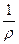 семейством изотерм Т = const
семейством изотерм Т = const Рис. 1.1 Диаграмма состояния «жидкость-пар».
(рис. 1.1). Величина 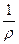 называется удельным объемом и обозначается υ. Тогда диаграмму, изображенную на рис. 1.1, называют p - υ диаграммой.
называется удельным объемом и обозначается υ. Тогда диаграмму, изображенную на рис. 1.1, называют p - υ диаграммой.
Характерной точкой на этой диаграмме является критическая точка О. Термодинамические параметры воды, например, в этой точке имеют значения Ткр = 647 К, pкр = 220-105 Па, ρкр = 400 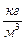 .
.
В области температур выше критической, вдоль изотермы наблюдается непрерывный переход вещества из жидкого состояния (при больших плотностях) в газообразное (при малых плотностях). Причем принципиальной перестройки структуры вещества в этом случае не происходит. Поэтому данное агрегатное состояние при T > T кр часто определяют как однородную фазу.
В зоне температур, T < T кр, отчетливо видны три области. Если двигаться вдоль изотермы из области малых плотностей к большим (движение справа налево по изотерме рис. 1.1), то в области паровой фазы давление будет непрерывно повышаться. После пересечения изотермой правой границы двухфазной зоны (пунктирная кривая) давление будет оставаться приблизительно постоянным в пределах всей зоны. Оно является характерной величиной, обозначается 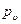 и называется давлением насыщенного пара, т. е, давлением равновесной системы жидкость-пар при заданной температуре. После пересечения изотермой левой ветви двухфазной зоны (в области жидкой фазы) давление вдоль изотермы вновь повышается, причем значительно быстрее, чем в области паровой фазы. Изотермы становятся почти вертикальными линиями, что и отражает малую сжимаемость жидкостей. Границу двухфазной зоны приближенно можно представить параболой p(υ), вершина которой находится в критической точке т.О. Изотерма T=Tкр в критической точке касается границы переходной области.
и называется давлением насыщенного пара, т. е, давлением равновесной системы жидкость-пар при заданной температуре. После пересечения изотермой левой ветви двухфазной зоны (в области жидкой фазы) давление вдоль изотермы вновь повышается, причем значительно быстрее, чем в области паровой фазы. Изотермы становятся почти вертикальными линиями, что и отражает малую сжимаемость жидкостей. Границу двухфазной зоны приближенно можно представить параболой p(υ), вершина которой находится в критической точке т.О. Изотерма T=Tкр в критической точке касается границы переходной области.
Внутри области, названной двухфазной, вещество находится в неустойчивом состоянии, а за ее пределами – в устойчивом. Малейшее изменение давления при заданной температуре внутри двухфазной области переводит вещество либо в жидкое, либо в газообразное состояние.
Таким образом, появления разрыва сплошности в жидкости можно добиться либо повышением температуры выше температуры кипения, либо снижением давления ниже давления насыщенных паров. Процесс выделения паровой фазы в виде отдельных полостей называется кавитацией. Кавитацию иногда называют холодным кипением.
 2014-02-02
2014-02-02 939
939







