Для равновесных процессов изменения состояния газа первое начало термодинамики 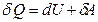 можно записать в виде
можно записать в виде 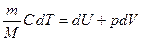 . (2.3.9)
. (2.3.9)
Применим это уравнение к изопроцессам в идеальном газе. Законы изопроцессов получим из уравнения Менделеева-Клапейрона  .
.
Практически изохорный процесс осуществляется при изменении температуры газа, находящегося в толстостенном сосуде постоянного объема. Для такого процесса уравнение состояния идеального газа удобно записать в виде  . Все величины, стоящие в правой части уравнения, постоянные. Следовательно, давление данной массы газа при постоянном объеме возрастает линейно с ростом температуры:
. Все величины, стоящие в правой части уравнения, постоянные. Следовательно, давление данной массы газа при постоянном объеме возрастает линейно с ростом температуры:
 .(2.3.10)
.(2.3.10)
 Рис.3.3 Рис.3.3 | Закон Шарля также описывает линейную зависимость давления газа от температуры. На рис.3.3 изображены  , , 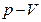 и и 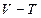 диаграммы изохорного процесса при различных значениях объема диаграммы изохорного процесса при различных значениях объема  газа. Поскольку в данном процессе объем газа не изменяется ( газа. Поскольку в данном процессе объем газа не изменяется (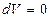 ), то газ работы не совершает ( ), то газ работы не совершает (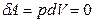 ) и вся сообщаемая теплота идет на изменение его внутренней энергии. Первое начало термодинамики имеет вид: ) и вся сообщаемая теплота идет на изменение его внутренней энергии. Первое начало термодинамики имеет вид: |
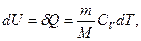 (2.3.11)
(2.3.11)
где 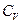 – молярная теплоемкость газа при постоянном объеме (
– молярная теплоемкость газа при постоянном объеме (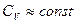 ).
).
При изохорном нагревании газа от температуры  до температуры
до температуры 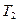 изменение внутренней энергии газа и сообщенная ему теплота равны
изменение внутренней энергии газа и сообщенная ему теплота равны
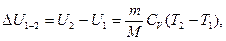
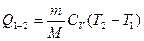 . (2.3.12)
. (2.3.12)
Для любого равновесного процесса первый закон термодинамики можно записать в виде:
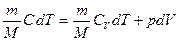 . (2.3.13)
. (2.3.13)
Для 1 моля газа 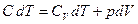 . (2.3.14)
. (2.3.14)
Изобарный процесс ( )
)
Практически изобарный процесс осуществляется, например, при нагревании или охлаждении газа, находящегося в цилиндре с подвижным поршнем, на который действует постоянное внутреннее давление. Для такого процесса уравнение состояния идеального газа удобно записать в виде  . Все величины, стоящие в правой части уравнения, постоянные. Следовательно, объем данной массы газа при постоянном давлении возрастает линейно с ростом температуры:
. Все величины, стоящие в правой части уравнения, постоянные. Следовательно, объем данной массы газа при постоянном давлении возрастает линейно с ростом температуры: 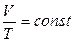 . (2.3.15)
. (2.3.15)
Закон Гей-Люссака также описывает линейную зависимость объема от температуры. На рис.3.4 изображены  ,
,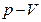 и
и 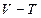 диаграммы изобарного процесса при различных значениях давления
диаграммы изобарного процесса при различных значениях давления 
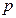 газа.
газа.
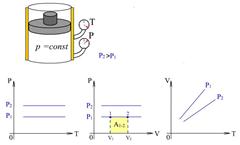 Рис.3.4 Рис.3.4 |
Элементарная теплота 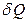 , сообщаемая газу в изобарном процессе, равна
, сообщаемая газу в изобарном процессе, равна
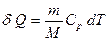 , (2.3.15)
, (2.3.15)
где 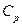 – молярная теплоемкость газа при постоянном давлении, которую также называют изобарной теплоемкостью.
– молярная теплоемкость газа при постоянном давлении, которую также называют изобарной теплоемкостью.
Продифференцируем уравнение состояния газа  при
при  :
: 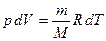 .
.
Следовательно, 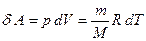 . (2.3.16)
. (2.3.16)
Подставим выражения (2.3.11), (2.3.15) и (2.3.16) в первое начало термодинамики (2.3.3):


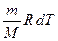 . (2.3.17)
. (2.3.17)
Отсюда следует, что  . (2.3.18)
. (2.3.18)
Это соотношение называется уравнением Майера. Его физический смысл заключается в том, что при изобарном нагревании газа к нему должна быть подведена большая теплота, чем при таком же изохорном нагревании. Разность значений теплоты должна быть равна работе, совершенной газом при изобарном расширении.
Работа, совершаемая газом при изобарном процессе расширения 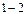
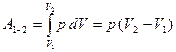
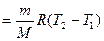 , (2.3.19)
, (2.3.19)
измеряется площадью, закрашенной на 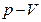 диаграмме.
диаграмме.
Изотермический процесс расширения или сжатия газа может происходить в условиях, когда теплообмен между газом и внешней средой осуществляется при постоянной разности температур. Для этого теплоемкость внешней среды должна быть достаточно велика и процесс расширения (или сжатия) должен происходить весьма медленно.
В уравнении состояния идеального газа  при изотермическом процессе все величины, стоящие в правой части уравнения, постоянные. Следовательно,
при изотермическом процессе все величины, стоящие в правой части уравнения, постоянные. Следовательно,
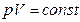 . (2.3.20).
. (2.3.20).
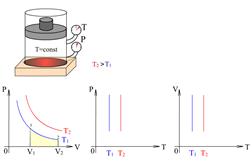 Рис.3.5 Рис.3.5 | Закон Бойля-Мариотта, установленный экспериментально, дает такую же зависимость. На 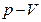 диаграмме (рис.3.5) такой процесс графически изображается изотермой,имеющей вид равнобочной гиперболы. Внутренняя энергия идеального газа в изотермическом процессе ( диаграмме (рис.3.5) такой процесс графически изображается изотермой,имеющей вид равнобочной гиперболы. Внутренняя энергия идеального газа в изотермическом процессе (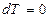 ) не изменяется ) не изменяется 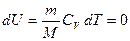 , , |
следовательно, вся теплота, сообщаемая газу, расходуется на совершение газом работы против внешних сил:
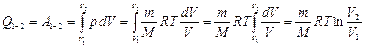 , (2.3.21)
, (2.3.21)
Работа изотермического расширения газа измеряется площадью, закрашенной на 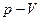 диаграмме.
диаграмме.
Поскольку в данном процессе 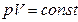 , то
, то  и
и 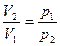 и
и
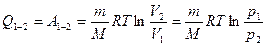 . (2.3.21а)
. (2.3.21а)
Практически адиабатными можно считать процессы быстрого расширения или сжатия газа при которых система не обменивается теплотой с окружающей средой.
Из первого начала термодинамики (2.3.3) для адиабатного процесса (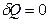 ) получаем, что система совершает работу за счет убыли ее внутренней энергии:
) получаем, что система совершает работу за счет убыли ее внутренней энергии:
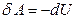 . (2.3.22)
. (2.3.22)
Подставим сюда выражения (2.3.1) и (2.3.11) получим: 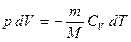 , (2.3.23)
, (2.3.23)
что работа, связанная с изменением объема газа, сопровождается изменением его температуры. Знак «минус» в уравнении означает, что увеличение объема (расширение) сопровождается понижением температуры, а уменьшение объема (сжатие) – повышением.
Уравнение адиабаты или уравнение Пуассона имеет вид:
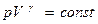 , (2.3.24)
, (2.3.24)
где  – безразмерная величина, называемая показателем адиабаты или коэффициентом Пуассона. Уравнение адиабаты можно записать и через другие параметры
– безразмерная величина, называемая показателем адиабаты или коэффициентом Пуассона. Уравнение адиабаты можно записать и через другие параметры
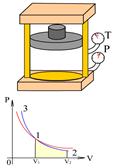 Рис.3.6 Рис.3.6 | состояния: 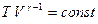 и и 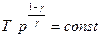 . (2.3.25) Линия, изображающая адиабатный процесс на . (2.3.25) Линия, изображающая адиабатный процесс на 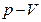 диаграмме (рис.3.6) называется адиабатой (синяя линия). Для сравнения на этом же рисунке красной линией изображена изотерма при температуре газа в состоянии диаграмме (рис.3.6) называется адиабатой (синяя линия). Для сравнения на этом же рисунке красной линией изображена изотерма при температуре газа в состоянии 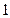 . Так как . Так как 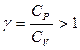 , то адиабата идет круче изотермы. Объясняется это тем, что при адиабатном сжатии (процесс , то адиабата идет круче изотермы. Объясняется это тем, что при адиабатном сжатии (процесс 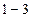 ) увеличение давления происходит не только за счет уменьшения объема, ) увеличение давления происходит не только за счет уменьшения объема, |
как при изотермическом сжатии, но и за счет увеличения температуры сжимаемого газа. При адиабатном расширении газа (процесс 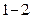 ) его температура уменьшается, и давление падает быстрее, чем при соответствующем изотермическом расширении.
) его температура уменьшается, и давление падает быстрее, чем при соответствующем изотермическом расширении.
Работа, совершаемая газом в адиабатном процессе 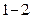
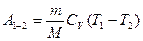 (2.3.26)
(2.3.26)
измеряется площадью, закрашенной на рис.3.6.
Из уравнения для внутренней энергии идеального газа  легко найти молярные теплоемкости
легко найти молярные теплоемкости 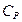 и
и 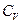 . Поскольку
. Поскольку  и
и  , то
, то
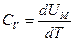
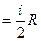 и
и 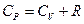 .
.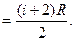 (2.3.29)
(2.3.29)
Соответственно, показатель адиабаты 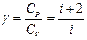 (2.3.30)
(2.3.30)
В табл.3.1 приведены значения 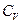 ,
, 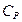 и
и 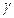 для идеальных газов с различными степенями свободы
для идеальных газов с различными степенями свободы
Таблица 3.1
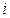 |  | 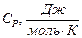 | 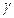 |
| 3 (одноатомный газ) | 12,5 | 20,8 | 1,67 |
| 5 (двухатомный газ) | 20,8 | 29,1 | 1,40 |
| 6 (многоатомный газ) | 24,9 | 33,2 | 1,33 |
Политропный процесс (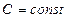 ) – термодинамический процесс, протекающий без изменения теплоемкости
) – термодинамический процесс, протекающий без изменения теплоемкости 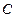 .
.
Уравнение политропы имеет вид: 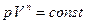 , (2.3.31)
, (2.3.31)
где 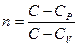 – показатель политропы (
– показатель политропы (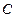 – теплоемкость газа в данном процессе).
– теплоемкость газа в данном процессе).
Все рассмотренные выше изопараметрические процессы являются частными случаями политропного процесса. Действительно, при 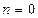 уравнение политропы описывает изобарный процесс (
уравнение политропы описывает изобарный процесс ( ). При
). При 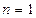 – изотермический процесс (
– изотермический процесс (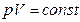 ). При
). При
 Рис.3.7 Рис.3.7 |
 это адиабатный процесс (
это адиабатный процесс (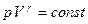 ). При
). При  уравнение политропы описывает изохорный процесс. В этом можно убедиться, если уравнение
уравнение политропы описывает изохорный процесс. В этом можно убедиться, если уравнение  , преобразовать к виду
, преобразовать к виду 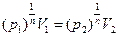 . При
. При 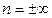 получаем
получаем  . Все эти процессы изображены на приведенной
. Все эти процессы изображены на приведенной 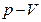 диаграмме (рис.3.7).
диаграмме (рис.3.7).
 2014-02-02
2014-02-02 9758
9758

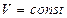 )
) )
)