ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ И НАПРАВЛЕНИЕ САМОПРОИЗВОЛЬНЫХ ПРОЦЕССОВ.
ЛЕКЦИЯ 5
Термодинамическими потенциалам называют такие термодинамические функции состояния, убыль которых в обратимо протекающих процессах при постоянстве определенных параметров равна максимальной полезной работе процесса.
Для того, чтобы получить представление о термодинамических потенциалах воспользуемся совместным математическим выражением I и II законов термодинамики. Получим его:
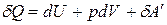 уравнение I закона термодинамики (6)
уравнение I закона термодинамики (6)
 или
или 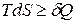 уравнение II закона термодинамики (49)
уравнение II закона термодинамики (49)
Из сравнения уравнений (6) и (49) следует:
 (68) для обратимых и необратимых процессов
(68) для обратимых и необратимых процессов
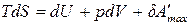 (69) для обратимых процессов полезная работа максимальна
(69) для обратимых процессов полезная работа максимальна
 (70) для обратимых и необратимых процессов, если единственной работой процесса является работа расширения
(70) для обратимых и необратимых процессов, если единственной работой процесса является работа расширения
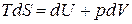 (71) для обратимых процессов, если единственной работой процесса является работа расширения
(71) для обратимых процессов, если единственной работой процесса является работа расширения
Известно, что 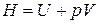 . Продифференцируем уравнение и решим его относительно
. Продифференцируем уравнение и решим его относительно 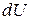 , получим:
, получим:
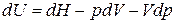 .
.
Подставим в уравнения (68) – (71) вместо 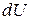 его значение, получим:
его значение, получим:
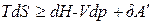 (72) для обратимых и необратимых процессов
(72) для обратимых и необратимых процессов
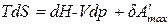 (73) для обратимых процессов полезная работа максимальна
(73) для обратимых процессов полезная работа максимальна
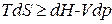 (74) для обратимых и необратимых процессов, если единственной работой процесса является работа расширения
(74) для обратимых и необратимых процессов, если единственной работой процесса является работа расширения
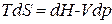 (75) для обратимых процессов, если единственной работой процесса является работа расширения
(75) для обратимых процессов, если единственной работой процесса является работа расширения
Воспользуемся выражениями (68) – (75) для анализа некоторых термодинамических процессов.
1.  (изохорно-изоэнтропийный процесс)
(изохорно-изоэнтропийный процесс)
Рассмотрим процесс, единственным результатом которого является работа расширения. Из выражения (70) имеем:
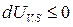 ;
; 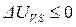 .
.
Знак неравенства относится к самопроизвольно протекающему (необратимому) изохорно-изоэнтропийному процессу, знак равенства характеризует термодинамическое равновесие.
Таким образом, получили, что выражение 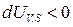 (
(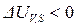 ), т.е. убыль внутренней энергии системы, характеризует условие самопроизвольного протекания изохорно-изоэнтропийного процесса. Как только внутренняя энергия достигает своего минимального значения устанавливается термодинамическое равновесие. Условие минимума внутренней энергии системы при
), т.е. убыль внутренней энергии системы, характеризует условие самопроизвольного протекания изохорно-изоэнтропийного процесса. Как только внутренняя энергия достигает своего минимального значения устанавливается термодинамическое равновесие. Условие минимума внутренней энергии системы при 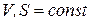 :
:
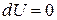 .
.
Из уравнения (69) получаем:
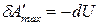 ;
;
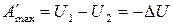 .
.
Как видим, уменьшение внутренней энергии системы в изохорно-изоэнтропийном процессе характеризует максимальную работу этого процесса.
Таким образом, внутренняя энергия является изохорно-изоэнтропийным термодинамическим потенциалом.
2. 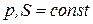 (изобарно-изоэнтропийный процесс)
(изобарно-изоэнтропийный процесс)
Из выражения (74) имеем:
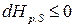 ;
; 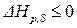 .
.
Знак неравенства характеризует условие самопроизвольного протекания (необратимого) изохорно-изоэнтропийного процесса. Как видно, таким условием является уменьшение энтальпии системы.
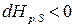 (
(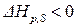 ).
).
При установившемся термодинамическом равновесии в системе при 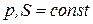 энтальпия системы минимальна. Условие минимума функции:
энтальпия системы минимальна. Условие минимума функции:
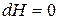 .
.
Используем теперь для анализа обратимого изобарно-изоэнтропийному процесса уравнение (73), которое перепишется в виде:
 ;
;
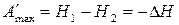 .
.
Как видим, уменьшение энтальпии системы в изобарно-изоэнтропийном процессе характеризует максимальную работу этого процесса.
Таким образом, энтальпия является изобарно-изоэнтропийным термодинамическим потенциалом.
Рассмотренные процессы на практике реализуются крайне редко. Поэтому материал имеет в большей степени теоретическое, чем практическое значение. Большинство же реальных процессов, протекающих в природе, технологии реализуются либо при 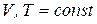 , либо при
, либо при 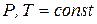 . Рассмотрим эти процессы.
. Рассмотрим эти процессы.
3. 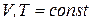 (изохорно-изотермический процесс)
(изохорно-изотермический процесс)
Для анализа воспользуемся выражением (70), тогда имеем:
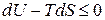 или
или 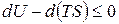 ;
;
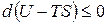 .
.
Слева полный дифференциал, следовательно, изменение функции
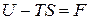 . (76)
. (76)
не зависит от пути протекания процесса, а определяется только начальным и конечным состояниями системы. Кроме того, функция аддитивная, так как составляющие ее функции аддитивные. Следовательно, функция 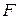 обладает всеми свойствами термодинамической функции состояния.
обладает всеми свойствами термодинамической функции состояния. 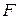 – функция (или энергия) Гельмгольца (свободная энергия) – одна из важнейших функций состояния.
– функция (или энергия) Гельмгольца (свободная энергия) – одна из важнейших функций состояния.
 ;
;  .
.
Знак неравенства характеризует условие самопроизвольного (необратимого) протекания изохорно-изотермического процесса. Как видно, таким условием является убыль энергии Гельмгольца.
При термодинамическом равновесии энергия Гельмгольца системы в изохорно-изотермических условиях минимальна. Условие минимума функции:
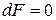 .
.
Воспользуемся теперь уравнением (69) для анализа обратимого изохорно-изотермического процесса, получим:
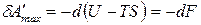 .
.
После интегрирования имеем:
 . (77)
. (77)
Как видим, уменьшение энергии Гельмгольца системы в изохорно-изотермическом процессе характеризует максимальную работу процесса.
Таким образом, энергия Гельмгольца является изохорно-изотермическим термодинамическим потенциалом.
Решим (76) относительно 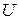 :
:
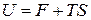 ,
,
где 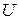 – полная внутренняя энергия системы, складывается из 2 частей:
– полная внутренняя энергия системы, складывается из 2 частей:
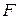 – свободная энергия – часть внутренней энергии, которая может быть превращена в работу (см. уравнение (77));
– свободная энергия – часть внутренней энергии, которая может быть превращена в работу (см. уравнение (77));
 – связанная энергия – часть внутренней энергии, которая не может быть превращена в работу. Она обеспечивает существование самой материальной системы.
– связанная энергия – часть внутренней энергии, которая не может быть превращена в работу. Она обеспечивает существование самой материальной системы.
 2014-02-12
2014-02-12 1930
1930