В природных белках одна и та же аминокислота не встречается подряд больше 3 раз.
Универсальность первичной структуры. Белки, выполняющие одинаковые функции в разных организмах имеют одинаковую или близкую первичную структуру.
Радикальная замена глу на вал в шестом положении в молекуле гемоглобина приводит к развитию серповидно-клеточной анемии. При этой патологии эритроциты в условиях низкого парциального давления приобретают форму серпа. После отдачи кислорода такой гемоглобин превращается в плохо растворимую форму и начинает выпадать в осадок в виде веретенообразных кристаллоидов, названных тактоидами. Тактоиды деформируют клетку и эритроциты приобретают форму серпа. При этом происходит гемолиз эритроцитов. Болезни протекает остро и дети погибают. Эта патология называется серповидно-клеточной анемией.
При радикальной замене возникает белок с другими свойствами, что может привести к патологии.
Невзаимозаменяемые аминокислоты, отличающиеся по структуре и свойствам.
Свойства первичной структуры белка
Пептидная связь способна к образованию двух водородных связей с другими группами, в том числе с пептидными.
Заместители по отношению связи C-N-связи находятся в транс положении.
Пептидная связь образует остов полипептидной цепи, она является повторяющимся фрагментом.
Особенности пептидной связи:
1. Копланарность – все атомы, входящие в пептидную связь, находятся в одной плоскости.
Пептидная связь – прочная ковалентная связь, энергия связи равняется 110 ккал/моль.
1. Детерминированность – последовательность аминокислот в белке генетически закодирована. Информация о последовательности аминокислот содержится в ДНК.
2. Уникальность – для каждого белка в организме характерна определенная последовательность аминокислот.
Аминокислоты, входящие в состав белков делят на 2 группы:
1. Взаимозаменяемые аминокислоты – это амиокислоты, сходные по структуре и свойствам.
В белковой молекуле различают 2 вида замен аминокислот:
1. Консервативная – замена одной аминокислоты на другую сходную по структуре. Такая замена не приводит к изменению свойств белка.
Примеры: гли-ала, асп-глу, тир-фен, вал-лей.
2. Радикальная замена – замена одной аминокислоты на другую отличающуюся по структуре. Такая замена приводит к изменению свойств белка.
Примеры: глу-вал, сер-цис, про-три, фен-асп, илей-мет.
Вторичная структура – это способ укладки полипептидной цепи в спиральную или складчатую конформацию.
Конформация – это пространственное расположение в органической молекуле замещающих групп, способных свободно изменять свое положение в пространстве без разрыва связей, благодаря свободному вращению вокруг одинарных углеродных связей.
Различают 2 вида вторичной структуры белка:
1. 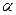 -спираль
-спираль
2. 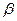 -складчатость.
-складчатость.
 2014-02-12
2014-02-12 3727
3727
