На анализ поступило лекарственное вещество со следующей структурой:
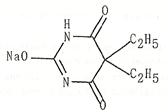
При оценке качества препарата показатели «Растворимость», «Прозрачность и цветность», «Содержание свободной щелочи» не отвечали требованиям НД. Раствор препарата опалесцировал сразу и количественное содержание примеси «Свободной щелочи» было значительно выше указанной в НД. Дайте обоснование причинам изменения его качества по данному показателю в соответствии с условиями хранения и свойствами. Приведите другие испытания, характеризующие его качество.
• Приведите русское, латинское и рациональное название препарата. Охарактеризуйте физико-химические свойства (внешний вид, растворимость, спектральные характеристики) и их использование для оценки качества.
• В соответствии с химическими свойствами предложите реакции идентификации и методы количественного определения. Напишите уравнения реакций.
1.
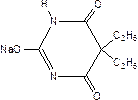
Barbitalum natrium
Барбитал натрия
Medinalum
Мединал
5,5-диэтилбарбитурат натрия
Препарат относится к лекарственным средствам, действующим на центральную нервную систему – снотворные средства. Снотворное действие барбитуратов впервые обнаружено в начале XX века Э. Фишером и Ф. Мерингом.
Физиологическая активность барбитуратов тесно связана с химическим строением. Для барбитала натрия характерно то, что это солевая форма, легко растворим в воде и действие наступает быстрее и может применяться не только в порошках и таблетках, но и в виде растворов, растворов для инъекций.
Барбитал натрия относится к производным барбитуровой кислоты или к группе циклических уреидов и представляет собой продукт взаимодействия мочевины и производных малоновой кислоты. Так как в результате конденсации мочевины и малоновой кислоты образуется циклическая система с 2 атомами азота (в положении 1 и 3), то из можно рассматривать как производные пиримидина.
Барбитураты способны проявлять лактим-лактальную таутомерию, и барбитал-натрия представляет собой натриевую соль лактимной формы барбитуратов.
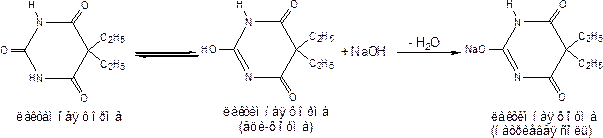
Барбитал-натрий представляет собой солевую форму, поэтому легко растворим в воде, мало – в спирте, водные растворы имеют щелочную среду по фенолфталеину (соль сильного основания и слабой кислоты).
Химические реакции обусловлены образованием комплексных соединений с солями тяжёлых металлов. Эти реакции лежат в основе определения подлинности:
общая реакция подлинности:
препарат растворяют в спирте, прибавляют 2 к.р. хлорид кальция, 2 к.р. р-р нитрата кобальта и 2 к.р. NaOH. Появляется сине-фиолетовое окрашивание (CaCl2 переводит в енольную форму) предварительно + HCl и осадок извлекают эфиром.
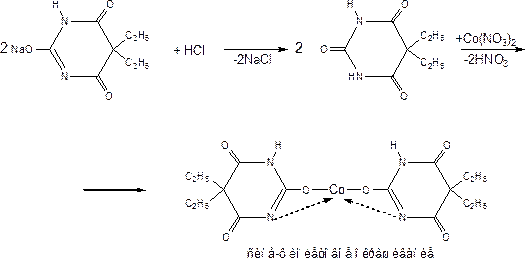
Отличительная реакция с раствором CuSO4 в присутствии раствора K2CO3 и KHCO3. Появляется синее окрашивание и осадок красно-сиреневого цвета.
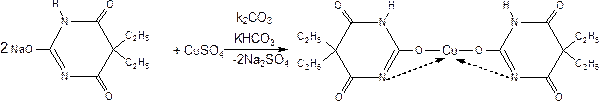
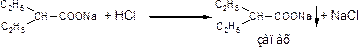
1) Т.к. это солевая форма, то при прибавлении HCl выпадает в осадок кислотная форма. Осадок отфильтровывают, промывают водой до отсутствия Cl– и сушат при 100-150°С до постоянного веса, а затем определяют температуру плавления (189-192°C)/

2) При взаимодействии с ионами серебра образуются двузамещённые соли серебра (в присутствии Na2CO3)
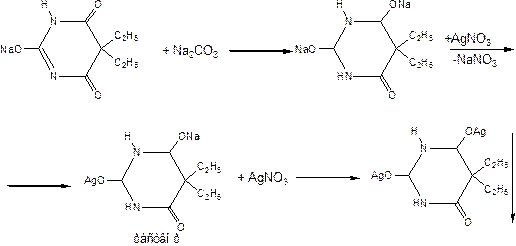
3) При сплавлении с едкими щелочами препарат разрушается и выделяется аммиак:
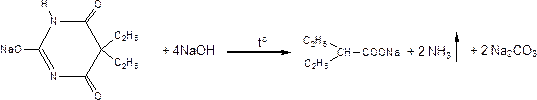
При подкислении HCl выделяется CO2 и запах жирной кислоты.
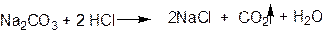
4) Т.к. препарат представляет соль натрия, то ион натрия обнаруживается по пламени (жёлтый цвет – отличительная реакция солевой формы).
Метод количественного определения кислотных форм – метод алкалиметрии в неводных растворителях (ДМФА). Титруют 0,1 М NaOH в смеси метанола и бензола. Индикатор – тимоловый синий. Диметилформамид усиливает кислотные свойства, присоединяет протон.
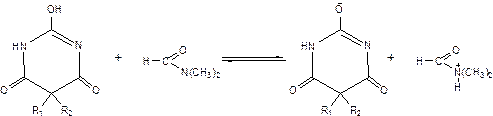
При последующем титровании NaOH выделяется диметилформамид, вода и Na+, который с анионом барбитурата образует натриевую соль:
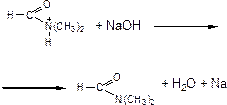 | 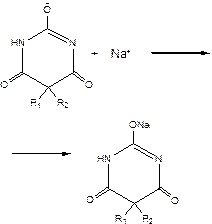 |
При определении солевых форм барбитуратов, имеющих в водных растворах щелочную реакцию (рН 9-11), используется метод ацидиметрии (титрант – 0,1 н р-р HCl, индикатор – метиловый оранжевый).
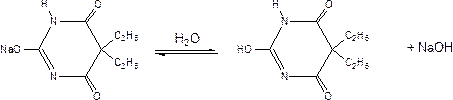
NaOH + HCl → NaCl + H2O.
Для количественного определения барбитуратов используют спектрофотометрическое титрование в области 239-240 нм. Растворителем служит боратный буферный раствор.
Параллельно проводят контрольный опыт, чтобы учесть возможную примесь свободной щёлочи. Поэтому при окончательном расчёте из полученного значения содержания барбитал-натрия (%) вычитают % содержания свободной щёлочи, умноженный на коэффициент 5,15.
Свободную щёлочь в солевых формах определяют путём титрования спиртового раствора барбитурата раствором HCl (0,05 М) в присутствии индикатора тимолового синего (оттитровывается только свободная щёлочь), которого в препарате должно быть не более 0,25%. Полученное значение учитывают при количественном определении.
 2015-01-30
2015-01-30 5611
5611








