В условиях промышленного производства и в аптеках готовят лекарственные средства с лекарственным веществом следующей структуры:
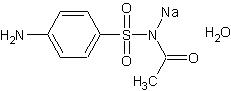
При оценке качества лекарственного вещества в образцах одной серии показатель «Прозрачность и цветность раствора» не отвечал требованиям НД. Дайте обоснование причинам изменения его качества по данному показателю в соответствии со свойствами. Предложите испытания для характеристики его качества.
• Приведите русское, латинское и рациональное название препарата. Охарактеризуйте физико-химические свойства (внешний вид, растворимость, спектральные характеристики) и их использование для оценки качества.
• В соответствии с химическими свойствами предложите реакции идентификации и методы количественного определения. Напишите уравнения реакций.
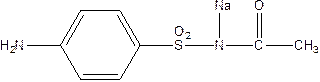
Sulfacetamide sodium
Sulfacylum-natrium
Сульфацил-натрий
Sulfacylum soluble
Сульфацил растворимый
Albucid-natium – альбуцид натрий
Sulfacetamidum Natricum* (международное название) – сульфацетамид натрия
Химическое название: n-аминобензолсульфенилацетамид-натрий.
Относится к антибактериальным средствам (средства для лечения и профилактики инфекционных заболеваний). Применяется для лечения стрептококковых, гонококковых, пневмококковых и колибациллярных инфекций в глазной практике в виде растворов и мазей при конъюктивитах, блефаритах и других инфекционных заболеваниях глаз; а также при пневмониях, инфекциях мочеполовых путей.
Представляет собой белый кристаллический порошок без запаха, легко растворим в воде, практически нерастворим в спирте, эфире, хлороформе (т.к. соль).
УФ-спектр 0,001%-ного раствора сульфацила натрия имеет максимум поглощения при 256 нм и минимум при 227 нм.
Т.к. представляет собой солевую форму, то может применяться в растворах, растворах для инъекций, глазных каплях, мазях.
Механизм действия основан на антогонизме с пара-аминобензойной кислотой и связан с нарушением образования микроорганизмами необходимых для их развития факторов – фолиевой и дигидрофолиевой кислот, в молекулу которых входит пара-аминобензойная кислота.
Т.к. сульфаниламиды близки по строению с ПАБК, они захватываются микробной клеткой вместо ПАБК и тем самым нарушают течение в ней обменных процессов. СА оказывают бактериостатическое действие.
- Наличие в структуре молекулы ароматической аминогруппы обуславливает реакцию образования азокрасителя, которая лежит в основе подлинности СА препаратов. Реакция основана на образовании хлорида диазония в результате действия растворов NaNO2 и HCl с последующим сочетанием со щелочным раствором β-нафтола, образуется вишнёво-красное окрашивание или оранжево-жёлтый осадок.
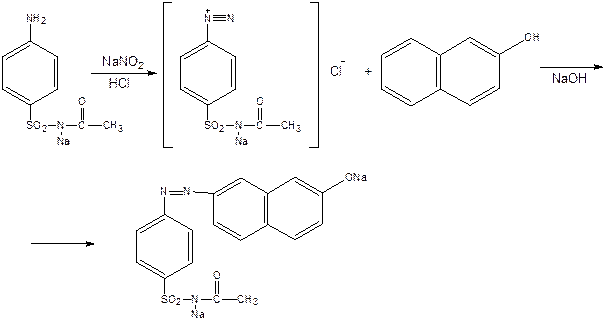
- Реакция обнаружения серы, т.к. препарат содержит серу в связанном состоянии, то вначале вещество окисляют конц. HNO3 или путём сплавления с 10-кратным количеством KNO2 до SO42–, который затем определяют по реакции с BaCl2.
- Т.к. соединение содержит имидную группу, то качественные реакции могут быть с солями тяжёлых металлов (Cu, Co, Fe, Ag и др.). Характерная реакция с CuSO4, соли образуют различные окрашивания, сульфацил натрия образует осадок голубовато-зеленоватого цвета, который не изменяется при стоянии (отличие от других СА препаратов).
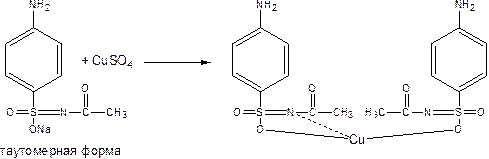
- Наличие аром. –NH2 групп характерна реакция конденсации с ароматическими альдегидами с образованием основания Шиффа – проводят на газетной бумаге: +HCl, лигнин подвергается гидролизу с образованием альдегидов:
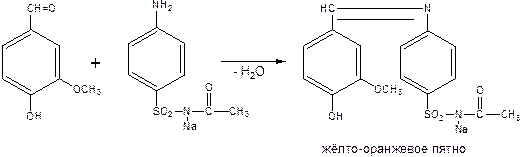
5. Наличие ароматического кольца обуславливает реакцию галогенирования (NH2 ориентант I рода) – образуются осадки
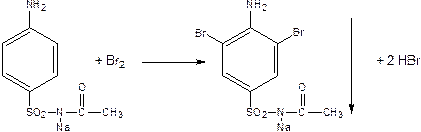
эта реакция лежит в основе количественного определения
- УФ-спектрофотометрия (оптические характеристики продуктов взаимодействия с сульфатом меди (I) в присутствии гидроксиламина).
- Реакция с нитропруссидом натрия. В присутствии NaOH и последующим подкислением HCl образуются окрашенные в красный или красно-коричневый цвет– наличие NH2 – объясняют реакции окисления с образованием окрашенных соединений хиноидной структуры (в качестве окислителя 3%-ный раствор пероксида водорода или 5%-ный раствор FeCl3).
- Отличительной реакцией сульфацила натрия является реакция кислотного гидролиза (имидная группа).
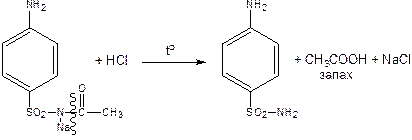
- Качественная реакция на Na+ (пламя в жёлтый цвет или с цинк-уранилацетатом в уксуснокислой среде образует жёлт. кр. ос.).
NaZn(NO2)3(CH3COOH)9·9H2O↓
При хранении необходимо учитывать химическое строение препарата: –NH2– обуславливает восстановленное вещество и легко окисляется под действием света (надо хранить в темноте).
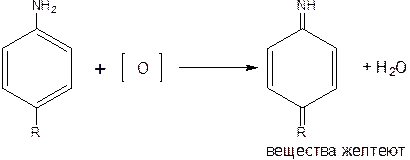
т.к. соль, то легко гидролизуется.
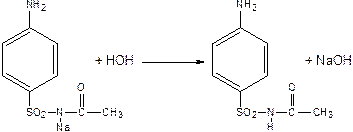
Т.к. содержит кристаллическую воду, то при хранении в неплотно закрытых склянках может происходить процесс потери воды и меняются физические свойства и терапевтический эффект.
СО2 также влияет отрицательно при хранении, т.к. происходит кислотный гидролиз с изменением химической структуры.
Количественный анализ обусловлен химическим строением:
1. ГФ – метод нитритометрии за счёт первичн. – NH2.
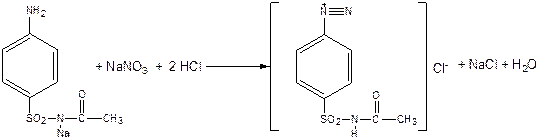
2. т.к. солевая форма – метод ацидиметрии (вариант вытеснения слабой кислоты более сильной)
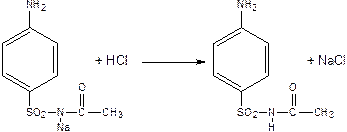 индикатор – метилоранж
индикатор – метилоранж
3. за счёт ароматического кольца возможны методы броматометрии, титруют р-р KBrO3 в кислой среде в присутствии KBr. Точка экв. определяется по обесцвечиванию бромом метилоранжа.
KBrO3 + 5KBr + 6HCl → 3Br2 + КCl + 3H2O
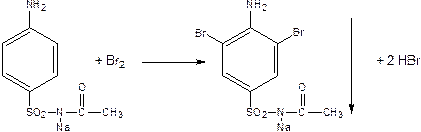
4. В лекарственных формах возможен метод рефрактометрии.
5. УФ-спектрометрия (УФ-спектр 0,001% раствора имеет максимум поглощения 257 и минимум – при 227 нм).
6. Фотоколориметрический метод определения основан на реакции образования азокрасителей.
7. ИК-спектроскопия в области 4000-400 см–1. Определяют по наличию характерных полос поглощения ИК-спектров.
Для стабилизации растворов сульфацила натрия используют р-р Na2S2O3 и HCl (в определённых количествах препарат 214) – что способствует предотвращению окисления препарата.
Хранят по способу Б. В таре, предохраняющей от действия влаги и света, с притёртыми пробками.
 2015-01-30
2015-01-30 6951
6951








