Катализаторы, которые находятся в системе в том же фазовом состоянии, что и реагенты, называются гомогенными. Механизм гомогенного катализа можно объяснить на основе теории промежуточных соединений. Большой вклад в развитие этой теории внесли П.Сабатье (Франция) и Н.Д. Зелинский (Россия). Согласно этой теории, катализатор образует с реагентами промежуточные соединения. Это приводит к уменьшению энергии активации реакции. Например, реакция:
АВ + D → A…B…D → A + BD
в присутствии катализатора К может проходить по схеме: D + K  D…K
D…K  DK
DK
DK + AB  A…B…D…K → A + BD + K
A…B…D…K → A + BD + K
Катализатор, как видим, не входит в продукты и не изменяет своего состава.
Примером каталитической гомогенной реакции является процесс окисления оксида углерода в присутствии паров воды:
2СО + О2 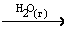 2СО2.
2СО2.
 2015-01-30
2015-01-30 1515
1515
