Так как гидролиз большинства солей является обратимым процессом, то степень гидролиза можно изменять, смещая равновесие реакций гидролиза и нейтрализации. Важнейшими факторами, влияющими на степень гидролиза, являются следующие: 1) константа диссоциации кислоты или основания, образующих соль, 2) общая концентрация соли, 3) температура, 4) рН раствора.
Влияние первого фактора видно из формулы Кг= К 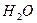 /Кдисс (табл.2).
/Кдисс (табл.2).
Константа гидролиза тем больше, чем меньше Кдисс. электролита, то есть чем слабее образующийся электролит, тем сильнее гидролизуется соль.
Из уравнения h = 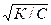 следует, что разбавление раствора усиливает гидролиз, а повышение концентрации соли подавляет его.
следует, что разбавление раствора усиливает гидролиз, а повышение концентрации соли подавляет его.
Влияние температуры на степень, гидролиза можно вывести из принципа Ле -Шателье. Реакция нейтрализации экзотермична, следовательно, гидролиз, (обратный ей процесс) эндотермичен, как и диссоциация воды. Поэтому при повышении температуры раствора гидролиз усиливается, охлаждение раствора подавляет гидролиз.
Выше было показало, что при гидролизе солей по катиону образуется кислая среда, при гидролизе но аниону – щелочная. Поэтому изменяя рН раствора, можно усиливать или подавлять гидролиз. Так, введение в раствор FеС1з кислоты вызовет смещение равновесия влево, то есть степень гидролиза уменьшится. Наоборот, связывание ионов Н+ усилит гидролиз. Поэтому при сливании растворов солей, одна из которых гидролизуется по катиону, а другая –по аниону, происходит взаимное усиление гидролиза и гидролиз может протекать необратимо. Так, в растворах FеС1з и Na2S, взятых в отдельности, протекает практически только по первой ступени, и устанавливаются соответственно равновесия (1) и (5). При сливании этих растворов происходит реакция нейтрализации:
Н+ + ОН- = Н2О
или в молекулярной форме
НСI + NaOH = H2O + NaCI,
и равновесие гидролиза (1, (5) смещаются вправо, становятся возможными вторая и третья (3), (4) стадии гидролиза, что приводит к необратимому протеканию совместного гидролиза этих двух солей:
FeCl2 + 3Na2S + 6HOH = 2Fe(OH)3 ↓ + 3H2S ↑ + 6NaCl
или
Fe3+ + 3S2- + 6HOH = 2Fe(OH)3 ↓ + 3H2S ↑
По подобной схеме взаимного усиления гидролиза, приводящего к образованию осадка и газа, взаимодействуют соли, образованные катионами Аl3+, Cr3+, Fe3+ c карбонатами и сульфидами щелочных металлов. Поэтому эти соли невозможно получить реакциями обмена из водных растворов.
 2015-01-07
2015-01-07 6495
6495
