Пример 1:
Написать молекулярные и ионно-молекулярные уравнения гидролиза сульфита калия K2 SO3.
Решение:
Соль образована катионом сильного основания и анионом слабой двухосновной кислоты. Гидролиз идет по аниону. В растворе щелочная реакция среды.
1 ступень: К2SО3 + H2O = KHSO3 + КОН
SO32- + Н2О = HSO3-+OH-
2 ступень: KHSO3 + Н2O = Н2SО3 + КОН
HSO3- + Н2O = Н2SО3 + ОН-
Пример 2:
Написать молекулярные и ионно-молекулярные уравнения гидролиза нитрата свинца (II).
Решение:
Соль образована катионом слабого двухкислотного основания и анионом сильной кислоты. Гидролиз идет по катиону. Раствор имеет кислую реакцию среды.
1 ступень: Pb(NO3)2 + Н2О = (PbOH)NO3 + HNO3
РЬ2+ + Н2О =РЬОН- + Н+
2 ступень: (РЬОН)NО3 + Н2О = Pb(OH)2 + НNО3
РbОН- + Н2О = Pb(OH)2 + Н+
Пример 3:
Написать уравнение гидролиза цианида аммония NH4CN. Какова реакция среды в водном растворе этой соли?
Решение:
Соль образована катионом слабого основания и анионом слабой кислоты, поэтому гидролиз идет как по катиону, так и по аниону:
NH4CN + Н2О = NH4OH + HCN
NH4+ CN- + Н2О = NH4OH + HCN.
Для оценки реакции среды необходимо сравнить константы диссоциации NH4OH и HCN (см. табл.1). Так как константа диссоциации гидроксида аммония больше, чем константа диссоциации синильной кислоты, то гидроксид аммония является более сильным электролитом. В растворе будут преобладать ионы ОН-, следовательно, реакция среды щелочная.
Пример 4:
Учитывая только первую ступень гидролиза 0,5М раствора Na2S, рассчитайте константу гидролиза, степень гидролиза и рН среды.
Решение:
Гидролизу по первой ступени соответствует следующее ионно-молекулярное уравнение:
S2- + Н2О = НS- + OH-
Константа гидролиза Na2S пo первой ступени есть отношение ионного произведения воды к константе диссоциации слабой кислоты HS-.
Кг = Косн /К(HS-)
Константа диссоциации гидросульфид - иона представляет собой константу диссоциации H2S по второй ступени, ее значение можно взять из табл.1.
Кг = Косн /К2(H2S) = 10-14/4х10-14 = 0,25
Степень гидролиза можно рассчитать по формуле:
h= 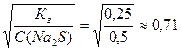
Для нахождения рН среды рассчитаем концентрацию водородных ионов:
[H+] = Kосн/С(Na2S) 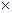 h = 10-14/0,5
h = 10-14/0,5  0.71 = 2.82
0.71 = 2.82  10-14 (моль/л).
10-14 (моль/л).
pH = -lg[H+] = -lg (2.82 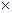 10-14) = 13,55
10-14) = 13,55 
 2015-01-07
2015-01-07 3756
3756
