В растворах многие реакции протекают между ионами; реакции могут быть обратимыми и необратимыми.
Обратимая реакция
– в молекулярном виде:
NaCl + KNO3 Á NaNO3 + KCl;
– в ионном виде:
Na+ + Cl– + K+ + NO3– Á Na+ + NO3– + K+ + Cl–.
Набор ионов в левой и правой части приведенного уравнения одинаков.
Необратимо реакции протекают в том случае, если образуются нерастворимые (1), малодиссоциирующие (2) или газообразные (3) продукты, то есть происходит удаление некоторых продуктов реакции из сферы реакции.
| в молекулярном виде | NaCl + AgNO3 = NaNO3 + AgCl¯, | |
| в полном ионном виде | Na+ + Cl– + Ag+ + NO3– = Na+ + NO3– + + AgCl¯ | |
| в сокращенном ионном виде | Ag+ + Cl– = AgCl¯ | |
| в молекулярном виде | 2NaOH+ H2SO4 = Na2SO4 + 2H2O | |
| в полном ионном виде | 2Na+ + 2OH– + 2H+ + SO42– = = 2Na+ + SO42– + 2H2O | |
| в сокращенном ионном виде | H+ + OH– = H2O | |
| в молекулярном виде | Na2S + H2SO4 = Na2SO4 + H2S | |
| в полном ионном виде | 2Na+ + S2– + 2H+ + SO42– = = 2Na+ + SO42– + H2S | |
| в сокращенном ионном виде | 2H+ + S2– = H2S |
Основы номенклатуры неорганических соединений можно изложить следующим образом:
1 Атомы неметаллов в бинарных соединениях (кроме соединений с водородом) называют, добавляя суффикс – ИД к латинскому названию элемента, например: О–2 – оксид, Cl– – хлорид, I– – йодид, N–3 – нитрид, P–3 – фосфид, S–2 – сульфид и т. д.
2 Формулы большинства сложных неорганических веществ записывают в последовательности «от катиона к аниону» в солях, основаниях и кислотах, например, Na+Cl–, H+2S–2, (NH4)+2SO4–2. В водородных соединениях элементов главных подгрупп IV и V групп на первом месте ставится этот элемент, а затем водород: CH4 – метан, SiH4 – силан, NH3 – аммиак, PH3 – фосфин, AsH3 – арсин и другие.
В России названия оксидов, оснований и солей часто составляют «от аниона к катиону», называя справа налево входящие в это соединение атомы или группы и указывая степень окисления главного (центрального) элемента, если она может иметь разные значения в различных веществах[1]. Например: MgО – оксид магния, SO2 – оксид серы (IV), SO3 – оксид серы (VI), FeCl2 – хлорид железа (II), FeCl3 – хлорид железа (III), Cu(OH)2 – гидроксид меди (II), (ZnOH)2SO4 – сульфат гидроксоцинка (или гидроксосульфат цинка), (NH4)2HPO4 – гидрофосфат аммония.
Таблица 1
Названия некоторых неорганических веществ и анионов или катионов, входящих в их состав
| Формула соединения | Название соединения | Формула кислотного остатка, аниона или катиона и их название |
| HNO2 | азотистая кислота | NO2– – нитрит |
| HNO3 | азотная кислота | NO3– – нитрат |
| NH3 | аммиак | NH4+ – аммоний |
| H2SiO3 | кремниевая (метакремниевая) кислота | SiO32– – силикат |
| HMnO4 | марганцевая кислота | MnO4– – перманганат |
| H2SO3 | сернистая кислота | SO32– – сульфит |
| H2SO4 | серная кислота | SO42– – сульфат |
| H2S | сероводородная кислота | S2– – сульфид |
| H2CO3 | угольная кислота | CO32– – карбонат |
| HClO4 | хлорная кислота | ClO4– – перхлорат |
| HClO3 | хлорноватая кислота | ClO3– – хлорат |
| HClO | хлорноватистая кислота | ClO– – гипохлорит |
| HCl | хлороводородная (соляная) кислота | Cl– – хлорид |
| HF | Фтороводородная (плавиковая) кислота | F– – фторид |
| HPO3 | метафосфорная кислота | PO3– – метафосфат |
| H3PO4 | ортофосфорная кислота | PO43– – ортофосфат (фосфат) |
| H4P2O7 | пирофосфорная кислота | P2O74– – пирофосфат |
| NaOH | гидроксид натрия | OH– – гидроксид |
1 КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
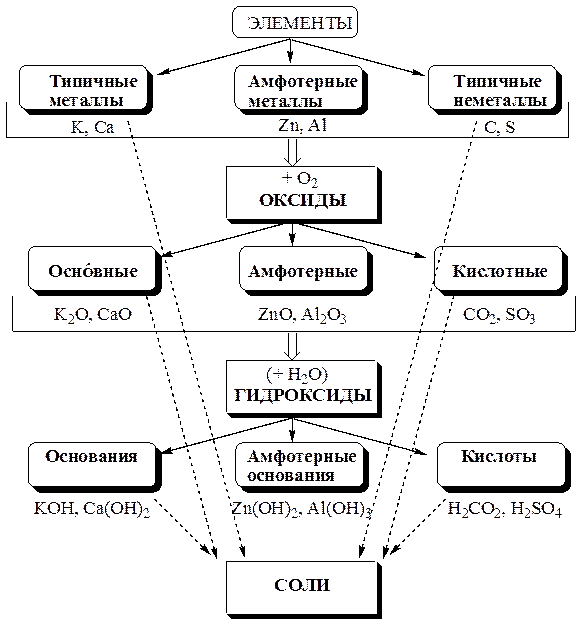
Рис. 1.1. Основные классы неорганических соединений и их взаимосвязь
3 Кислородосодержащие кислоты, имеющие в своем составе атом неметалла или металла в высшей степени окисления, имеют суффикс –НАЯ (кислота), в предыдущей – -ИСТАЯ (кислота), например: HNO3 – азотная кислота и HNO2 – азотистая кислота, H2SO4 – серная кислота и H2SO3 – сернистая кислота.
Оксиды – сложные вещества, состоящие из двух элементов, один из которых кислород в степени окисления –2.
Оксиды классифицируются на солеобразующие (большинство) и несолеобразующие (CO, N2O, NO).
Солеобразующие оксиды подразделяют на кислотные, амфотерные и оснόвные.
 2015-02-27
2015-02-27 1194
1194








