 Рис. 10.4 Рис. 10.4 |
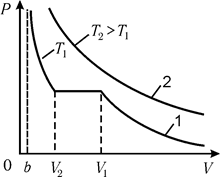
На рис. 10.4 показаны опытные изотермы реального газа. Кривая 2 соответствует более высокой температуре и похожа на изотерму идеального газа с тем отличием, что при сжатии газа его объем не стремится к нулю, а асимптотически приближается к b. Вторая изотерма, соответствующая более низкой температуре, имеет более сложную форму – на ней имеется горизонтальный участок (изотерма-изобара). Опыт показывает, что по мере сжатия реального газа при некотором значении объема V1 он начинает превращаться в жидкость и образуется двухфазное состояние – жидкость + насыщенный пар. Насыщенным называется пар, который находится в состоянии динамического равновесия с собственной жидкой фазой, а его давление не зависит от объема и возрастает с повышением температуры. При достижении системой объема V2 насыщенный пар полностью превращается в жидкость и далее следует ее сжатие. Поскольку жидкость мало сжимаема, эта ветвь изотермы круто поднимается вверх.
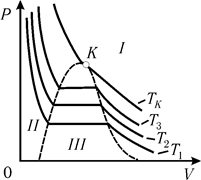 Рис. 10.5 Рис. 10.5 |
С ростом температуры горизонтальный участок, соответствующий двухфазному состоянию системы (жидкость – насыщенный пар), сужается и, в конце концов, превращается в точку (точка К на рис. 10.5). В точке К могут одновременно могут сосуществовать в равновесии газообразное, жидкое и двухфазное состояния. Точка К называется критической, а состояние системы в этой точке критическим. Этому состоянию соответствуют критические параметры вещества – давление, объем и температура.
Критическая температура есть наивысшее значение температуры, при которой еще возможно существование вещества в жидком состоянии.
Критическое давление есть наивысшее давление насыщенного пара данной жидкости.
Критический объем есть наибольший возможный объем данной массы жидкости.
В критическом состоянии теряется различие между жидким и газообразным состоянием, их плотности становятся равными, а поверхностное натяжение и теплота перехода обращаются в нуль.
 2015-02-04
2015-02-04 1591
1591








