Всшсч'ша. i'oiij icmvHuiino инпсрн.шм
Кроме глицеридов ц составе жиров находятся и другие сопутствующие нм вещества: фосфатнды. воскн. стеролы (стернны). красящие вещества, витамины. Все эти вещества растворимы в липндах и переходят в жиры в процессе их выработки
11 ■■ п ф.11111 и. ">то сложные Л11ПИЛЫ, содержащие кроме глицерина и двух жирных кислот остаток фосфорной кисл01ы и азожстое основание.
Важнейшие и наиболее изученные прелставителн фосфатнлов, содержащиеся в природных жирах. — лецитины н кефалнны
Подавляющее большинство фосфатидов содержат в своем составе остатки одной насыщенной (обычно в сс-положенин) и одной ненасыщенной (в (З-положсннн) кислоты, но встречаются и такие, которые образованы только предельными кислотами (их называют насыщенными).
В лецитинах фосфорная кислота связана эфирной связью с азотистым основанием — холимом:
a CHjOCOR, р C1IOCOR;
в'С№0
OCH2CH,N(CH,),OH
а-лецитнн
Возможно присоединение холима и в (3-положеннн с образованием р-лецитина
В кефалинах (|юс<|х>рная кислота связана с азотистым основанием каламином (этаноламнном) I Ю(11 CH?NH> Из жирных кислот в кефаишы чаше всего входят пальмитиновая, стеариновая и олеиновая В жирах лецитин и кефалнн встречаются в смеси. причем в животных жирах преобладает кефалнны. в растительных маслах — лецитины.
Учитывая, что в образовании фосфатидов участвуют разные жирные кислоты, которые, как и остатки фосфорной кислоты. могут быть в а- и (3-положснни. возможно существование многих изомеров.
Несмотря на разнообразие, большинство фосфатидов построено по общему принципу в их состав входят как пглрофобные (углеводородные остатки), так и гидрофильные (полярные) i руины
Построенные таким образом, обладающие двойным сродством (к воде и жиру) фосфатнды имеют высокую эмульсионную активность, поэтому они находят широкое применение в качестве эмуль-■аторов при производстве маргарина, кулинарных жиров и мучных кондитерских изделий.
:i
Фосфат! еды выполняют важную физиологическую роль в жизненных процессах, связанных с проницаемостью клеточных мембран животных и растительных тканей, участвуют в построении нервной и мозговой тканей организма животных и человека
Лецитины в количестве 9 10 % содержатся в желтке яйца, где они впервые были обнаружены и откуда произошло их название (от лат. fecitos желток), в молочном жире— I — 1,5%.
Кефалнны (от лат. cepfuilm голова) впервые выделены из тканей головного мозга, где их содержание достигает 6 %; находятся также в бобах сои и масличных семенах — от0,2 до 5%.
Фосфатнды гигроскопичны — при контакте с водой набухают. теряют растворимость н выпадают в осадок На этом основана очистка масел от фосфатндов и их производство в промышленном масштабе из отстоев масел, что позволило заменить более дорогостоящие яичные желтки, из которых они вырабатывались
При хранении возможен гидролиз фосфатндов на составные части — глицерин, жирные кислоты, фосфорную кислоту и азотистое основание. При гидролизе лецитина может образовываться три метиламин, имеющий запах рыбьего жира, что вызывает порчу продуктов
При взаимодействии с кислородом воздуха фосфатнды легко окисляются, так как в их молекуле содержится непредельная кислота, что ускоряет порчу жиров Поэтому для повышения стойкости растительных масел при хранении фосфатнды удаляют.
Воскн. Это простые липиды. не содержащие фосфора и азота Они представляют собой сложные эфнры высокомолекулярных жирных кислот н высокомолекулярных одноатомных спиртов (реже двухатомных) От жиров отличаются тем, что не содержат глицерина, вместо него — высокомолекулярные спирты; причем и кислоты, и спирты большей частью содержат четное число углеродных атомов (Cm — Об). В общем виде формула выглядит гак:
НгСНзОС^ или R|CH.OCOR. Rj
где R) — спиртовой радикал; R? — жирнокнелотный радикал
Воскн в основном твердые, пластичные вещества, нерастворимые в воде и трудно растворимые в органических растворителях; температура плавления их выше, чем у высокоплавких трнглние-рнлов.
По происхождению воскн делят на растительные и животные. В растениях воскн играют важную роль главным образом как защитное средство, покрывая тонким слоем семена листьев, стебли и плоды; восковой налет предохраняет их от повреждений и лишней потерн воды. Содержание восков в зерне, семенах и плодах невелико — от 0.01 до 0,2 %.
К животным коскам относят спермацет, добываемый ш головы и туши кашалота, и ланолин жиропот, вымываемый m шерсти овеа Их используют для приготовления косметических кремов и мазей, так как они не разлагаются, не прогоркают и хорошо впитываются кожей Широкое применение имеет пчелиный воск, получаемый из пчелиных сот.
При производстве растительных масел воскн переходят в масло в виде мельчайших кристаллов, не выпадающих в осадок; из частичек восков образуется так называемая «сетка», масло становится непрозрачным и теряет товарный вид.
Воскн из масел полностью не удаляются даже при рафинации
При получении прозрачных масел их медленно охлаждают для укрупнения кристаллов восков, которые затем удаляют фильтрованием.
Существуют также минеральные (ископаемые) воскн. например монгановый (горный), получаемый путем экстракции растворителем бурых углей, торфяной — экстракт торфа и др. Эти воскн имеют техническое назначение.
Стеролы (стернны). По химической природе представляют высокомолекулярные циклические одноатомные спирты Встречаются в природных жирах в свободном (стеролы) н связанном состоянии — в виде стерндов (эфиров стеролов и высокомолекулярных жирных кислот)
По происхождению различают три вида стеролов животные эоостеролы, растительные — фитостеролы и микостеролы —- содержатся в грибах и дрожжах.
Основной представитель зоостеролов — холестерол (С?тН4бО), который содержится во всех животных жирах, а также в тканях всех живых организмов, особенно в мозговой и печени, где происходит основной синтез холестерола Содержание холестерина (в %) составляет в сливочном масле — 0,17 -— 0,21, яйцах — 0,57, мясе —0,06 —0,1.
Основной представитель с|*постеролов — ентостерол (С?9Н*0) — содержится в растительных маслах (0.4—1.6 %), и в больших количествах в зародышах зерна пшеницы, риса, кукурузы.
Зоо- и фитостеролы различаются между собой по форме кристаллов и температуре плавления.
При ми крое копировании неомыляемой части, куда переходят стернны при омылении жиров, можно установить природу исследуемого жира или примесь одного жира к другому, определив кристаллическую структуру стеролов
Кристаллы холестерина имеют форму ромба, а снюстерина нрнзм.
Стернны и их производные, несмотря на невысокое содержание. играют исключительно важную роль в жизни всех живых организмов, регулируют обмен веществ в клетке и синтез стероидных
гормонов, участвуют в синтезе жирных кислот Пол действием ультрафиолетовых лучен в животных орюннзмах из стеролов образу-ются витамины группы D.
Красящие вещеспщ. Глнцернды в чистом виде бесцветны: окраску им придаю) красящие вещества пигменты и хром01ены, переходящие из сырья в жиры при их производстве.
К основным пигментам относятся каротиноиды. хлорофилл и госснпол.
Ка/нштютНи —»то группа красящих вапеств от желто-оранжевого до красного цвета Общее название каротиноиды получили от слова «каротин» — желтого пигмента моркови. Известно около 100 каротнноидов
Каротиноиды — полннснасыщснные углеводороды — шлсржат, как правило, 40 углеродных атомов. Их подразделяют на две группы: каротины (углеводородные соединения) и ксантофиллы (кнс-лородосолержащне производные углеволоролов — стгрты. альдегиды, кетоны).
Каротин (C|Oll(6) оранжевый пигмент, по химической природе непредельный углеводород с большим числом двойных связей (9 в углеродной цепи) В маслах содержится в виде смеси а-, S-. у-. 8-нзомеров
Помимо красящих веществ отдельные каротиноиды (в том числе а-, (3-формы) обладают нровитаминнымн свойствами, так как распадаясь в живом организме, они превращаются в витамин А:
С«НИ+ 2Н,0 — 2CjoH*OH
Изомеры у и 8 обладают Ш1Тиокнслнтельнымн свойствами, являясь естественными антнокенд антами
Ксантофилл (C4oHj.4(Orihl — желтьв! пигмент, спиртовое производное каротина
Каротин и ксантофилл сопутствую! друг другу, содержазся почти во всех растительных маслах (подсол! 1ечном. соевом, кукурузном, пальмовом и др.), в i «значительных количествах — в говяжьем и бараньем жирах
При окислении, особенно на свету, каротиноиды постепенно обесцвечиваются и теряют витаминные свойства. При пирогенизации в результате насыщения двойных связен они обесцвечиваются.
Xw/mx/hiii — зеленый тггмент, придаюнигн зеленый оттенок маслам конопляному, льняному, оливковому, рапсовому. В ряде ма-сел (еленый цвет маскируется кароппч-м.мчи (юсос. о.:ивовое)
Хлорофилл — азотсодержащее комплексное соединение с магнием, представляет собой смесь двух видов хлорофилла «а»- сине-зеленою цвет,1 н хлорофилла «в» желю-зеленой окраски, находящихся в соотношении 3.1 на свету, при нагревании хлорофилл ускоряет окисление жиров. Содержание его в жирач очень незначительно
Гмеситм — ядовитыii пигмент черного цвета, характерный дли хлопкового масла.
Молекула госенпола СлНоО- "мест четыре бензольных кольца, т с. два каерталнновых ядра, что и придаст ему ядовитые свойства:
сооо
Для удаления госенпола млею подвергают щелочной рафинации п. in воздействию анграпнловон кислотой. В результате госсипол переходит в нерастворимые соединения и удаляется фильтрованием.
Хлопковое пищевое масло вырабатывают только рафинированным
Хромогены вещества, почти не имеющие окраски или бес-цветные в с веже выработанных жпрл\ о ц:;и;- при ко {действии кислорода воздуха или других агентов переходят в окрашенные соединения. например сезамин кчнжчтного масла из бесивегного становится оранжево-красным.
Витамины. Жирам сопутствуют витамины A. D. Ь и К.
Витамин А (ретинол) — ненасыщенный циклический спирт (общая формчда С\> Н;>ОН (с одним (3-ионовым кольцом):
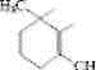
СН,,"' I"'
СН=СН-С=СН-СН=СН-С=СН-СН20Н
Витамин А содержится только в продуктах животного происхождения. так как он синтезируется в живом ор1аннзмс ii: каротина. поступающего с растительной пищей. Богаты витамином А рыбин жир. коровье мзело. печень
Витамин А необходим для нормальною роста живого организма. является защитным фактором прошв инфекций, улучшает острогу зрения
Он легко окисляется кислородом воздуха и теряет биологическую активность. Причем, и' лчченные нерскисные соединения способствуют дальнейшему окислению. Воздействие ультрафиолетового излучении также инактивируст витамин А
Витамины гр\ппы D представлены комплексом витаминов IX. D;, Di. D.i, D. и Dr. которые близки по структуре, но различаются степенью биологической активности, т. е. витамин О как индивидуальное вещество не существует
Витамин D является регулятором кальциевого и фосфорного обмена, способствчет нормалыюмч формированию костной ткани. предупреждает заболевание рахитом
Z5
В химическом отношении витамин D относится к группе стеро-лов, in числа коюрых наиболее распространен эргостерол [С?кН4зОН|- После ультрафиолетового облучения эргостерол приобретает [}-биологнчсскую активность
Витамины (руины D синтезируются только в животных организмах. Богаты витамином!) рыбий жир. жиры печени морских рыб и сливочное масло, а также молочный жир в летний период.
Витамин D стоек к окислению и действию высоких температур, однако ннактнвируется при действии света
Нитаиин Е представляет собой смесь токоферолов — высокомолекулярных циклических спиртов. Участвует в регулировании репродуктивной функции Известны восемь модификации токоферолов, и) коюрых в жирах преобладаю! четыре а, (3, у, 8.
Биологическая активность этих изомеров уменьшается от а- к 5-токоферолу. а антиокислительные свойства возрастают Наибольшая Е-витаминная активность у а-токоферола (Г>911<оО<).
Токоферолы преобладают в растительных маслах — соевом, кукурузном, хлопковом (100—ISO мг%), особенно в масле зародышей пшеницы (180 — 250 мг%), в животных жирах их немного (в говяжьем, свином, бараньем, костном 0,3 — 2,9 мг%), в рыбьих жирах Отсутствуют
Витамин Е относится к числу естественных антиокендантов, защищающих растительные масла от окисления Принимая кислород на себя (Окисляясь), витамин Е ннгибнрует Окисление масел и теряет при этом витаминные свойства.
Витамин Е стоек к действию температур, но разрушается в щелочной среде и при окислении.
Питании К (филлохинон (анпнеморрагнческнн) кровеосганав-ливаюшнй. регулирующий свертываемость кроен) в основе молекулы имеет нафтохнконовос кольцо, к которому присоединены метальная группа и углеводородный остаток спирта (R):
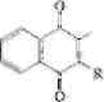
|
| СН, |
Если углеводородный радикал является остатком спирта фнто-ла (СдЛ 1з9011), то это bi i 1-l.mi in К, а если это остаток другого спирта с более длинной цепью (CioH,X)II). то такая структура соответствует витамину К?.
Витамин Kj синтезируется растениями, особенно в зеленых частях, и поступает в организм человека с пишей (богаты внтамн-1юм Кг шпинат, крапива, капуста).
:>:•
Витамин К? спится г рустся микроорганизмами кишечника человека и животных
На основе приролных витаминов К) и К- синтезирован водора-С1воримын кровоостанавливающий препарат «Викасол».
Достаточно высокое содержание вшамина К в конопляном масле, меньше в подсолнечном, льняном, соевом и очень мало в ЖИЮ1НЫХ жирах.
Витамин К разрушается от действия света и щелочен.
Углеводороды. Относятся к группе простых липидов. Большинство из них является производными изопрена:
сн,
CH.-CH-C-CHj
Среди них находятся насыщенные и ненасыщенные углеводороды с нормальной и разветвленной цепью углеродных атомов
Их содержание в жирах невелико (несколько больше в рыбьих жирах), но они оказываю! влияние на вкус и запах жиров Многие углеводороды придаю! жирам неприятные запах и вкус, поэтому itx стараются удалить.
В жирах могут присутствовать белковые, слизистые вещества. которые переходят из перерабатываемою жировою сырья. Белковые примеси вместе с фосфатидами при храпении выпадают в осадок. образуя на дне так называемый фуз. Эти примеси нежелательны, так как ухудшают товарный вид и ускоряют порчу жиров
Присутствующие в жирах в небольших количествах альдешды, кетоны, спирты, кислоты и эфнры, которые переходят из сырья при выработке жиров, обусловливают для каждого вида жира специфические вкус и запах.
При производстве и особенно хранении протекают процессы расщепления жиров, поэтому свободные жирные кислоты всегда присутствуют в большем или меньшем количестве в маслах и животных жирах Накапливающиеся свободные жирные кислоты, а также продукты окисления жиров (пероксиды, альдегиды, кетоны и др.) снижают пищевую ценность жиров.
Классификация жиров
В настоящее время нет единой универсальной классификации жиров, которая отвечала бы требованиям товароведения, научным и техническим целям
Жиры классифицирую! по различным признакам. В зависимости от природы жиров их подразделяют на животные и растительные. Природу жиров можно установить мнкроскопированием их неомыляечон части, где содержатся стерины, различающиеся по форме кристаллов у животных и растительных жиров.
.Т.'
Жиры животного происхождения, в свою очередь, подразделяют на жиры наземных животных (говяжий, баранин, свиной, конский. жиры коровьего молока), жиры птии. жиры рыб и морских. животных; жиры растительного происхождения делят на масла из семян и мякоти плодов
В товароведении в настоящее время пользуются наиболее обшей классификацией, учитывающей ряд признаков: происхождение. консистенцию и физико-химические свойства жиров и масел.
Согласно этой классификации жиры делят на две группы — животные и растительные. Каждую из этих групп в зависимости от количественного содержания твердых триглнцеридов подразделяют на жиры твердые и жидкие.
Твердые животные миры подразделяют на содержащие ннзко-молекулярпые кислоты (коровье масло) и не солержашие тг,м> молекулярные жирные кислоты — говяжий, баранин, свиной и
КОСТНЫЙ
Жидкие животные жи/ы (жиры рыб и морских животных) содержат много высоконепредельных жирных кислот.
Твердые растительные маем подразделяют на твердые жиры. не имеющие в своем составе летучих Ж1грных кислот (масло какао, пальмовое) и твердые жиры, содержащие летучие жирные кислоты (кокосовое, пальмоядровое).
Количественное содержание летучих жирных кислот характеризует показатель число Ренхерга-Мейссдя, а нелетучих жирных кислот — число I [оленске.
Жидкие растите.1Ы1ые маем делят на следующие фуппы:
невысыхающие масла (в их составе преобладает олеиновая кис-лога) оливковое, миндальное и арахисовое. Йодное число эшх масел — не больше 100;
полувысыхающне масла (содержат в равных количествах олеиновую н лннрлсвую кислоты) — подсолнечное, хлопковое, кукурузное и др. Йодное число 100 145,
высыхающие масла (с большим количеством линолевой и лн-ноленовой кислоты) — льняное, конопляное Йодное число — больше 145,
совершенно невысыхающие — масла рииинолевой кислоты, содержащие одну гндрокенльную группу (ОЩ, — касторовое (клещевинное).
Основные свойства жиров
Лнпнды. хотя и включают группу веществ, разнообразных по химическому составу и структуре, обладают такими общими свойствами, как нерастворимость в воде (гндрофобность), растворимость в органических растворителях, плотность меньше единицы
(0.90 — 0.У8 r/смэ. определенная вялость, а также способность к гидролизу. окислению, гидрогенизации. нереэтерификацин и гид-ропереэтернфнкаиим
Жиры в воде не растворяются, но в присутствии эмульгаторов. веществ, обладающих поверхностно-активными свойствами, образуют 'эмульсии. В эмульсионных продуктах (сливки, сметана, майонез. соусы н др) жир лучше усваивается, так как увеличивается поверхность ею соприкосновения с пищеварительными соками.
Трнглнцсрнды природных жиров имеют высокою молекулярную массу (840—.950). Поэтому в обычных условиях они не летучи, т. е. не испаряются при комнатной температуре и нагревании. Однако при повышении температуры до определенных пределов они разлагаются с образованием дыма Температура дычообразовання большинства жиров 250 —300 °С При этом, чем больше степень очистки масла от сопутствующих веществ, т.е.. чем выше степень рафинации, тем выше температура дымообраювання и возможность использования данного жира для кулинарной обработки продуктов. Температура дымообразовання у растительных жиров выше, чем у животных.
Жиры — плохие проводники теплоты, но обладают высокой теплотворной способностью при окислении Энергетическая ценность жиров значительно выше, чем углеводов н белкой, и составляет соответственно 9—-3.7S и 4 ккал/г. или 37.7—15.7 и 16.7 кДж/г. Это обусловлено тем, что по элементарному составу (соотношению углерода, водорода н кислорода) жиры являются менее окисленными соединениями но сравнению с углеводами и белками, и при окислении их в организме выделяется большее количество теплоты.
Физические свойства глнцерндов зависят от состава жирных кисло! и их места расположения в молекуле. В зависимости от лого жиры имеют различную консистенцию — жидкую, мазеобразную или твердую
Температура плавления глицеридов зависит от места положения остатка жирных кислот ос-форма чоноглнцстшдов. например, п.тавнтся при более низкой температуре, чем р-форма. Температура застывания несколько ниже температуры плавления
Растительные часта имеют более низкую температуру плавления и застывания, чем животные жиры.
Жиры хорошо растворяют газы. Кислород в различных жирах |\тстворястся неодинаково — от 4 до Я % и от этого зависит степень окнелясчости жиров при хранении.
Химические свойства жиров обусловлены составом глицеридов и зависят прежде всего от свойств входящих в их состав жирных кислот
Реакции, протекающие в жирах в процессе производства и хранения, приводят к изменениям их физико-химических и органо-лептнческнх показателей.
-«
Гидролиз. Это реакция расщепления (от лат Лц/л» — вата, lysis — разложение) жиров на составные компоненты (глицерин и жирные кислоты), протекает при нч хранении и переработке, физиологических процессах в организме животных и растений, применяется в технике, а также при исследовании жиров.
Общая реакция гидролиза:
CHjOCOR CHjOH
CHOCOR + ЗН20 =Г СНОН + 3RCOOH
CH,OCOR CHjOH
Гидролиз жиров и масел всегда имеет место, если в системе находится вола Это принципиальная установка, но практически реакция протекает очень мелзенно. так как жир не растворяется в воле.
Процесс гидролиза можно ускорить действием различных факторов В связи с >тнм существует четыре способа расщепления жиров: с помощью воды при действии высоких температур, давления и катализатора, омыление, кислотное, ферментативное.
Гидролиз при комнатой температуре практически не происходит. реакция возможна лишь при совместном воздействии трех факторов температуры не ниже 220 "С. давления (12 —15 атм) н катализатора (оксиды цинка, оксиды магния или кхзьция)
Образующиеся при гидролизе свободные жирные кислоты являются катали заторами, т.е. пшролнз жира — процесс автокаталн-тическнй
Реакция протекает последовательно бимолекудярно, участвуют две молекулы, одна молекула глицерида и одна молекула воды
C.H.iOCOR), • Н,0 =ZT C,H,OH(OCOR); i RCOOH CsH^OHfOCORh+HjO i=T C,H,<OHhOCOR + RCOOH
с,н5(он),оаж * н,о — с>н,(Онь + rcooh
Такой процесс гидролиза до конца не идет, так как реакция частично обратима
Расщепление с помощью оснований приводит к образованию солеи жирных кислот Их называют мылами, а реакцию со щелочами — омылением:
С,Н5<ООЖ>,+ 3NaOH = C,Hj(OH>( * 3RCOONa
Реакция протекает в две стадии:
CHOCOR), * 311,0 = C,Hj(OH>(+ 3RCOOH RCOOH ♦ NaOH - RCOONa + H.O
Реакция омыления необратима, идет в одну сторону и до конца, так как образующиеся при гидролизе кислогы переходят в мыла л имио.шсм in ivaiuiiiii ОГ'|\|]>1.'1Ш1с vi-:.ia cokiaioi '■:\льч1к\ увеличивая поверхность соприкосновения жира с водой и тем самым ускоряют реакцию гидролиза При пом катализаторами также являются гидрокенльные ноны (ОН-).
Эту реакцию используют в масложнровой промышленности при рафинации масел для нейтрализации свободных жирных кислот. в мыловарении, а также при исследовании состава жиров для установления коэффициента омыления, зависящего от природы жира
Расщепление с помощью кислот используют в технических целях, например в производстве глицерина В этом случае применяют обычно 5%-ную серную кислоту Водородные ноны Mil кислоты действуют на гидролиз каталитически, а образующиеся сульфо-жнрные кислоты, обладая хорошей эмульгирующей способностью. увеличиваю! поверхность соприкосновения реагирующих веществ и тем самым ускоряют расщепление.
Ферментативное расщепление происходит под действием фермента липазы. Животные и растительные ткани всегда содержат в большем пли меньшем количестве этот жирорасщепляющий фермент, который переходит в жиры при их производстве. Поэтому при хранении, особенно влажных нерафинированных жиров, липаза гидролитует жиры с образованием свободных жирных кислот, наличие коюрых снижает степень свежести жира п ускоряег его порчу, так как свободные жирные кислоты катализируют процессы окисления
В связи с этим в процессе производства и хранения жиров стремятся свести к минимуму действие факторов, ускоряющих гидролиз.
Дтя определения количественного содержания свободных жирных кислот пользуются показателем «кислотное число жира» — количество мг КОН. требующееся для нейтрализации свободных жирных кислот, содержащихся в I г жира
Величина кислотного числа по нормам ГОС'Та должна сосгав-лять не более 0,3 —6 мг КОН для растительных масел и 1,1—3,5 мг КОН для животных жиров.
Окшмснмс. Жиры окисляются атмосферным кислородом в тон или иной степени при их получении, переработке и храпении. В результате воздействия кислорода накапливаются различные продукты распада, что приводит к снижению пищевой ценности, ухудшению вкуса и запаха жиров и даже появлению токсичности. При этом понижается их стойкость к окислению при дальнейшем хранении.
При окислении жиров разрушаются жирорастворимые витамины, эссенциальные жирные кислоты, а образующиеся токсичные продукты окисления (пероксиды. альдегиды, кетоны, окенполн-
меры) кс только вызывают нежелательные вкус и запах, но и оказывают вредное воздействие на организм человека.
Окисленные жиры не рекомендуется использовать в пшапнн не только вследствие утраты ими биологически активных веществ, но и наличия токсичных соединений.
Окисление по своей сущности — процесс химического взаимодействия кислорода с остатками жирных кислот, входящих в состав глицеринов.
Окисление жира под влиянием атмосферного кнеторола называют «автоокислением», так как оно протекает при обычных условиях, без катализаторов, а образующиеся продукты окисления активизируют этот процесс
Лвтоокисление протекает по схеме, которую условно делят на четыре стадии:
индукционный период, когда в жире еше не обнаруживаются продукты окисления Продолжительность ею зависит от химического состава глнцершюв, наличия естественных антиокендаптов (каротнноидов и токоферолов) и от присутствия металлов, которые являются проокнелителямн и ускоряют окисление;
образование первичных продуктов окисления пероксилов (RO>) и гицропероксидов (ROOM),
образование вторичных продуктов окисления — альдегидов, ке-тонов, оксикислот, оксиполнмеров. ннзкомолекулярных жирных кислот;
полимеризация продуктов окисления с образованием оксиполнмеров различной сложности
Накопление продуктов окисления приводит к порче жиров, основные из которых нрогорканне и осалнвание.
Прогорканне обусловлено накоплением альдегидов, кетонов и ннзкомолекулярных жирных кислот, обладающих неприятным горьким вкусом и резким запахом Прогорклые жиры становятся непригодными к употреблению. Таким изменениям наиболее подвержены жиры, содержащие непредельные жирные кислоты, главным образом олеиновую.
Жиры могут прогоркать только при совместном действии воздуха и света, который ускоряет процесс окисления.
При хранении сливочного масла на его поверхности образуется непищевой слой прогорклого жира — «штафф», который подлежит удалению, и масло подвернется зачистке.
Осалнвание связано с накоплением оксикислот, имеющих высокую температуру плавления (например, моноокенстеарнновая плавится только при 84 °С> а дноксистсарнновая — при 136 °С). Такие жиры во рту не тают, вызывают вкусовое оигущенис «сала». Цве1 их белый в результате окисления ши мен гон Осалпванию в большей степени подвержены животные жиры, в том числе и сливочное масло.
12
Механизм окисления жиров довольно сложен, поскольку они представляют собой смесь неоднородных глицеридов, и потому не может быть представлен каким-либо одним уравнением
Наиболее известны перекисная теория Баха-'Энглера (которая была первой научной теорией) и теория свободнораднкальных цепных реакции академика П. 11 Семенова
Согласно теории БахаОнгдера молекула активированного кислорода присоединяется по месту двойной связи с образованием циклического перокенда:
-СН=СН- + 0-0 —- -СН-СН—
1 ' О—О
Дальнейшими превращениями пероксидов обьяснялось обра-юванне альдегидов, кетонов. низкомолекулярных жирных кислот ">гон Teopneii показано значение промежуточных неустойчивых веществ в реакциях окисления
Однако она не давала объяснения природе индукционного периода. а также действию антнокендантов. К тому же, как выяснилось позднее, циклические пероксиды образуются лишь при температуре выше 100 "С
В соответствии с теорией Н.Н.Семенова окисление лнпидов следует рассматршзать как цепную реакцию, которая развивается через образование и превращение свободных радикалов Сущность механизма цепных реакции состойi в том, что они возникаю! н развиваются через образование н инактивацию свободных радикалов Свободные радикалы — это молекулы жирных кислот, один из атомов которого имеет свободную валентность, поэтому они химически активны, легко присоединяю! кислород При этом кислород присоединяется к свободным радикалам, а не по месту двойных связен, как по теории Баха-Энглера Свободный радикал активно соединяется не только с кислородом, но и с другими молекулами.
Свободный радикал образуется при отнятии от молекулы жирной кислоты атома водорода под действием световой, тепловой или ионизирующей энергии:
 2015-04-12
2015-04-12 441
441








