Железные руды представляют собой горные породы, содержащие железо, причем в таком количестве, что руду выгодно перерабатывать. В природе имеется около 20 минералов с высоким содержанием железа (23—72%). Железо в руде находится в виде окислов или солей, соединенных с горной породой. В зависимости от состояния, в котором находится железо, различают четыре вида железных руд.
Бурый железняк содержит Железо в виде водного окисла 2Fe2O3-3H2O. Цвет руды желто-бурый. Эта руда бедна железом (от 35 до 60%), а серы и фосфора, наоборот, содержит больше, чем другие руды. Руда легко восстановима. Крупнейшие ее месторождения находятся на Урале (Бакальские руды с высоким содержанием железа, почти без примесей серы и фосфора). Большие запасы бурого железняка в порошкообразном виде имеются на Керченском полуострове. Известны также Тульское и Липецкое месторождения, руды Кольского полуострова, Тогайского железорудного бассейна.
Красный железняк содержит Железо в виде окисла Fe2O3. Руда красного цвета, содержание железа 55—60%. Это одна из лучших железных руд; она легко восстанавливается, содержит мало серы и фосфора. Богатейшие месторождения красного железняка находятся в Кривом Роге. Крупные запасы красного железняка имеются также в районе Курской магнитной аномалии.
Магнитный железняк содержит Железо в виде окисла Fe304. Руда черного цвета, содержание железа 45—70%. Это наиболее богатая железом руда. Она обладает магнитными свойствами, плотна, восстанавливается с трудом. Залегает главным образом на Урале — в горах Магнитная, Высокая, Благодать. Недавно разведаны месторождения магнитного железняка в Тогайской степи в Казахстане.
Шпатовый железняк содержит Железо в виде соли FeCO3. Эту руду называют сидеритом, или болотной рудой. Она бедна железом (от 30 до 45%). Залежи шпатового железняка встречаются на Урале в районе Бакальского месторождения
Комплексные железные руды содержат, кроме железа, другие металлы (хром, никель, титан, ванадий), восставав-ливаемые в доменной плавке:
хромиты содержат до 37,5% окиси хрома и применяются для выплавки феррохрома, а также в качестве огнеупорного материала; месторождения этих руд находятся на Урале и в Казахстане;
хромоникелевые бурые железняки Орско-Халиловского месторождения содержат 35—45% железа; 1,3—1,5% хрома и 0,3—0,5% никеля;
титаномагнетиты, содержащие 42—48% железа; 0,3—0,4/о ванадия и 4,5—13,0% двуокиси титана, добываются на Урале в Качканарском, Кусинском и Первоуральском месторождениях.
Марганцевые руды применяют, чтобы увеличить содержание марганца в выплавляемых чугунах. Эти руды мягки, рыхлы и гигроскопичны. Содержание окиси марганца в них 28— 40%. Наиболее важным месторождением богатых руд (содержание окиси марганца 48—52%) являются Чиатурское на Кавказе, Никопольское на Украине, у г. Ачинска в Сибири, Уралоазовское и Полуночное на Урале и в Казахстане.
В процессе доменной плавки, кроме железных и марганцевых руд, используют различные отходы: чугунный лом и стружку, загрязненный стальной лом.
Флюсы
Флюсы применяют в доменной плавке для сплавления пустой породы и золы топлива в шлак. При работе доменных печей на коксе используют главным образом известняк (СаСO3). Если в пустой породе находятся основные окислы, применяют кислые флюсы — кварциты.
Топливо
В качестве топлива для доменной плавки используют кокс. Металлургическое топливо должно иметь следующие качества: высокую теплотворную способность, прочность, пористость, невысокую зольность и минимальное содержание серы. Кокс отвечает почти всем этим требованиям. Теплота сгорания кокса 5600 ккал/кг [23 520 кдж/кг], поэтому на нем выплавляют 98% мирового чугуна. Кокс получают из каменного угля при нагревании его до 950—1000° без доступа воздуха в специальных печах. При этом из угля удаляются летучие вещества, а остающаяся часть спекается в твердый и пористый кокс.
Современная коксовая печь (батарея) состоит из 50—70 узких длинных камер емкостью 18—20 мв каждой из них выжигается 12—16 т кокса. Длительность процесса коксования около 12—15 часов. Из одной тонны угля можно получить 750—800 кг кокса и 300—350 м3 высококалорийного газа.
Лучшим коксом считается кузнецкий, содержащий 0,5—0,6% серы и 12—13,5% золы.
Одним из наиболее эффективных частичных заменителей кокса в доменной плавке является природный газ. Стоимость его не превышает 2 руб. за 1000 л3, т. е. в десятки раз ниже стоимости кокса.
Применение природного газа способствует снижению себестоимости чугуна, так как экономится от 10 до 15% кокса.
5. Устройство доменной печи и её работа
Доменная печь — домна) является шахтной печью непрерывного действия. Она имеет форму двух усеченных конусов, сложенных широкими основаниями, между которыми находится цилиндрическая часть, называемая распаром.
Чугун выплавляется из железных руд в специальных печах, называемых доменными. Отсюда процесс получения чугуна из железных руд называется доменным процессом.
Доменная печь имеет большое количество специальных устройств и механизмов, обеспечивающих беспрерывность процесса. Большинство механизмов работает автоматически.
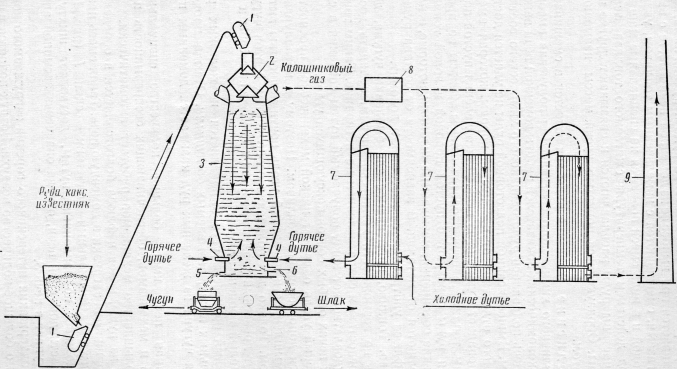
1-скип; 2-засыпной аппарат; 3-доменная печь; 4-фурменные отверстия; 5- чугунная летка; шлаковая летка; 7-воздухонагреватели; 8-газоочистительные устройства; 9-дымовая труба
Смесь из руды, кокса и флюса подготовляется в определенной пропорции для загрузки в доменную печь. Такая смесь называется шихтой. Специальный подъемник — скип 1 перемещающийся по наклонным путям, доставляет шихту к верхней части доменной печи, откуда она через засыпной аппарат 2 поступает в печь 3.
Для поддержания интенсивного горения загружаемого кокса необходимо большое количество воздуха. Воздух подается в печь через специальные отверстия 4 в нижней части печи, которые называются фурменными отверстиями. Чтобы воздух пробил высокий столб шихты и проник во все части печи, а также чтобы имелось достаточное количество кислорода для сгорания всего топлива, воздух вдувают в печь под давлением в 1—2 ати. Воздух подогревается до температуры 600—800°, так как вдувание большого количества холодного воздуха снижает температуру внутри печи, в результате чего процесс плавки руды замедляется.
Подогрев воздуха осуществляется в воздухонагревателях 7, которые строятся рядом с доменной печью. Воздухонагреватели отапливаются доменным (колошниковым) газом, получающимся при выплавке чугуна. Доменный газ предварительно очищается от пыли в специальных газоочистительных устройствах 8. Продукты сгорания из воздухонагревателей удаляются через дымовую трубу 9.
Полученный в печи жидкий чугун опускается в нижнюю ее часть, откуда периодически выпускается через отверстие 5, называемое чугунной леткой. В специальных ковшах большой емкости чугун от доменной печи отвозится в сталеплавильные цехи для переработки в сталь или к разливочной машине для получения чугунных чушек.
Пустая порода, флюсы и зола топлива образуют в печи жидкий шлак, который имеет меньший удельный вес, чем чугун, и поэтому располагается над жидким чугуном. Шлак выпускается из печи через шлаковую летку 6 и направляется для переработки и дальнейшего использования в качестве строительного материала или в шлаковый отвал.
Доменная печь работает беспрерывно по принципу противотока: исходные материалы загружаются сверху, постепенно опускаются вниз, превращаясь в чугун и шлак, а газы, нагревшиеся в нижней зоне печи, поднимаются кверху навстречу исходным материалам.
Печь имеет наружную стальную оболочку, которая называется кожухом, и внутреннюю кладку, или футеровку. Футеровка должна устойчиво сопротивляться износу от трения беспрерывно опускающихся столбом исходных материалов, выдерживать действие высоких температур, не расплавляясь и не давая деформаций. Поэтому для футеровки применяется высококачественный огнеупорный (шамотный) кирпич.
6. Производство стали в конвертерах
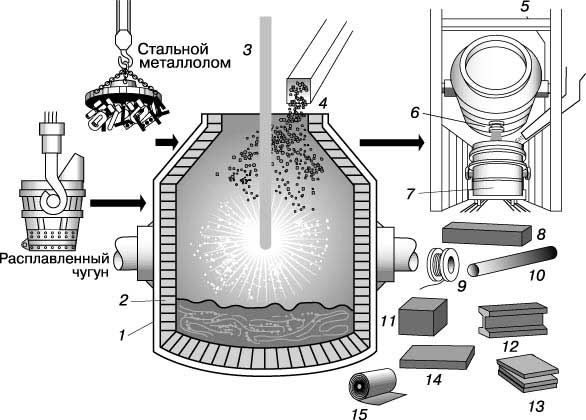
КИСЛОРОДНЫЙ КОНВЕРТЕР с верхней продувкой. 1 – стальной кожух; 2 – огнеупорная футеровка; 3 – кислородная фурма; 4 – завалка флюса; 5 – легирующие добавки; 6 – летка; 7 – ковш; 8 – заготовка; 9 – проволока; 10 – бесшовная труба; 11 – блюм; 12 – балка; 13 – толстолистовая сталь; 14 – листовая заготовка (сляб); 15 – листовой прокат.
Кислородный конвертер с верхней продувкой представляет собой грушевидный сосуд (с открытой узкой верхней горловиной) диаметром ок. 6 м и высотой ок. 10 м, облицованный изнутри магнезиальным (основным) кирпичом. Эта футеровка выдерживает примерно 1500 плавок. Конвертер снабжен боковыми цапфами, закрепленными в опорных кольцах, что позволяет наклонять его. В вертикальном положении конвертера его горловина находится под вытяжным колпаком дымоотводящего камина. Боковое выпускное отверстие, имеющееся с одной стороны, позволяет отделить металл от шлака при сливе. В конвертерном цеху рядом с конвертером обычно имеется загрузочный пролет. Сюда транспортируется в большом ковше жидкий чугун из доменной печи, а в стальных бункерах накапливается металлолом для загрузки. Все это сырье переносится к конвертеру мостовым краном. По другую сторону от конвертера расположен разливочный пролет, где имеются приемный ковш для выплавленной стали и железнодорожные тележки для транспортировки его на разливочную площадку.
Перед началом кислородно-конвертерного процесса конвертер наклоняют в сторону загрузочного пролета и через горловину засыпают металлолом. Затем в конвертер заливают жидкий металл из доменной печи, содержащий около 4,5% углерода и 1,5% кремния. Предварительно металл подвергается десульфуризации в ковше. Конвертер возвращают в вертикальное положение, сверху вводят охлаждаемую водой фурму и включают подачу кислорода. Углерод в чугуне окисляется до CO или CO2, а кремний – до диоксида SiO2. По «течке» (загрузочному лотку) добавляется известь для образования шлака с диоксидом кремния. Со шлаком выводится до 90 % кремния, содержащегося в чугуне. Содержание азота в готовой стали сильно понижается благодаря промывающему действию CO. Приблизительно через 25 мин дутье прекращается, конвертер немного наклоняют, отбирают пробу и анализируют ее. При необходимости в корректировке можно снова возвратить конвертер в вертикальное положение и ввести в горловину кислородную фурму. Если же состав и температура расплава соответствуют спецификациям, то конвертер наклоняют в сторону разливочного пролета и через выпускное отверстие сливают сталь.
7. Получение стали в мартеновских печах
Мартеновский процесс был разработан в 1865 г. французскими металлургами отцом Э. Мартеном и сыном П. Мартеном. Мартеновская печь по устройству и принципу работы является пламенной регенеративной печью. В ее плавильном пространстве сжигается газообразное топливо или мазут. Высокая температура для получения стали в расплавленном состоянии обеспечивается регенерацией тепла печных газов. Рабочее плавильное пространство печи ограничено снизу ванной, образованной подиной и откосами; сверху - сводом; с боков - передней и задней стенками; с торцов - головками. В передней стенке расположены окна, через которые в печь загружают исходную шихту и дополнительные материалы (по ходу плавки), а также берут пробы металла и шлака, удаляют шлак при дефосфорации. Окна закрыты заслонками со смотровыми отверстиями. Готовую плавку выпускают через отверстие, расположенное в задней стенке на нижнем уровне подины. Отверстие плотно забивают малоспекающимися огнеупорными материалами.
Для более полного использования тепла отходящих газов в системе газоотводов установлены регенераторы. Регенераторы выполнены в виде камер, заполненных насадкой из огнеупорного кирпича. Принцип регенерации тепла заключается в том, что насадка одной пары регенераторов некоторое время нагревается до 1250 – 1300 оС отходящими из печи газами. Затем при помощи клапанов направление движения регенераторов меняется автоматически. Через один из нагретых регенераторов в рабочее пространство печи подается воздух, через другой – газ. Проходя через насадку, они нагреваются до 1100- 1200 С. В это время другая пара регенераторов нагревается, аккумулируя тепло отходящих газов. После охлаждения насадки регенераторов до установленной температуры снова происходит автоматическое переключение клапанов.
8. Получение стали в электропечах
Плавка в электропечах имеет ряд преимуществ перед плавкой в конверторах и мартеновских печах. Высокая температура позволяет применять сильноосновные шлаки, вводить большое количество флюсов и достигать максимального удаления из стали серы и фосфора. Для плавки в электропечи не требуется воздуха; окисляющая способность печи невысока, поэтому количество FeO в ванне незначительно, сталь получается достаточно раскисленная и плотная. Благодаря высокой температуре в печи можно получить легированные стали с тугоплавкими элементами: вольфрамовые, молибденовые и др.
Исходными материалами для плавки в электропечах являются стальной лом, железная руда, окалина. Передельный мартеновский чугун применяют только для сталей с высоким содержаниемуглерода, но чаще заменяют электродным боем или малосернистым коксом.
В качестве флюсов в основных печах применяют известь, а в кислых печах — кварцевый песок. Для разжижения основных шлаков применяют плавиковый шпат, боксит и шамотный бой, а для кислых шлаков — известь и шамотный бой. Для раскисления стали, кроме обычных ферросплавов, применяют комплексные раскислители (АМС, содержащий по 10% кремния, марганца и алюминия, силикомарганец, силикокальций).
 Все материалы, загружаемые в электрические печи, должны быть сухими, чтобы не произошло насыщения стали водородом от разложения влаги.
Все материалы, загружаемые в электрические печи, должны быть сухими, чтобы не произошло насыщения стали водородом от разложения влаги.
Электрические печи для плавки металла делятся на три вида: печи сопротивления, дуговые и индукционные.
Для плавки стали применяют в основном дуговые и индукционные печи, а в печах сопротивления плавят сплавы цветных металллов.
Дуговые печи н аиболее распространены в промышленности, так как устройство и эксплуатация их несложны, коэффициент полезного действия высок и, кроме того, в них можно выплавлять самые разнообразные сорта стали и сплавов цветных металлов. В дуговых печах электроэнергия превращается в тепловую энергию дуги, которая передается плавящейся шихте посредством излучения.
Индукционные печи применяют для выплавки высоколегированных сталей и сплавов с низким содержанием углерода, а также для производства тонкостенного фасонного литья специальными методами (по выплавляемым моделям, под давлением и т. п.).
Электрошлаковый переплав стали представляет собой совершенно новый метод получения высококачественных легированных сталей, в том числе и быстрорежущих. Он разработан Институтом электросварки им. Е. О. Патона Академии наук УССР.
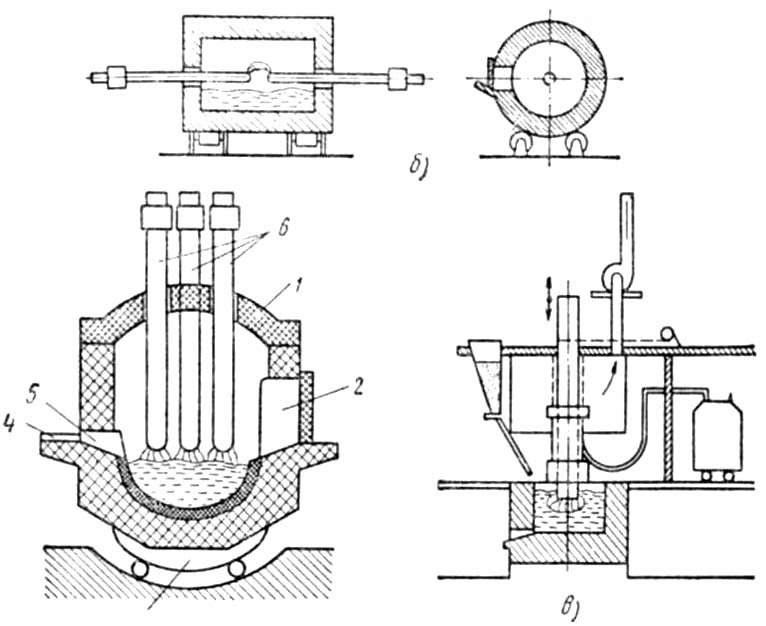
Сущность его состоит в том, что слитки из стали, полученной в обычных печах, перерабатываются на электроды для последующей переплавки их в электрошлаковой печи. плавление электродов происходит не за счет тепла электрической дуги, а за счет тепла, выделяющегося в слое расплавленного шлака, служащего сопротивлением при прохождении через него электрического тока. Принцип электрошлакового переплава очень прост. Электрод-слиток 1 (рис. 3) диаметром до 150 мм и длиной от 2 до б м вводят в медный водоохлаждаемый кристаллизатор 2, который представляет собой полый цилиндр. К дну кристаллизатора прикреплен поддон 5 с затравкой 4 — это шайба из переплавляемой стали. На затравку насыпают электропроводный флюс из порошка алюминия с магнием. В зазор между слитком-электродом и стенкой кристаллизатора засыпают рабочий флюс 3, состоящий из Аl2O3, CaFe2 и СаО.
9. Прогрессивные способы получения стали
Одним из прогрессивных способов получения сложных и высоколегированных сталей является электрометаллургический: плавка в электрических дуговых и индукционных печах.
Сталь особо высокого качества выплавляют в вакуумных электрических печах, а также путем электрошлакового, плазменного переплава, электронно-лучевой плавки.
10. Общее сведения о металлах. Классификация металлов.
Металлы — материалы кристаллической структуры, обладающие рядом специфических свойств: металлическим блеском; высокой электропроводностью и теплопроводностью; положительным температурным коэффициентом электросопротивления; электронной эмиссией; при нормальных условиях находятся в твердом состоянии (исключением является ртуть).
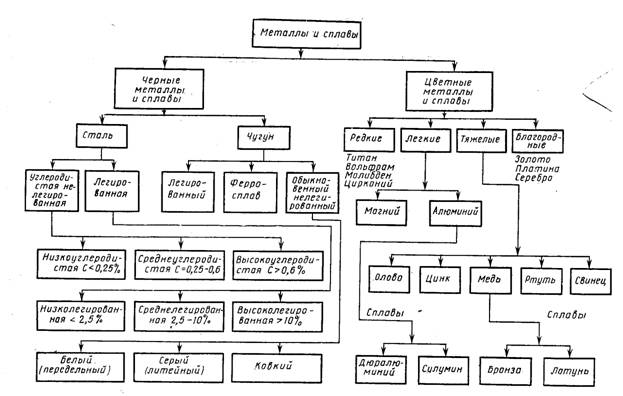
По внешнему виду металлы подразделяются на черные и цветные. К черным металлам относят железо и сплавы на его основе, остальные металлы принято относить к цветным.
Черные металлы, используемые в производстве хозяйственных товаров, представлены двумя сплавами: сталью (сплав железа с углеродом, с содержанием последнего не более 2,14%) и чугуном (сплав железа с углеродом, с содержанием последнего более 2,14%).
Чугун выплавляют из железной руды в доменных печах.
Сталь получают из чугуна путем выжигания из него избытка углерода кислородом воздуха.
11. Атомно-кристаллическое строение металлов.
Под атомно-кристаллической структурой понимают взаимное расположение атомов, существующее в кристалле. Кристалл состоит из атомов (ионов), расположенных в определенном порядке, который периодически повторяется в трех измерениях.
В кристаллах существует не только ближний, но и дальний порядок размещения атомов, т. е. упорядоченное расположение частиц в кристалле сохраняется на больших участках кристаллов. Для описания атомно-кристаллической структуры пользуются понятием пространственной или кристаллической решетки.
Кристаллическая решетка представляет собой воображаемую пространственную сетку, в узлах которой располагаются атомы (ионы), образующие металл (твердое кристаллическое тело).
Наименьший объем кристалла, дающий представление об атомной структуре металла во всем объеме, получил название элементарной кристаллической ячейки.
12. Свойства металлов и сплавов
К основным механическим свойства относят:
- прочность
- пластичность
- твердость
Прочность – способность материала сопротивляться разрушению под действием нагрузок.
Пластичность – способность материала изменять свою форму и размеры по действием внешних сил.
Твердость – способность материала сопротивляться проникновению в него другого тела.
К физическим свойства относят:
- цвет
- плотность
- температуру плавления
- теплопроводность
- магнитные свойства
Цвет – способность металлов отражать излучение с определенной длиной волны. Например, медь имеет розовато-красный цвет, алюминий – серебристо-белый.
Плотность металла определяется отношением массы к единице объема. По плотности металлы делят на легкие (менее 4500 кг/м3) и тяжелые.
Температура плавления – температура, при которой металл переходит из твердого состояния в жидкое. По температуре плавления различают тугоплавкие (вольфрам – 3416 оС, тантал – 2950 оС и др.) и легкоплавкие (олово – 232 оС, свинец – 327 оС). В единицах СИ температуру плавления выражают в градусах Кельвина (К).
Теплопроводность – способность металлов передавать тепло от более нагретых участков тела к менее нагретым. Большой теплопроводностью обладают серебро, медь, алюминий. В единицах СИ теплопроводность имеет размерность Вт/(м·К).
Способность металлов проводить электрический ток оценивают двумя противоположными характеристиками – электрической проводимостью и электрическим сопротивлением.
Электропроводность оценивается в системе СИ в сименсах (См). Электросопротивление выражают в омах (Ом). Хорошая электропроводность необходима, например, для токонесущих проводов (их изготавливают из меди, алюминия). При изготовлении электронагревательных приборов и печей необходимы сплавы с высоким электросопротивлением (из нихрома, константана, манганина). С повышением температуры металла его электропроводность уменьшается, а с понижением – увеличивается.
Магнитные свойства выражаются в способности металлов намагничиваться. Высокими магнитными свойствами обладают железо, никель, кобальт и их сплавы, которые называют ферромагнитными. Материалы с магнитными свойствами применяют в электротехнической аппаратуре и для изготовления магнитов.
Химические свойства характеризуют способность металлов и сплавов сопротивляться окислению или вступать в соединение с различными веществами: кислородом воздуха, растворами кислот, растворами щелочей и др.
К химическим свойствам относят:
- коррозионную стойкость
- жаростойкость
Коррозионная стойкость – способность металлов сопротивляться химическому разрушению под действием на их поверхность внешней агрессивной среды (коррозия происходит при вступлении в химическое взаимодействие с другими элементами).
Жаростойкость – способность металлов сопротивляться окислению при высоких температурах
Химические свойства учитывают в первую очередь для изделий или деталей, работающих в химически агрессивных средах:
- емкости для перевозки химических реактивов
- трубопроводы химических веществ
- приборы и инструменты в химической промышленности
13. Понятия: Сплав, компонент, фаза, механические смеси, твёрдые растворы, химические соединения.
Сплав — макроскопически однородный металлический материал, состоящий из смеси двух или большего числа химических элементов с преобладанием металлических компонентов.
Компоненты — вещества, образующие систему. В качестве компонентов выступают чистые вещества и химические соединения, если они не диссоциируют на составные части в исследуемом интервале температур.
Фаза — однородная часть системы, отделенная от других частей системы поверхностного раздела, при переходе через которую структура и свойства резко меняются.
МЕХАНИЧЕСКАЯ СМЕСЬ (в металловедении) - строение сплава из двух компонентов, которые неспособны к взаимному растворению в твердом состоянии и не вступают в химическую реакцию с образованием соединений. Сплав состоит из кристаллов компонентов А и Б
Твёрдые растворы — фазы переменного состава, в которых атомы различных элементов расположены в общей кристаллической решётке.
Хими́ческое соедине́ние — сложное вещество, состоящее из химически связанных атомов двух или более элементов (гетероядерные молекулы). Некоторые простые вещества также могут рассматриваться как химические соединения, если их молекулы состоят из атомов, соединённых ковалентной связью (азот, кислород, иод, бром, хлор, фтор, предположительно астат).
14. Кристаллизация металлов и сплавов
Процессы кристаллизации металлов и сплавов, являющиеся процессами перехода их из жидкого состояния в твердое, связаны с выделением скрытой теплоты кристаллизации. Для того чтобы происходил процесс кристаллизации металла или сплава, его необходимо все время охлаждать (отводить, отнимать от него тепло).
При рассмотрении процессов кристаллизации мы прежде всего должны иметь в виду определенный объем жидкого металла или сплава, который отдает тепло, и форму, которая принимает его. Передача тепла от жидкого металла и сплава форме проходит не мгновенно, так как теплопроводность жидкого металла или сплава и формы имеет определенные конечные значения. Поэтому одновременная кристаллизация всего объема металла или сплава в форме невозможна даже при одинаковых температурах во всех точках его объема.
15. Экспериментальное построение диаграмм состояния двойных сплавов
16. Правила фаз и отрезков
Фазами могут быть жидкие растворы, твердые растворы и химические соединения. Следовательно, однородная жидкость представляет собой однофазную систему, механическая смесь двух видов кристаллов — двухфазную систему и т. д.
Под числом степеней свободы (вариантностью) системы понимают число внешних и внутренних факторов (температура, давление и концентрация), которые можно изменять без изменения числа фаз в системе.
Количественную зависимость между числом степеней свободы системы, находящейся в равновесном состоянии, и числом компонентов и фаз принято называть правилом фаз (закон Гиббса). Правило фаз для металлических систем выражается уравнением
С = К - Ф + m,
где С —число степеней свободы системы; К —число компонентов; Ф — число фаз; т — число внешних факторов (температура, давление).
Если принять, что все превращения происходят при постоянном давлении (Р = const), это уравнение примет следующий вид: С = К – Ф + 1, где 1 - внешний переменный фактор (температура).
Пользуясь правилом фаз, рассмотрим, как происходит изменение числа степеней свободы однокомпонентной системы для случая расплавленного чистого металла (К=1; Ф=1) С = 1-1 + 1 = 1, т.е. температуру можно изменять не меняя числа фаз. Такое состояние системы называют моновариантным (одновариантным). В процессе кристаллизации Ф = 2 (две фазы — жидкая и твердая), а К=1, тогда С= 1-2+1=0. Это значит, что две фазы находятся в равновесии при строго определенной температуре (температура плавления), и она не может быть изменена, пока одна из фаз не пропадет. Такое состояние системы называют нонвариантным (безвариантным).Для диухкомпонентной системы, находящейся в жидком состоянии (К = 2; Ф=1), правило фаз имеет вид С = 2-1 + 1=2, такая система называется бивариантной (двухвариантной). В этом случае возможно изменение двух факторов равновесия (температуры и концентрации), число фаз при этом не меняется. Для этой же системы при существовании двух фаз (жидкой и твердой) К=2, Ф = 2, согласно правилу фаз С = 2—2+1 = 1, т.е. с изменением температуры концентрация должна быть строго определенной.
Применение правила фаз для диаграммы состояния первого типа(см. рис.). Пользуясь этой диаграммой, можно определить фазовое состояние сплавов любого состава при любой температуре. Так, например, в области 1 существует одна фаза — жидкий раствор. Правило фаз запишется в виде С = К – Ф + 1 = 2- 1 + 1 = 2, т. е. система имеет две степени свободы. Для остальных областей 2, 3, 4 и 5 система характеризуется одной степенью свободы (С = 2 – 2 + 1 = 1).
17. Диаграмма состояния сплавов с механической смесью
22. Структурные составляющие железоуглеродистых сплавов
Феррит – это твёрдый раствор углерода в α-железе. Максимальная концентрация углерода – всего лишь 0,025% (точка P). При комнатной температуре – не выше 0,006%. Феррит мягок и пластичен.
Аустенит – твёрдый раствор углерода в γ-железе. Максимальная концентрация углерода — 2,14 % (точка E). Аустенит имеет невысокую твёрдость, пластичен, не магнитится.
Цементит — химическое соединение железа с углеродом (карбид железа, Fe3C). Концентрация углерода, соответственно, постоянная – 6,67 % углерода. Цементит очень твёрд, хрупок, непластичен.
Необходимо так же выделить 2 структурные составляющие железоуглеродистых сплавов:
Перлит (эвтектоид) – механическая смесь 2 фаз – пластинок/зерен феррита и цементита. Перлит образуется в результате перлитного превращения аустенита («свободного» или входящего в состав ледебурита) с концентрацией углерода 0,8% при прохождении ниже линии PSK:
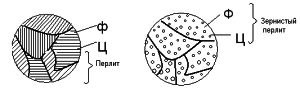 А0,8→Ф0,025 + Ц6,67
А0,8→Ф0,025 + Ц6,67
Железо при этом переходит из γ-формы в α-форму. Механические свойства сильно зависят от размера (дисперсности) частичек, из которых состоит данный перлит.
Ледебурит (эвтектика) – механическая смесь 2 фаз – пластинок/зерен аустенита и цементита. Ледебурит образуется из жидкой фазы с концентрацией углерода 4,3% при прохождении ниже линии ECF:
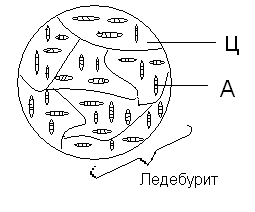 Ж4,3→А2,14 + Ц6,67
Ж4,3→А2,14 + Ц6,67
Структура ледебурита. Ц — цементит, А — аустенит.
23. Диаграмма состояния сплавов железо-цементит
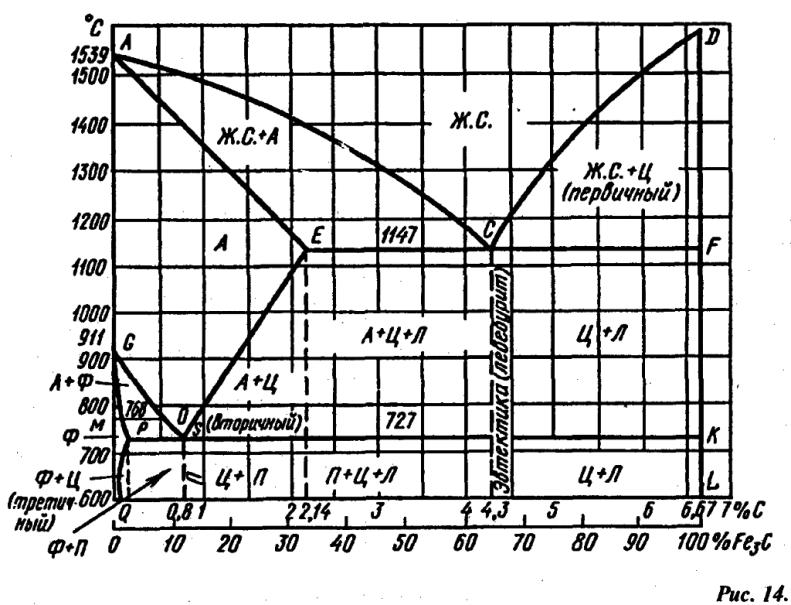 Диаграмма железо-углерод (железо-цементит) – это графическое отображение структуры сплавов, состоящих только из железа и углерода, в зависимости от исходной средней концентрации углерода и текущей температуры сплава. Диаграмма железо-углерод позволяет понять процессы, происходящие при термообработке стали.
Диаграмма железо-углерод (железо-цементит) – это графическое отображение структуры сплавов, состоящих только из железа и углерода, в зависимости от исходной средней концентрации углерода и текущей температуры сплава. Диаграмма железо-углерод позволяет понять процессы, происходящие при термообработке стали.
Диаграмма железо-углерод (железо-цементит). Упрощенная
линия ACD. Линия ликвидус. При охлаждении сплавов ниже нее начинается их кристаллизация;
линия AECF. Линия солидус. При охлаждении сплавов ниже нее весь сплав переходит в твердое состояние;
линия ECF. Иногда называется линией ледебуритного превращения. При охлаждении сплавов с содержанием углерода выше 2,14% ниже нее жидкая фаза превращается в ледебурит;
линия PSK. Линия перлитного превращения. При охлаждении сплавов ниже нее аустенит превращается в перлит.
Отметим несколько важных точек на диаграмме:
точка E. Точка максимального насыщения аустенита углеродом – 2,14%, при температуре 1147°С;
точка P. Точка максимального насыщения феррита углеродом – 0,025%, при температуре 727°С;
точка S. Точка «0,8% С-727°С» превращения аустенита с концентрацией углерода 0,8% в перлит (эвтектоид) той же средней концентрации;
точка C. Точка «2,14 % С-1147°С» превращения жидкости с концентрацией углерода 2,14% в ледебурит (эвтектику) той же средней концентрации.
 2015-04-30
2015-04-30 3988
3988
