Классический вариант конкуретного ингибирования проявляется при взаимодействии ингибитора с активным центром фермента. Структура аналога субстрата, действующего как ингибитор - I, обычно сходна со структурой самого субстрата. Поэтому ингибитор может обратимо связываться с ферментом, образуя вместо комплекса [ES] фермент-ингибиторный комплекс [EI]. Если в реакционной смеси одновременно присутствуют субстрат и ингибитор указанного типа, они конкурируют за один и тот же центр связывания на поверхности фермента. Один из наиболее подробно изученных примеров конкурентного ингибирования – это ингибирование сукцинат-дегидрогеназы малоновой кислотой, которая конкурирует с субстратом фермента – сукцинатом (–ООС–СН2–СН2–СОО–) за один и тот же активный центр.
Сукцинат-дегидрогеназа катализирует образование фумаровой кислоты за счет отщепления атомов водорода от каждого из двух a-углеродных атомов сукцината. Малоновая кислота, (–ООС–СН2–СОО–) выступающая в роли ингибитора способна связываться с ферментом, образуя комплекс [EI]. От единственного Сa-атома малоната отщепление атома водорода невозможно. Поэтому образующийся комплекс [EI] может только распадаться на свободный фермент и ингибитор.
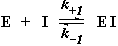 |
Для этой обратимой реакции связывания ингибитора с ферментом:
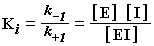 |
константа диссоциации (константа ингибирования) комплекса фермент-ингибитор, К i, равна:
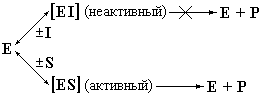 |
Действие конкурентных ингибиторов можно представить в виде следующей схемы:
Как упоминалось выше, скорость образования продукта зависит только от концентрации комплекса [ES]. Предположим, что I очень прочно связывается с ферментом (величина K i мала). Тогда количество свободного фермента [E], который мог бы связывать S, образуя комплекс [ES] с распадом последнего на E + Р, будет весьма мало. Таким образом, скорость реакции, т.е. скорость образования Р будет мала. При той же концентрации слабо связывающегося ингибитора (величина K i велика) катализируемая реакция существенно не замедлится. Предположим теперь, что при фиксированной концентрации ингибитора, I, концентрация субстрата растет. Это повышает вероятность образования комплекса [ES] по сравнению с концентрацией комплекса [EI]. С увеличением отношения [ES]/[EI] будет расти и скорость реакции. При достаточно высокой концентрации S концентрация комплекса [EI] станет исчезающе мала. Но тогда скорость катализируемой реакции будет такой же, как и в отсутствие I.
 2015-05-12
2015-05-12 660
660