4.3.1 Электролитическая диссоциация
Электролиты – вещества, которые при растворении подвергаются диссоциации на ионы. В результате раствор приобретает способность проводить электрический ток, т.к. в нем появляются подвижные носители электрического заряда. Например, при растворении в воде уксусная кислота диссоциирует на ион водорода и ацетат-ион:
CH3COOH  H+ + CH3COO–
H+ + CH3COO–
Необходимым условием, определяющим возможность процесса электролитической диссоциации, является наличие в растворяемом веществе ионных * или полярных связей *, а также достаточная полярность * самого растворителя *. Количественная оценка процесса электролитической диссоциации дается двумя величинами: степенью диссоциации a и константой диссоциации K.
Степенью диссоциации (a) электролита называется отношение числа его молекул, распавшихся на ионы, к общему числу молекул электролита в растворе, т. е. 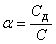 . Так, если C =0,1 моль/л, а концентрация диссоциированной части вещества С д=0,001 моль/л, то для растворенного вещества a=0,001/0,1=0,01, или a=1%. Степень электролитической диссоциации зависит как от природы растворенного вещества, так и от концентрации раствора, увеличиваясь с его разбавлением.
. Так, если C =0,1 моль/л, а концентрация диссоциированной части вещества С д=0,001 моль/л, то для растворенного вещества a=0,001/0,1=0,01, или a=1%. Степень электролитической диссоциации зависит как от природы растворенного вещества, так и от концентрации раствора, увеличиваясь с его разбавлением.
Электролиты можно разделить на две большие группы: сильные и слабые. Сильные электролиты диссоциируют практически полностью. К сильным электролитам относятся, например, H2SO4Серная кислота., HClСоляная кислота., HNO3Азотная кислота., H3PO4Ортофосфорная кислота., HClO3Хлорноватая кислота., HClO4Хлорная кислота., KOHГидроксид калия., а также хорошо растворимые соли: NaClХлорид натрия (поваренная соль)., KBrБромид калия., NH4NO3Нитрат аммония (аммиачная селитра). и др. Для слабых электролитов устанавливается равновесие между недиссоциированными молекулами и ионами. К слабым электролитам относятся плохо растворимые соли (см. таблицу растворимости), вода и большинство органических кислот (например, уксусная CH3COOH, муравьиная HCOOH), а также неорганические соединения: H2CO3Угольная кислота., H2SСероводородная кислота., HCNЦиановодородная (синильная) кислота., H2SiO3Метакремниевая кислота., H2SO3Сернистая кислота., HNO2Азотистая кислота., HClOХлорноватистая кислота., HCNOЦиановая кислота., NH4OHГидроксид аммония. и др.
Константа равновесия для процесса диссоциации называется константой диссоциации (K). В общем случае для электролита, диссоциирующего на два иона:
АВ  А+ + В–
А+ + В–
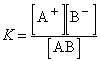
Для приведенного выше процесса диссоциации уксусной кислоты:
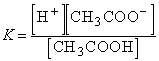
Если обозначить концентрацию электролитаВ приведенных здесь выражениях используется Молярная концентрация., распадающегося на два иона, через C, то
[A+] = [B–] = a C; [AB] = C(1–a);
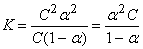
Это уравнение соответствует закону разбавления Оствальда. Если электролит слабый, и диссоциация очень мала (a<<1), то закон разбавления Оствальда упрощается:
K =a2 C; 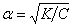 .
.
Таким образом, степень диссоциации возрастает с разбавлением раствора.
Многоосновные кислоты, а также основания многовалентных металлов диссоциируют ступенчато. Например:
H2CO3  H+ + HCO3–
H+ + HCO3–
HCO3–  H+ + CO32–
H+ + CO32–
Первое равновесие – диссоциация по первой ступени – характеризуется константой
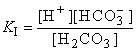
Для диссоциации по второй ступени:
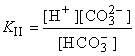
В случае угольной кислоты константы диссоциации имеют следующие значения: K I = 4,3×10–7, K II = 5,6×10–11. Для ступенчатой диссоциации всегда K I> K II> K III>¼, т.к. энергия, которую необходимо затратить для отрыва иона, минимальна при отрыве его от нейтральной молекулы.
4.3.2 Произведение растворимости. Водородный показатель
Растворение твердых электролитов * прекращается, когда образуется насыщенный раствор, в котором устанавливается гетерогенное равновесие между твердой фазой и перешедшими в раствор ионами. Например:
CaSO4 (т)  Ca2+(р-р) + SO42–(р-р)
Ca2+(р-р) + SO42–(р-р)
В выражение константы этого гетерогенного равновесия не входит концентрация твердой фазы (см. особенности закона действия масс для гетерогенных процессов):
K= [Ca2+][SO42–]
В насыщенном растворе твердого электролита произведение концентраций его ионов есть величина постоянная при данной температуре. Она называется произведением растворимости.
ПР(CaSO4) = [Ca2+][SO42–]
Если молекула электролита содержит несколько одинаковых ионов, то концентрации этих ионов, согласно закону действия масс *, должны быть возведены в соответствующие степени. Например:
PbI2  Pb2+ + 2 I–
Pb2+ + 2 I–
ПР(PbI2) = [Pb2+][I–]2
Зная произведения растворимости, можно решать вопросы, связанные с образованием или растворением осадков при химических реакциях. Например, пусть диссоциация соли АВ происходит на два иона:
АВ  А+ + В–
А+ + В–
Обозначив растворимость через s (моль/л), получим [A+]=[B–]= s, ПР=[A+][B–]= s 2. На практике чаще возникает обратная задача определения растворимости. Для соли, диссоциирующей на два иона, 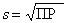 . Значения ПР можно найти в химических справочниках. Например, ПР(AgCl)=1,8·10–10, ПР(AgBr)=6·10–13, ПР(BaSO4)=1,1·10–10, ПР(HgS)=10–52. Если соль имеет общую формулу AB2, то она диссоциирует по уравнению:
. Значения ПР можно найти в химических справочниках. Например, ПР(AgCl)=1,8·10–10, ПР(AgBr)=6·10–13, ПР(BaSO4)=1,1·10–10, ПР(HgS)=10–52. Если соль имеет общую формулу AB2, то она диссоциирует по уравнению:
AB2  A2+ + 2 B–
A2+ + 2 B–
В этом случае [A2+]= s, [B–]=2 s, ПР=[A2+][B–]2= s ·(2 s)2=4 s 3, 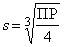 .
.
Если фактическое произведение концентраций (ПС) ионов в некотором растворе превышает значение произведения растворимости, т.е. ПС>ПР, то раствор является пересыщенным *, и из него выпадает осадок. Условие растворения осадка (ненасыщенности раствора): ПС<ПР. Оба процесса идут с одинаковой скоростью, и система приходит в состояние равновесия при ПС=ПР (насыщенный раствор).
Чистая вода обладает незначительной электрической проводимостью, которая объясняется небольшой диссоциацией воды на ионы водорода и гидроксид-ионы:
H2O  H+ + OH–
H+ + OH–
Такой процесс называется автопротолизом (самодиссоциацией). По величине электропроводности чистой воды можно вычислить концентрации ионов H+ и OH–. При 25°С они равны по 10–7 моль/л.
Выражение для константы диссоциации * воды имеет вид:
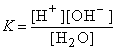 ,
,
откуда [H+][OH–]= K [H2O]= Kw.
В воде и разбавленных водных растворах концентрацию воды можно считать постоянной: [H2O]=55,5 моль/лЭта величина получается как масса одного литра воды (1000 г/л), деленная на молярную массу воды (18 г/моль)., поэтому Kw – константа. Выражение, полученное для Kw, показывает, что в воде и разбавленных водных растворах при постоянной температуре произведение концентраций ионов водорода и гидроксид-ионов есть величина постоянная. Она называется ионным произведением воды. При 25°С Kw =10–14.
В кислых растворах больше концентрация ионов водорода, в щелочных – концентрация ионов OH–. Однако произведение этих молярных концентраций всегда остается постоянным. Если, например, к чистой воде добавить столько кислоты, чтобы концентрация ионов водорода повысилась до 10–3 моль/л, то концентрация гидроксид-ионов станет равной 10–11 моль/л. Следовательно, если известна величина [H+], то однозначно определяется величина [OH–]. Поэтому степень кислотности или щелочности раствора можно количественно охарактеризовать концентрацией ионов водорода:
Нейтральный раствор [H+]=10–7 моль/л;
кислый раствор [H+]>10–7 моль/л;
щелочной раствор [H+]<10–7 моль/л.
Наиболее часто используют не концентрацию [H+], а ее десятичный логарифм, взятый с обратным знаком:
pH= –lg [H+]
Эта величина называется водородным показателем. Например, если [H+]=10–5 моль/л, то pH=5; если [H+]=10–9 моль/л, то pH=9. Отсюда следует, что в нейтральном растворе pH=7, в кислом растворе pH<7, в щелочном растворе pH>7. Иногда пользуются значением гидроксидного показателя pOH= –lg[OH–]. При 25°С выполняется равенство: pH+pOH=14.
Для многих процессов величина pH очень важна (для жизнедеятельности растений и животных – pH крови, почвенного раствора). Свойства природных вод, в частности их коррозионная активность, сильно зависят от pH.
4.3.3 Смещение ионных равновесий
Ионное равновесие, как и любое другое, смещается при изменении концентрации одного из ионов. Например, если в раствор уксусной кислоты, диссоциирующей по уравнению
CH3COOH  H+ + CH3COO–
H+ + CH3COO–
ввести какую-либо соль этой кислоты и тем самым увеличить концентрацию ионов CH3COO–, то в соответствии с принципом Ле-Шателье * равновесие смещается влево. Отсюда следует, что введение в раствор слабого электролита * одноименных ионов (т.е. ионов, одинаковых с одним из ионов электролита) уменьшает степень диссоциации * этого электролита.
Аналогично нарушается равновесие в случае малорастворимого электролита (соли). Например, если к насыщенному раствору сульфата кальция CaSO4 добавить другой, хорошо растворимый сульфат (K2SO4), то вследствие увеличения концентрации ионов SO42– равновесие сместится в сторону образования кристаллов (образуется осадок CaSO4). Этот процесс прекратится, когда произведение концентраций [Ca2+] и [SO42–] станет равно произведению растворимости *, т.е. установится новое состояние равновесия.
На основании рассмотренных примеров можно сделать следующий вывод: реакции в растворах электролитов всегда идут в сторону образования наименее диссоциированных или наименее растворимых веществ. Из этого, в частности, следует, что сильные кислоты вытесняют слабые из растворов их солей:
CH3COONa + HCl = CH3COOH + NaCl
Суть этой реакции более точно отражается ионно-молекулярным уравнением, где формулы слабых электролитов записаны в виде молекул, а сильных – в виде ионов:
CH3COO– + Na+ + H+ + Cl– = CH3COOH + Na+ + Cl–
или в сокращенном видеСокращенное ионное уравнение отражает самую суть происходящего процесса. Вступают в реакцию или образуются в ней в действительности только те частицы (ионы или молекулы), которые записаны в сокращенном уравнении.:
CH3COO– + H+ = CH3COOH
Аналогично протекают реакции между сильными основаниями и солями слабых оснований. Например:
FeSO4 + 2 NaOH = Na2SO4 + Fe(OH)2
Fe2+ + SO42– + 2 Na+ + 2 OH– = SO42– + 2 Na+ + Fe(OH)2
Fe2+ + 2 OH– = Fe(OH)2
4.3.4 Гидролиз солей
Химическая реакция обменного характера растворяемого вещества с растворителем называется сольволизом. Если растворителем является вода, то процесс – гидролиз (частный случай сольволиза).
Суть гидролиза солей заключается в том, что происходит смещение равновесия диссоциации воды вследствие связывания одного из ее ионов с образованием малодиссоциированного или труднорастворимого продукта. Гидролиз идет по-разному в зависимости от силы кислоты и основания, образовавших соль. Рассмотрим различные случаи.
а) Соль образована слабой кислотой и сильным основанием (CH3COONa, KCN, Na2CO3).
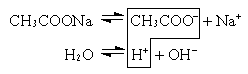
или CH3COO– + Na+ + H2O  CH3COOH + Na+ + OH–
CH3COOH + Na+ + OH–
CH3COO– + H2O  CH3COOH + OH–
CH3COOH + OH–
Так как уксусная кислота слабо диссоциирует, ацетат-ион связывает ион H+, и равновесие диссоциации воды смещается вправо согласно принципу Ле Шателье. В растворе накапливаются ионы OH– (pH>7)*.
Если соль образована многоосновной кислотой, то гидролиз идет ступенчато. Например, гидролиз карбоната:
I ступень: CO32– + H2O  HCO3– + OH–
HCO3– + OH–
II ступень: HCO3– + H2O  H2CO3 + OH–
H2CO3 + OH–
Практическое значение обычно имеет только процесс, идущий по первой ступени, которым, как правило, и ограничиваются при оценке гидролиза солей. Равновесие гидролиза по второй ступени значительно смешено влево по сравнению с равновесием первой ступени, поскольку на первой ступени образуется более слабый электролит (HCO3–), чем на второй (H2CO3) (о смещении ионных равновесий см. раздел 4.3.3).
б) Соль образована сильной кислотой и слабым основанием (NH4NO3, AlCl3, Fe2(SO4)3).
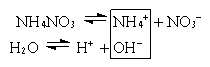
NH4+ + NO3– + H2O  NH4OH + NO3– + H+
NH4OH + NO3– + H+
NH4+ + H2O  NH4OH + H+
NH4OH + H+
(pH<7)
В случае многозарядного катиона гидролиз протекает ступенчато, например:
I ступень: Cu2+ + HOH  CuOH+ + H+
CuOH+ + H+
II ступень: CuOH+ + HOH  Cu(OH)2 + H+
Cu(OH)2 + H+
При этом концентрация ионов водорода и pH среды * в растворе также определяются главным образом первой ступенью гидролиза.
в) Соль образована слабой кислотой и слабым основанием (CH3COONH4, (NH4)2CO3).
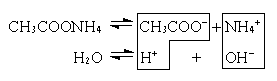
CH3COO– + NH4+ + H2O  CH3COOH + NH4OH
CH3COOH + NH4OH
В этом случае образуются два малодиссоциированных соединения, и pH раствора зависит от относительной силы кислоты и основания.
Если продукты гидролиза могут удаляться из раствора- например, в виде осадка или газообразного вещества., то гидролиз протекает до конца. Например:
Al2S3 + 3 H2O  Al(OH)3¯ + H2S
Al(OH)3¯ + H2S
г) Соли, образованные сильной кислотой и сильным основанием, гидролизу не подвергаются, т.к. единственным малодиссоциирующим соединением является H2O.
Взаимное усиление гидролиза. Допустим, что в разных сосудах установились равновесия:
CO32– + H2O  HCO3– + OH–
HCO3– + OH–
Al3+ + H2O  AlOH2+ + H+
AlOH2+ + H+
Обе соли гидролизованы незначительно, но если растворы смешать, то происходит связывание ионов H+ и OH–. В соответствии с принципом Ле-Шателье * оба равновесия смещаются вправо, и гидролиз протекает полностью:
2 AlCl3 + 3 Na2CO3 + 3 H2O = 2 Al(OH)3 + 3 CO2 + 6 NaCl
Это называется взаимным усилением гидролиза.
4.4 РЕШЕНИЕ ТИПОВЫХ ЗАДАЧ ПО ТЕМЕ “РАСТВОРЫ”
(для нехимических специальностей)
1. Какой из указанных ниже электролитов является слабым?
а) H2SO4; б) NaI; в) HCNO; г) HCl.
Решение.
Серная и соляная кислоты являются сильными (см. раздел 4.3.1), а иодид натрия представляет собой легко растворимую соль (таблица 3 приложения). Эти электролиты хорошо диссоциируют на ионы в водном растворе. Слабым, т.е. плохо диссоциирующим на ионы электролитом, является циановая кислота.
Ответ: HCNO.
2. Определите концентрацию (моль/л) ионов H+ в растворе, если pH среды равен 12,7.
Решение.
По определению pH=–lg[H+]. Поэтому [H+]=10–pH. Следовательно, в данном случае [H+]=10–12,7=2·10–13.
Ответ: 2·10–13 моль/л.
3. Определите pH среды, если концентрация ионов OH– в растворе составляет 1,8·10–9 моль/л.
Решение.
Используя ионное произведение воды, вычислим концентрацию ионов H+ в растворе:
[H+]= Kw /[OH–]=10–14/1,8·10–9=5,56·10–6 моль/л
Определим pH cреды: pH = –lg[H+] = –lg 5,56·10–6 = 5,25.
Ответ: 5,25.
4. Запишите в молекулярной и ионно-молекулярной формах уравнения реакций между веществами. В ответе укажите молярную массу образующегося слабого электролита. а) H2S + Ba(OH)2 →...; б) Pb(NO3)2 + H2SO4 →....
Решение.
а) Реакция между сероводородом и гидроксидом бария относится к типу реакций ионного обмена. Поэтому в образующихся соединениях положительно заряженный ион из одного исходного вещества соединяется с отрицательно заряженным ионом из другого. Молекулярное уравнение реакции:
H2S + Ba(OH)2 → BaS + H2O.
В ионно-молекулярном уравнении сильные электролиты должны быть записаны в виде ионов, а слабые – в виде молекул. Слабо диссоциирующими веществами в этой реакции являются сероводород и вода. Поэтому ионно-молекулярное уравнение реакции имеет вид:
H2S + Ba2+ + 2OH– → Ba2+ + S2– + 2H2O.
В сокращенном ионно-молекулярном уравнении должны быть исключены одинаковые частицы, находящиеся в левой и правой частях полного уравнения, т.е. ионы, которые не претерпевают изменений в ходе реакции. В данном случае это ионы Ba2+. Сокращенное ионно-молекулярное уравнение реакции:
H2S + 2OH– → S2– + 2H2O.
Слабым электролитом, образующимся в реакции, является H2O. Вычисляем молярную массу воды: 1+1+16=18.
Ответ: 18 г/моль.
б) Реакция между нитратом свинца и серной кислотой относится к типу реакций ионного обмена. Поэтому в образующихся соединениях положительно заряженный ион из одного исходного вещества соединяется с отрицательно заряженным ионом из другого. Молекулярное уравнение реакции:
Pb(NO3)2 + H2SO4 → 2HNO3 + PbSO4↓.
Слабо диссоциирующим веществом в этой реакции является сульфат свинца (плохо растворимая соль, выпадающая в осадок, см. таблицу 3 приложения). Поэтому ионно-молекулярное уравнение реакции имеет вид:
Pb2+ + 2NO3– + 2H+ + SO42– → 2H+ + 2NO3– + PbSO4↓.
В сокращенном ионно-молекулярном уравнении должны быть исключены одинаковые частицы, находящиеся в левой и правой частях полного уравнения, т.е. ионы, которые не претерпевают изменений в ходе реакции. В данном случае это ионы NO3– и H+. Сокращенное ионно-молекулярное уравнение реакции:
Pb2+ + SO42– → PbSO4↓.
Слабым электролитом, образующимся в реакции, является PbSO4. Вычисляем молярную массу сульфата свинца: 207+32+4·16=303.
Ответ: 303 г/моль.
5. Cоставьте ионно-молекулярные и молекулярные уравнения реакции гидролиза солей. а) K2S; б) CuCl2. В ответе укажите разность молярных масс ионов, образующихся при гидролизе.
Решение.
а) Гидролизом солей называется процесс взаимодействия ионов соли с ионами воды, приводящий к образованию слабодиссоциирующих веществ и часто сопровождающийся изменением реакции среды (рН).
При растворении в воде K2S диссоциирует: K2S 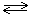 2K+ +S2-.
2K+ +S2-.
При составлении уравнений гидролиза в первую очередь необходимо определить ионы соли, связывающие ионы воды в малодиссоциирующие соединения, т.е. ионы, обусловливающие гидролиз.
В данном случае ионы S2- связывают катион H+, образуя ион HS–
S2– +H2O 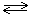 HS– +OH–
HS– +OH–
Уравнение гидролиза в молекулярной форме:
K2S+H2O 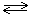 KHS+KOH
KHS+KOH
Практически гидролиз соли ограничивается первой ступенью с образованием кислой соли (в данном случае KHS). Таким образом, гидролиз соли, образованной сильным основанием и слабой кислотой (такой, как K2S) протекает по аниону соли. Избыток ионов OH– в растворе обусловливает щелочную реакцию среды в растворе (pН>7). В результате гидролиза образуются 2 иона: HS– и OH–. Рассчитываем разность их молярных масс: (1+32)–(16+1)=16.
Ответ: 16 г/моль.
б) При растворении в воде CuCl2 диссоциирует: СuCl2 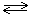 Cu2+ +2Cl–
Cu2+ +2Cl–
В данном случае ионы Cu2+ соединяются с ионами OH–, образуя гидроксоионы CuOH+. Гидролиз соли практически ограничивается первой ступенью, и образование молекулы Cu(OH)2 не происходит. Ионно-молекулярное уравнение имеет вид:
Cu2+ + HOH 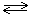 CuOH++ H+
CuOH++ H+
В данном случае продуктами гидролиза являются основная соль и кислота. Уравнение гидролиза в молекулярной форме записывается следующим образом:
CuCl2+H2O 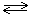 CuOHCl+ HСl
CuOHCl+ HСl
Таким образом, гидролиз соли, образованной слабым основанием и сильной кислотой (в данном случае CuCl2) протекает по катиону соли. Избыток ионов H+ в растворе обусловливает кислую реакцию среды в растворе (рН<7). В результате гидролиза образуются 2 иона: CuOH+ и H+ (cм. ионно-молекулярное уравнение). Рассчитываем разность их молярных масс: (64+16+1)–1=80.
Ответ: 80 г/моль.
 2015-05-26
2015-05-26 2649
2649