Пигментные наборы фотосинтезирующих эубактерий позволяют им использовать весь диапазон длин волн падающей на Землю солнечной энергии (рис. 71; см. рис. 35). Обращает внимание большое различие в спектрах поглощения у представителей разных групп фотосинтезирующих организмов и прежде всего существенные сдвиги в максимумах поглощения хлорофиллов в красной области спектра. Несомненно экологическое значение этого явления, позволяющего избегать конкуренции за свет между разными группами фотосинтезирующих организмов. Что же касается эволюции спектров поглощения хлорофиллов, то очевидна тенденция к перемещению в более коротковолновую часть спектра с более высоким энергетическим уровнем.
СТРОЕНИЕ ФОТОСИНТЕТИЧЕСКОГО АППАРАТА ЭУБАКТЕРИЙ
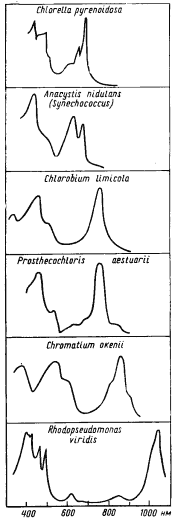 |
| Рис. 71. Спектры поглощения клеток эукариотной зеленой водоросли Chlorella pyrenoidosa и представителей разных групп фотосинтезирующих эубактерий: цианобактерии (Anacystis nidulans, Synechococcus), зеленых (Chlorobium limicola, Prosthecochloris aestuarii) и пурпурных (Chromatium okenii, Rhodopseudomonas viridis) бактерий |
Фотосинтетический аппарат основных групп эубактерий организован по-разному. Это проявляется как в химической природе составляющих его компонентов (набор пигментов, состав переносчиков электронов), так и в структурной организации в клетке. Фотосинтетический аппарат состоит из трех основных компонентов: 1) светособирающих пигментов, поглощающих энергию света и передающих ее в реакционные центры; 2) фотохимических реакционных центров, где происходит трансформация электромагнитной формы энергии в химическую; 3) фотосинтетических электронтранспортных систем, обеспечивающих перенос электронов, сопряженный с запасанием энергии в молекулах АТФ. В фотохимической реакции участвуют, как правило, хлорофиллы или бактериохлорофиллы a в модифицированной форме. Эти же виды хлорофиллов, наряду с другими, а также пигментами иных типов (фикобилипротеины, каротиноиды) выполняют функцию антенны. У некоторых пурпурных бактерий, содержащих только бактериохлорофилл b, он выполняет обе функции. У недавно описанных гелиобактерий бактериохлорофилл g также служит светособирающим пигментом и входит в состав реакционного центра (табл. 21).
Два компонента фотосинтетического аппарата — реакционные центры и электронтранспортные системы — всегда локализованы в клеточных мембранах, представленных ЦПМ и у большинства фотосинтезирующих эубактерий развитой системой внутрицитоплазматических мембран — производных ЦПМ (см. рис. 4). Локализация светособирающих пигментов в разных группах фотосинтезирующих эубактерий различна (табл. 22). У пурпурных бактерий, гелиобактерий и прохлорофит светособирающие пигменты в виде комплексов с белками интегрированы в мембраны (рис. 72, А). В клетках зеленых бактерий и цианобактерий основная масса светособирающих пигментов находится в особых структурах, прикрепленных к поверхности мембраны, но не являющихся ее компонентом. Это хлоросомы зеленых бактерий и фикобилисомы цианобактерий (см. рис. 4).
В хлоросомах зеленых бактерий содержится весь бактериохлорофилл с, d или е (в зависимости от вида), а также небольшие количества бактериохлорофилла a, служащего промежуточным звеном при переносе энергии света от основного светособирающего бактериохлорофилла к бактериохлорофиллу a, локализованному в ЦПМ. С этой формы пигмента энергия света передается на модифицированную форму бактериохлорофилла a реакционного центра. Локализованные в хлоросомах светособирающие бактериохлорофиллы организованы в виде палочковидных структур диаметром 5 — 10 нм, расположенных параллельно длинной оси хлоросомы (рис. 72, Б). Высокоупорядоченная их организация и упаковка осуществляется с помощью белковых молекул. В основании хлоросомы, примыкающем к ЦПМ, расположен слой молекул бактериохлорофилла a.
Таблица 21. Функции пигментов в фотосинтезе
| Группы фотосинтезирующих эубактерий | Светособирающие пигменты | Хлорофиллы, входящие в состав реакционного центра | ||
| хлорофиллы | фикобилипротеины | основные каротиноиды | ||
| Пурпурные бактерии | бактериохлорофилл a или b | нет | алифатические и арильные | бактериохлорофилл a или b |
| Зеленые бактерии | бактериохлорофиллы a+с, a+d, a+e | нет | арильные и алициклические | бактериохлорофилл a |
| Гелиобактерии | бактериохлорофилл g | нет | единственный алифатический: нейроспорин | бактериохлорофилл g |
| Цианобактерии | хлорофилл a | фикоцианин, аллофикоцианин, фикоэритрин | алициклические | хлорофилл a |
| Прохлорофиты | хлорофиллы a+b | нет | алициклические | хлорофилл a |
Таблица 22. Локализация фотосинтетического аппарата в клетках разных групп эубактерий
| Группы фотосинтезирующих эубактерий | Компоненты фотосинтетического аппарата | |
| светособирающие пигменты | фотохимические реакционные центры и электронтранспортные системы | |
| Пурпурные бактерии | ЦПМ и ее производные | ЦПМ и ее производные |
| Зеленые бактерии | ЦПМ и хлоросомы* | ЦПМ |
| Гелиобактерии | ЦПМ | ЦПМ |
| Цианобактерии | фикобилисомы и тилакоиды** | тилакоиды** |
| Прохлорофиты | тилакоиды | тилакоиды |
* У недавно описанной бактерии Heliolhrix oregonensis, близкой по данным анализа 5S рРНК к нитчатым зеленым бактериям, обнаружен только один вид хлорофилла — бактериохлорофилл a и отсутствуют хлоросомы; все компоненты фотосинтетического аппарата этой бактерии локализованы в ЦПМ.
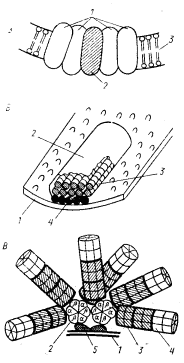 |
| Рис. 72. Структурная организация и локализация светсобирающих пигментов в разных группах фотосинтезирующих эубактерий: А — локализованные в мембране свет- собирающие комплексы пурпурных бактерий: 1 — светособирающие пигмент-белковые комплексы; 2 — реакционный центр; 3 — мембрана; Б — модель хлоросомы зеленых бактерий: 1 — ЦПМ; 2 — хлоросома; 3 — палочковидные структуры, образованные молекулами бактериохлорофилла с, d или е; 4 — слой молекул бактериохлорофилла a; В — модель типичной фикобилисомы цианобактерий: 1 — мембрана тилакоида; 2 — аллофикоцианиновое ядро; 3 — фикоцианин; 4 — фикоэритрин; 5 — белок, обеспечивающий прикрепление фикобилисомы к тилакоидной мембране |
** Исключение составляет Gloeobacter violaceus.
В группе цианобактерий обнаружены два типа структурной организации фотосинтетического аппарата. У единственного представителя этой группы — одноклеточной цианобактерии Gloeobacter violaceus — нет тилакоидных мембран и типичных для всех остальных видов фикобилисом. Единственной мембраной является ЦПМ, не образующая никаких впячиваний в цитоплазму. В ЦПМ локализованы реакционные центры и электронтранспортные системы фотосинтеза. Фикобилипротеины (фикоцианин, аллофикоцианины и фикоэритрины) в виде слоя толщиной 50 — 70 нм прилегают к внутренней поверхности ЦПМ.
Клетки всех остальных цианобактерий содержат развитую систему внутрицитоплазматических мембран — тилакоидов, к наружным поверхностям которых прикреплены регулярно расположенные дискретные гранулы — фикобилисомы. Их форма, размеры и количество на единицу поверхности мембраны могут меняться в значительных пределах, но всегда в клетках каждого вида содержатся фикобилисомы одного типа. Организация фикобилипротеинов в фикобилисомах показана на рис. 72, В. Молекулы аллофикоцианина и аллофикоцианина В составляют внутреннее ядро фикобилисомы. К нему примыкают расходящиеся в разные стороны палочковидные образования. построенные из агрегированных молекул фикоцианина и фикоэритрина, при этом фикоэритрин располагается на периферической части этих структур. У видов, у которых фикоэритрин отсутствует, палочковидные образования состоят только из фикоцианина. Такая организация фикобилисом в наилучшей степени обеспечивает перенос энергии возбуждения в направлении:

Помимо пигментов в составе фикобилисом найдены неокрашенные полипептиды, необходимые для высокоупорядоченной пространственной организации фикобилипротеинов в фикобилисоме, а также для прикрепления ее к мембране.
ФОТОФИЗИЧЕСКИЕ ПРОЦЕССЫ, ЛЕЖАЩИЕ В ОСНОВЕ ФОТОСИНТЕЗА
Известно, что энергия молекулы в основном определяется электронной энергией, а последняя, в свою очередь, зависит от расположения электронов на энергетических орбитах. Электрон, находящийся на более удаленной от ядра орбите, обладает большим запасом энергии, т. е. его энергетический уровень выше, чем у электрона, располагающегося на орбите ближе к ядру. Электроны могут переходить с одной электронной орбиты на другую, и это сопровождается потерей или поглощением извне энергии молекулой, т. е. изменением ее энергетического состояния. Подобные переходы имеют место и при поглощении или испускании молекулой кванта света. Способность вещества поглощать свет определенной длины волны зависит от его молекулярного строения и в первую очередь от расположения электронов на энергетических орбитах.
Каким требованиям должен удовлетворять свет как фактор для "возбуждения" электронов? Кванты света должны обеспечивать переходы электронов с низкоэнергетических на высокоэнергетические уровни. Это возможно в том случае, когда разница между энергетическими уровнями при переходе электрона с орбиты на орбиту равна энергии кванта света. Должны были образоваться такие вещества, в молекулах которых эти электронные переходы соответствуют энергии поглощенного кванта света. Подобным требованиям отвечают молекулы хлорофиллов и других пигментов, у которых переход электронов в возбужденное высокоэнергетическое состояние происходит под действием квантов света с длиной волны в диапазоне 300 — 1100 нм.
Рассмотрим процессы, происходящие при поглощении кванта света молекулой хлорофилла (рис. 73). В темноте молекула хлорофилла находится в стабильном невозбужденном состоянии, а ее электроны — на основном энергетическом уровне. Когда квант света попадает на молекулу хлорофилла, порция энергии этого кванта поглощается одним из электронов, который переходит на новый, более богатый энергией уровень, а молекула хлорофилла переходит при этом в возбужденное состояние. В зависимости от того, какова энергия поглощенного кванта, электрон может перейти на разные энергетические уровни: квант синего света поднимает электрон на второй синглетный уровень, квант красного света — на первый. Время жизни молекулы хлорофилла в возбужденных синглетных состояниях очень коротко (на втором синглетном уровне — 10 – 12 – 10 – 13 с, на первом — 10 – 9 — 10 – 7 с), после чего молекула возвращается в исходное стабильное состояние. Возвращение молекулы в исходное состояние возможно разными путями, и энергия, поглощенная электроном, теряется им в виде тепла, флюоресценции или фосфоресценции.
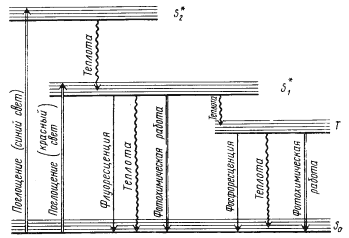 |
| Рис. 73. Схема электронных переходов между энергетическими уровнями молекулы хлорофилла при поглощении и испускании света: S0 — основной энергетический уровень S1 * и S2 * — первый и второй синглетные уровни; T — триплетный уровень (по Рубину, 1976) |
Перечисленные выше пути перехода молекулы хлорофилла из возбужденного состояния в основное не исчерпывают всех возможностей. В клетке молекулы хлорофилла в норме достаточно жестко сопряжены друг с другом, поэтому перешедшая в возбужденное состояние молекула пигмента может передавать энергию поглощенного кванта света соседней молекуле, переводя ее в возбужденное состояние. Основная масса хлорофилла и других фотосинтетических пигментов клетки представляет собой антенну, улавливающую световую энергию. Светособирающие пигменты организованы в виде комплексов, в которых они связаны с молекулами белка. Энергия возбуждения мигрирует в направлении от пигментов, поглощающих свет более коротких длин волн, к более длинноволновым формам и от последних поступает в реакционные центры. Для передачи энергии электронного возбуждения необходимо, чтобы среднее расстояние между молекулами пигментов составляло около 10Å.
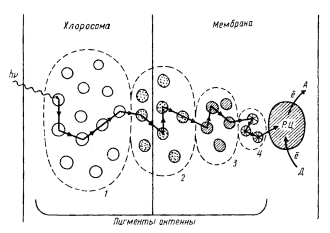 |
| Рис. 74. Миграция энергии света у зеленой бактерии Chloroflexus aurantiacus:1 — бактериохлорофилл c; 2–4 — разные формы бактериохлорофилла a; Д — первичный донор электрона; А — первичный акцептор электрона; Р. Ц. — реакционный центр |
Поглощение и миграция энергии света у зеленой бактерии Chloroflexus aurantiacus схематически изображены на рис. 74. Порция энергии, поглощенная молекулой локализованного в хлоросоме бактериохлорофилла с (максимум поглощения пигмента — 742 нм), передается на форму бактериохлорофилла a с максимумом поглощения при 792 нм. Эта форма пигмента локализована как в хлоросоме, так и в мембране. С нее через расположенные в мембране более длинноволновые формы бактериохлорофилла а (максимум поглощения 805 и 865 нм) энергия поступает на модифицированную форму бактериохлорофилла a реакционного центра, поглощающую при 865 нм. Таким образом, процесс переноса энергии электронного возбуждения у C. aurantiacus может быть представлен в виде следующей цепочки:
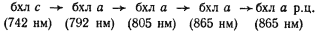
У зеленых серобактерий на один реакционный центр приходится до 2000 молекул бактериохлорофилла с, a, или e; у некоторых пурпурных бактерий — порядка 50 молекул бактериохлорофилла a.
ФОТОХИМИЧЕСКИЕ ПРОЦЕССЫ И ПУТИ ЭЛЕКТРОННОГО ТРАНСПОРТА. ФОТОФОСФОРИЛИРОВАНИЕ
В то время как основная масса фотосинтетических пигментов способна только поглощать энергию света и передавать ее соседним молекулам, небольшая часть молекул хлорофилла участвует в осуществлении фотохимической реакции, т. е. преобразовании электромагнитной энергии в химическую. Процесс этот происходит в реакционных центрах, состоящих из первичного донора электронов, первичного акцептора и одного или более вторичных акцепторов электронов. Кроме того, в составе реакционных центров обнаружены молекулы каротиноидов и полипептидов. Основные компоненты реакционных центров разных групп фотосинтезирующих эубактерий представлены в табл. 23.
При поглощении кванта света реакционным центром первичный донор электронов (Д), которым всегда является длинноволновая форма молекулы хлорофилла или бактериохлорофилла, возбуждается, переходит в новое состояние (Д*), в котором становится активным восстановителем, и переносит электрон на первичный акцептор электронов (А). Чтобы предотвратить возвращение электрона на Д+, вторичный акцептор (В) принимает электрон от первичного акцептора и стабилизирует таким способом разделение зарядов. Для дальнейшей стабилизации этого разделения вторичный донор электронов (Е), в качестве которого почти всегда выступают цитохромы типа с, отдает электрон на молекулу первичного донора (Д+). Все перечисленные этапы можно суммировать следующим образом:
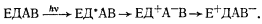
Эти реакции происходят в реакционном центре и являются "первичными" химическими реакциями фотосинтеза. Таким образом, индуцированные светом перемещения электрона в реакционном центре в конечном итоге приводят к переносу его на вторичный акцептор с отрицательным потенциалом.
Таблица 23. Реакционные центры эубактерий
| Группы фотосинтезирующих эубактерий | Состав реакционных центров | |||
| первичный донор электронов | первичный акцептор электронов | вторичный акцептор электронов | ||
| Пурпурные серные и несерные бактерии | бхл а (П870) бхл b (П960) | б/феоф а б/феоф b | УХ MX | |
| Зеленые бактерии | нитчатые | бхл a (П865) | б/феоф a | MX |
| серные | бхл a (П840) | бхл с (П663) | FeS | |
| Гелиобактерии | бхл g (П798) | бхл g (П670) | FeS Х-подобное соединение | |
| Цианобактерии | I ФС | хл а (П700) | хл а | FeS |
| II ФС | хл a (П680) | феоф a | ПХ | |
| Прохлорофиты | I ФС | хл а (П700) | ? | ? |
| II ФС | хл a (П680) | ? | ? |
ФС — фотосистема; бхл — бактериохлорофилл; хл — хлорофилл; б/феоф — бактериофеофитин; феоф — феофитин; П — фотохимически активные формы хлорофилла с указанием длины волны, при которой происходит индуцированное светом изменение поглощения пигмента; Х — хинон; УХ — убихинон; MX — менахинон; ПХ — пластохинон; FeS — железосероцентры;? — информация отсутствует.
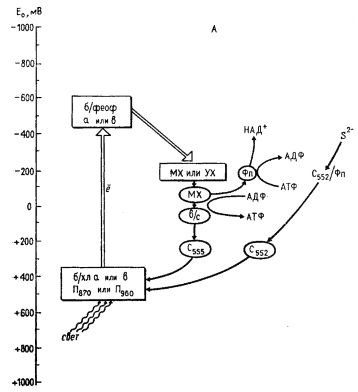 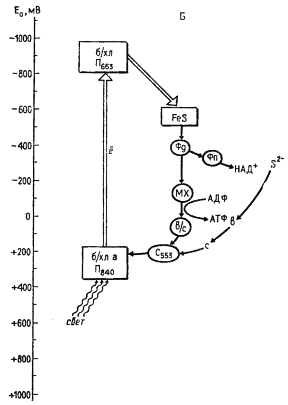 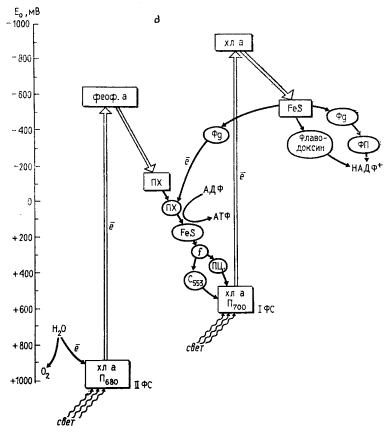 |
| Рис. 75. Организация фотосинтетического аппарата разных групп эубактерий: А — пурпурные бактерии; Б — зеленые серобактерии; В — цианобактерии. Хл — хлорофилл; б/хл — бактериохлорофилл; феоф — феофитин; б/феоф — бактериофитин; ФС — фотосистема; FeS — железосеросодержащий белок; Фд — ферредоксин; Фп — флавопротеин; ПХ — пластохинон; MX — менахинон; УХ — убихинон; ПЦ — пластоцианин; b, с, f — цитохромы. Прямоугольниками обведены компоненты реакционного центра, овалом — компоненты электронного транспорта, связанные с мембраной. Двойной стрелкой обозначены перемещения электрона в реакционном центре |
Что происходит после того, как вторичный акцептор захватывает электрон? В фотосинтетической мембране в непосредственной близости от реакционного центра локализованы определенным образом ориентированные переносчики электронов, и по этим переносчикам электрон может возвращаться на "свое" место в молекуле хлорофилла. Последним переносчиком, с которого электроны поступают на хлорофилл реакционного центра, у фотосинтезирующих организмов в большинстве случаев служат цитохромы типа с. Возвращение электрона — темновой процесс. Электрон перемещается по цепи переносчиков в соответствии с электрохимическим градиентом. Имеет место циклический транспорт электронов.
Циклическим электронным транспортом у фотосинтезирующих эубактерий не исчерпываются все возможные пути переноса электронов. Электрон, "оторванный" от первичного донора реакционного центра, может по цепи, состоящей из других переносчиков, не возвращаться к молекуле хлорофилла, а передаваться на такие клеточные метаболиты, как НАД(Ф)+ или окисленный ферредоксин, которые используются в реакциях, требующих восстановителя. Таким образом, электрон, покинувший молекулу хлорофилла, выводится из "системы". Возникает однонаправленный незамкнутый электронный поток, получивший название нециклического пути переноса электронов. У пурпурных и зеленых нитчатых бактерий функционирует только циклический светозависимый поток электронов. У остальных групп эубактерий фотоиндуцируется как циклический, так и нециклический перенос электронов, при этом у зеленых серобактерий и гелиобактерий оба пути электронного транспорта связаны с функционированием одной фотосистемы, а у цианобактерий и прохлорофит циклический перенос электронов зависит от активности I фотосистемы, а для нециклического потока электронов необходимо функционирование обеих фотосистем. Поток электронов по цепи переносчиков на определенных этапах сопряжен с направленным перемещением протонов через мембрану, что приводит к созданию протонного градиента, используемого для синтеза АТФ.
Фосфорилирование, сопряженное с циклическим потоком электронов, получило название циклического фотофосфорилирования. Соответственно, нециклическим фотофосфорилированием называют синтез АТФ, сопряженный с нециклическим электронным транспортом.
ОБРАЗОВАНИЕ ВОССТАНОВИТЕЛЯ ПРИ ФОТОСИНТЕЗЕ
Для протекания процессов биосинтетической природы необходима не только энергия в форме АТФ, но и восстановитель.
Особенно четко потребность в восстановителе проявляется, если основным или единственным источником углерода для конструктивных процессов служит CO2 — предельно окисленное углеродное соединение. Для превращения углекислоты в структурные компоненты клетки и клеточные метаболиты необходимо ее восстановление до уровня углеводов, белков, липидов. Это же справедливо и при использовании в качестве источника углерода органических соединений, более окисленных, чем вещества тела, например ацетата.
При циклическом электронном транспорте восстановитель как конечный продукт фотоиндуцированного процесса не образуется, поскольку электрон, покинувший молекулу хлорофилла, в конечном итоге вновь возвращается к ней. Образование восстановителя возможно только на путях нециклического переноса электронов.
Отсутствие у пурпурных и зеленых нитчатых бактерий светозависимого восстановления НАД+ или ферредоксина связано с тем, что электроны, отрывающиеся от молекулы хлорофилла, в результате фотохимической реакции акцептируются на хиноновых соединениях, окислительно-восстановительный потенциал которых недостаточно отрицателен для непосредственного восстановления НАД+ или ферредоксина (см. табл. 11). В этих группах фотосинтезирующих эубактерий восстановитель образуется в результате темнового переноса электронов от экзогенных доноров (сульфид, тиосульфат, органические соединения) против электрохимического градиента — обратного переноса электронов (рис. 75, А). Последний осуществляется с участием электронтранспортной цепи, в состав которой входят флавопротеины, за счет энергии, генерируемой в процессе циклического электронного транспорта.
У зеленых серобактерий и гелиобактерий в реакционных центрах под действием поглощенного кванта света "подъем" электронов осуществляется до уровня порядка — 500 мВ, что делает возможным прямое восстановление НАД+ или ферредоксина путем переноса электронов со вторичного акцептора на эти соединения, т. е. восстановитель образуется в фотохимической реакции. Таким образом, в этих группах фотосинтезирующих эубактерий в результате фотохимической реакции одного типа индуцируется как циклический транспорт электронов, приводящий к образованию АТФ, так и нециклический, при котором возникает восстановитель (рис. 75, Б).
У цианобактерий и прохлорофит в результате двух фотохимических реакций электроны поднимаются до уровня приблизительно — 500 мВ, что делает возможным их прямой перенос на молекулы ферредоксина и НАДФ+ (рис. 75, В). В группах эубактерий, осуществляющих кислородный фотосинтез, фотоиндуцируются два потока электронов: циклический и нециклический. Циклический перенос электронов, связанный с активностью I фотосистемы, приводит к получению только энергии. При нециклическом электронном транспорте, обеспечиваемом активностью двух последовательно функционирующих фотохимических реакций, на конечном этапе электронного переноса образуется восстановитель, а на отрезке электронтранспортной цепи между двумя фотосистемами, где электроны переносятся по электрохимическому градиенту, имеет место запасание энергии в молекулах АТФ.
ЭКЗОГЕННЫЕ ДОНОРЫ ЭЛЕКТРОНОВ В БЕСКИСЛОРОДНОМ ФОТОСИНТЕЗЕ
Нециклический транспорт электронов приводит к тому, что электрон, "оторвавшийся" от молекулы хлорофилла, не возвращается к ней, а переходит на другие переносчики, с которых потом используется в системе реакций восстановительной природы. В результате в молекуле хлорофилла возникает электронная "вакансия", которую необходимо заполнить, чтобы молекула пигмента могла функционировать. Для этой цели сформировался поток электронов, донорами которых являются легко окисляемые экзогенные вещества.
В качестве веществ — экзогенных доноров электронов — используются как органические, так и неорганические соединения. В последнем случае это в основном различные восстановленные соединения серы (H2S, сульфит, молекулярная сера, тиосульфат, тетратионат, тиогликолят), а также молекулярный водород.
Что представляют собой сформировавшиеся у эубактерий, осуществляющих бескислородный фотосинтез, пути переноса электронов от экзогенных доноров? Окислительно-восстановительные потенциалы органических и неорганических соединений, используемых в качестве экзогенных доноров электронов, таковы, что эти соединения не могут осуществлять темновое восстановление НАД+. В то же время они достаточно отрицательны, чтобы обеспечить донирование электронов на молекулы бактериохлорофилла реакционного центра55.
55 Исключение составляет молекулярный водород, окислительно-восстановительный потенциал которого (— 420 мВ) достаточен для темнового восстановления НАД+.
У пурпурных и зеленых нитчатых бактерий, у которых функционирует только светозависимый циклический электронный транспорт, нет надобности в заполнении электронной "вакансии" в молекуле хлорофилла. В то же время проблема получения фотохимическим путем восстановителя не решена.
Конкретные пути, ведущие к получению восстановленного НАД или ферредоксина, зависят от окислительно-восстановительного потенциала экзогенных доноров электронов. При окислении сукцината, например, электроны прямо поступают на хиноновые соединения и от них с помощью энергозависимого обратного электронного транспорта на НАД+ и ферредоксин. При окислении восстановленных соединений серы, потенциал которых недостаточно отрицателен для восстановления хинонов, электроны поступают на них не прямо, а через реакционные центры (см. рис. 75, А). В их переносе до реакционного центра участвуют растворимые и связанные с мембраной флавопротеины и цитохромы.
Функционирование фотохимического пути образования восстановителя у зеленых серобактерий и гелиобактерий ставит их перед проблемой заполнения возникающих электронных "вакансий" в молекулах бактериохлорофилла реакционного центра. Это достигается путем переноса электронов по электрохимическому градиенту от экзогенного донора к молекулам пигмента. В переносе участвуют растворимые и связанные с мембраной цитохромы типа b и с (см. рис. 75, Б). Таким образом, на определенном этапе эволюции эубактерий сформировался способ получения энергии, в основе которого лежит использование энергии света, и для функционирования этого пути необходимы определенные экзогенные вещества.
Можно только предполагать, как складывались механизмы для более эффективного использования этого вида энергии. На первых этапах, когда в окружающей среде содержалось достаточное количество восстановленных органических соединений, свет, вероятно, использовался в качестве дополнительного к субстратному фосфорилированию источника энергии. Чтобы осуществить эту функцию, необходимо трансформировать энергию света в химическую энергию в форме АТФ. Для этого достаточно было сформирования фотоиндуцированного циклического электронного транспорта, приводящего только к синтезу АТФ. Потребность в восстановителе обеспечивалась за счет органических соединений, содержавшихся во внешней среде.
Постепенное уменьшение содержания в среде восстановленных органических субстратов привело существовавшие тогда фототрофные организмы к необходимости расширить круг используемых источников углерода. Они приобрели способность усваивать в качестве такого источника углекислоту. Возникновение этой способности остро поставило вопрос об источнике электронов, необходимых для восстановления углекислоты до уровня восстановленности углеродсодержащих соединений клетки. Световая энергия стала использоваться не только для получения АТФ, но и для образования восстановителя, т. е. сформировался нециклический путь переноса электронов. Отток электронов на конструктивные процессы необходимо было компенсировать притоком электронов, способных заполнить электронную "вакансию" в молекуле хлорофилла.
Происходил постоянный поиск в окружающей среде соединений, которые могли бы выполнять функцию экзогенных доноров электронов. Определенным шагом вперед была большая независимость от органических соединений внешней среды, выразившаяся в способности использовать в качестве экзогенных доноров электронов восстановленные соединения серы.
ВОЗНИКНОВЕНИЕ ВТОРОЙ ФОТОСИСТЕМЫ
Выбор в качестве экзогенных доноров электронов восстановленных соединений серы обусловил определенную привязанность возникших фототрофных эубактерий к местам обитания, где эти соединения имеются. Колоссальное преимущество форм, которые сохранив положительные моменты сформированного фотосинтетического аппарата, могли бы в качестве экзогенного донора электронов использовать повсеместно распространенное вещество, очевидно. Таким веществом является вода. Поэтому следующий принципиально важный шаг на пути эволюции фотосинтеза и фотосинтезирующих организмов — способность использовать воду в качестве донора электронов.
Однако окислительно-восстановительный потенциал системы вода — молекулярный кислород равен+ 820 мВ, из чего следует, что электронная "вакансия", возникающая, например, в молекуле бактериохлорофилла реакционного центра зеленых серобактерий при нециклическом транспорте электронов, не может быть заполнена электроном воды (фотоокисленная форма бактериохлорофилла реакционного центра зеленых серобактерий — пигмента П840 — имеет окислительно- восстановительный потенциал порядка +250 мВ). Чтобы использование электронов воды стало возможным, необходимо, во- первых, их "оторвать" от молекулы H2O, термодинамически очень невыгодного донора электронов, и, во- вторых, "поднять" на более высокий энергетический уровень, позволяющий включаться в фотосистему, описанную выше. Природа решила эти проблемы путем создания дополнительной пигментной системы, обозначаемой как фотосистема II.
Известны две группы эубактерий, у которых фотосистема II уже сформировалась, и процесс фотосинтеза функционирует на качественно ином уровне. Это цианобактерии и прохлорофиты. Формирование II фотосистемы у них связано с появлением новых фоторецепторов и образованием новых типов фотохимических реакционных центров. Возник новый вид хлорофилла — хлорофилл а, функционирующий как светособирающий пигмент и в модифицированных формах входящий в состав реакционных центров: II фотосистемы — П680, I фотосистемы — П700. Возникли и новые пигменты антенны: фикобилипротеины и хлорофилл b.
Обнаружено, что в фотоокисленном состоянии хлорофилл a реакционного центра II фотосистемы имеет окислительно-восстановительный потенциал порядка +1000...+1300 мВ, т. е. настолько положительный, что может быть восстановлен за счет электронов воды. Механизм реакций, связанных с переносом электронов от молекул воды на П680, неизвестен. Установлено, что необходимым компонентом системы разложения воды является марганец. Очевидно также, что путь электронов от воды до П680 включает больше, чем один этап. Таким образом, фотосистема II была достроена к фотосистеме I для того, чтобы стало возможным использование воды в качестве донора электронов. Побочный продукт этого процесса — молекулярный кислород. Фотосинтез, осуществляемый при координированном функционировании двух фотосистем и сопровождающийся выделением O2 из воды, стал одним из основных типов энергетического метаболизма у высших форм жизни и занимает доминирующее положение в энергетической системе живого мира.
Общая схема фотосинтеза цианобактерии представляет собой определенную серию реакций, включающую две последовательно действующие фотореакции (рис. 75, В). Свет, поглощаемый фоторецепторами II фотосистемы — фикобилипротеинами, хлорофиллом a, каротиноидами, — передается на хлорофилл реакционного центра. Поглощение кванта света этим пигментом приводит к отрыву от него электрона и акцептированию молекулой особой формы пластохинона. Окисленная молекула Лево восстанавливается за счет электронов воды, подвергающейся фотоокислению в реакционных центрах фотосистемы II:
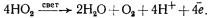
Электрон от акцептора II фотосистемы проходит через цепь переносчиков и поступает в реакционный центр I фотосистемы, на фотоокисленную форму хлорофилла a — пигмент П700 (E 0 ~+500 мВ), заполняя электронную "вакансию" аналогично тому, как это происходит при фотосинтезе зеленых серобактерий. Перенос электронов от акцептора электронов II фотосистемы до реакционного центра I фотосистемы — темновой процесс, состоящий из серии этапов, в которых участвуют переносчики с понижающимися восстановительными потенциалами, такие как цитохромы разного типа, пластоцианин (медьсодержащий белок), пластохинон. Электронный транспорт на этом участке на определенных этапах сопровождается ориентированным поперек мембраны переносом протонов и, следовательно, генерированием H+, разрядка которого с помощью протонной АТФ-синтазы приводит к синтезу АТФ.
Поглощение еще одного кванта света молекулой хлорофилла реакционного центра I фотосистемы (П700) приводит к отрыву от нее электрона, перемещающегося против электрохимического градиента, и акцептированию его молекулой FeS-белка, функционирующего у цианобактерии в качестве вторичного акцептора электронов I фотосистемы. От FeS-центра электрон проходит через цепь переносчиков (ферредоксин, флавопротеин) и акцептируется молекулой НАДФ+56. Восстановленные молекулы НАДФ далее используются как доноры электронов в различных биосинтетических процессах и в первую очередь для восстановления CO2.
56 У цианобактерии два этапа электронного транспорта могут осуществляться с помощью разных переносчиков: от цитохрома f до П700 с помощью пластоцианина или при недостатке меди с помощью цитохрома c553; от FeS до НАДФ+ с участием ферредоксина и флавопротеина или при недостатке железа в среде с участием специфического флавопротеина — флаводоксина.
Итогом двух фотохимических реакций является создание "ассимиляционной силы" — НАДФ-H2 и АТФ. Конечные продукты фотосинтеза в этом случае в принципе аналогичны продуктам, образующимся при бескислородном фотосинтезе, за исключением того, что в последнем случае восстановитель находится в форме НАД-H2.
I фотосистема цианобактерий и прохлорофит (как и эубактерий, имеющих только одну фотосистему) фотоиндуцирует также циклический перенос электронов (рис. 75, В), обеспечивающий клетку энергией. В циклическом потоке электроны, акцептированные FeS-белком, через цепь переносчиков вновь возвращаются к месту своего старта и заполняют электронную "вакансию" в молекуле П700. Циклический электронный транспорт сопровождается генерированием протонного градиента и синтезом АТФ.
Для восстановления 1 молекулы CO2 у фототрофов, имеющих две фотосистемы, необходима энергия 8 — 10 квантов поглощенного света. Эта величина складывается из следующих значений. Перенос одного электрона от воды на НАДФ+ требует 2 квантов света. Восстановление молекулы НАДФ+ происходит с использованием 2 электронов, т. е. 4 квантов света. Для ассимиляции 1 молекулы CO2 в восстановительном пентозо-фосфатном цикле необходимы 2 молекулы НАДФ-H2, т. е. 8 квантов света. Кроме восстановителя в процессе ассимиляции CO2 используется энергия в виде АТФ. В нециклическом электронном транспорте наряду с НАДФ-H2 при переносе 2 электронов синтезируются предположительно 2 — 3 молекулы АТФ. Ассимиляция 1 молекулы CO2 в восстановительном пентозофосфатном цикле требует 3 молекул АТФ.
Таким образом, нециклическая электронтранспортная система способна или целиком обеспечивать ассимиляцию CO2 в восстановительном пентозофосфатном цикле энергией, или для этого нужны дополнительные молекулы АТФ. Последние могут быть получены в циклическом процессе при затрате дополнительных квантов света.
Определение квантового расхода при восстановлении CO2 у эубактерий с одной фотосистемой обнаружило такую же величину. Поскольку у этих бактерий только одна фотосистема, для активирования электрона необходим 1 квант света. Поэтому восстановление молекулы НАД+ требует только 2 квантов света и, следовательно, общий квантовый расход для ассимиляции CO2 у эубактерий с одной фотосистемой должен быть значительно ниже, чем у организмов с двумя фотосистемами. Чтобы объяснить экспериментально полученные данные, высказываются следующие предположения. У пурпурных и зеленых нитчатых бактерий, у которых фотоиндуцируется только циклический транспорт электронов, квантовый расход отражает величину световой энергии, затрачиваемой на осуществление обратного транспорта электронов, приводящего к восстановлению НАД+, а также на ассимиляцию CO2. У зеленых серобактерий и гелио-бактерий фотоиндуцируемый нециклический перенос электронов (в отличие от фототрофов с двумя фотосистемами) не связан с получением клеточной энергии. Энергия вырабатывается только в процессе циклического переноса электронов, при этом система циклического фотофосфорилирования включает 2 генератора H+.
ПУТИ ИСПОЛЬЗОВАНИЯ СO2 ФОТОСИНТЕЗИРУЮЩИМИ ЭУБАКТЕРИЯМИ
Согласно распространенным представлениям наиболее древние формы жизни, источником энергии для которых служили реакции субстратного фосфорилирования, использовали органические соединения внешней среды одновременно по двум каналам: в качестве источника энергии и источника углерода. Постепенное исчерпание таких соединений из окружающей среды поставило организмы перед двумя проблемами: поиском новых источников энергии и новых источников углерода. В первом случае это привело к использованию энергии света, во втором — к использованию углекислоты.
Как предельно окисленное соединение CO2 не может служить источником энергии, эта же ее особенность делает углекислоту и "дорогостоящим" источником углерода. И только обеднение среды восстановленными углеродными соединениями на начальном этапе развития жизни поставило организмы перед необходимостью использовать углекислоту в качестве источника углерода ценой больших энергетических затрат, т. е. сформировать механизмы автотрофной фиксации CO2 и выработать способность синтезировать все углеродные соединения из углерода углекислоты. Однако было бы неверным считать, что до этого углекислота была инертным соединением и никак не вовлекалась в метаболизм анаэробных хемогетеротрофов. Наоборот, углекислота весьма активно использовалась в конструктивном и энергетическом метаболизме разных групп первично анаэробных хемогетеротрофов.
Все гетеротрофные организмы (низшие и высшие) с помощью определенных ферментативных реакций активно включают углекислоту в метаболизм, при этом у прокариот пути использования CO2 намного многообразнее, чем у эукариот57. Углекислота у прокариот активно используется по путям как конструктивного, так и энергетического метаболизма. В конструктивном метаболизме она выполняет две основные функции: присоединение углекислоты в качестве C1-группы к молекуле клеточного метаболита приводит к удлинению ее углеродного скелета; кроме того, при этом происходит регулирование общего уровня окисленности- восстановленности клеточных метаболитов, поскольку включение CO2-группы в молекулу приводит к заметному повышению степени ее окисленности. В этом случае CO2 входит в состав веществ клетки.
57 Предположение о том, что использование CO2 является, вероятно, общим свойством всех организмов, было высказано еще в 1908 г. А. Ф. Лебедевым. Впервые фиксацию CO2 наблюдали в 1936 г. у пропионовых бактерий X. Вуд и К. Веркман.
Свойство предельной окисленности молекулы CO2 используется в энергетическом метаболизме ряда анаэробных эубактерий, получающих энергию в процессе брожения, где CO2 служит для удаления избытка восстановителя, т. е. как конечный акцептор электронов. Эта же особенность молекулы CO2 находит применение и в энергетическом метаболизме некоторых анаэробных эубактерий (ацетогены) и архебактерий (метаногены), но у них электроны на CO2 поступают через цепь связанных с мембраной переносчиков электронного транспорта. CO2, участвующая в реакциях энергетического метаболизма, не включается в вещества клетки, а продукты ее восстановления (в виде молекул формиата, ацетата, метана) накапливаются в среде. В наибольшей степени способность вовлекать CO2 в метаболизм среди первично анаэробных хемогетеротрофных эубактерий проявляется в группе клостридиев.
Основным путем включения CO2 в вещества клетки у хемогетеротрофных прокариот служат реакции карбоксилирования. Обнаружено несколько десятков таких реакций, некоторые из них приведены в табл. 24.
Можно полагать, что к тому времени, когда возникла необходимость шире использовать CO2 как источник углерода для построения веществ клетки, уже были сформированы различные ферментативные реакции включения CO2 в хемогетеротрофный метаболизм. Обращает на себя внимание, что акцепторами углекислоты служили органические кислоты, используемые в большинстве случаев в активированной форме. Поэтому основа для перехода к более интенсивному использованию CO2 в конструктивном метаболизме, приведшая в конечном итоге к автотрофии, была заложена в недрах хемогетеротрофного метаболизма.
Некоторые анаэробные прокариоты, относящиеся к эу- и архебактериям, — хемоавтотрофы. Фиксация CO2 у них происходит по ацетил-КоА-пути, не замкнутому в цикл (см. рис. 62). Образующийся ацетил-КоА служит акцептором третьей молекулы CO2, что приводит к синтезу пировиноградной кислоты (см. табл. 24). Возможно, этот путь фиксации CO2 — первая примитивная форма автотрофии. Кажется вполне вероятным, что дальнейшие поиски путей автотрофного метаболизма проходили параллельно с формированием аппарата для использования энергии света, поскольку на первом этапе эволюции энергетические и конструктивные процессы зависели от одних и тех же источников и, следовательно, организмы одновременно были поставлены перед проблемой поиска новых источников энергии и углерода.
Таблица 24. Включение CO2 в клеточные метаболиты у хемогетеротрофов
| Фермент | Катализируемая реакция |
| Пируваткарбоксилаза | пировиноградная кислота + CO2 + АТФ ЩУК + АДФ +ФН |
| ФЕП-карбоксикиназа | ФЕП + CO2 + АДФ ЩУК + АТФ |
| ФЕП-карбоксилаза | ФЕП + CO2 ЩУК + ФН |
| ФЕП-карбокситрансфосфорилаза | ФЕП + CO2+ ФН ЩУК + ФФН |
| Малатдегидрогеназа | пировиноградная кислота + CO2 НАДФ-H2 яблочная кислота + HAДФ+ |
| Изоцитратдегидрогеназа | -кетоглутаровая кислота + CO2 + НАД(Ф)-H2 изолимонная кислота + НАД(Ф)+ |
| Пируватсинтаза | ацетил-КоА + CO2 + Фдвосст пировиноградная кислота + Фдок + КоА-SH |
| -Кетобутиратсинтаза | пропионил-КоА + CO2+ Фдвосст -кетобутират + Фдок + КоА-SH |
| -Кетоглутаратсинтаза | сукцинил-КоА + CO2 + Фдвосст -кетоглутарат + Фдок + KoA-SH |
| Пропионил-КоА-карбоксилаза | пропионил-КоА + CO2 + АТФ метилмалонил-КоА + АДФ + ФН |
| Ацетил-КоА-карбоксилаза | ацетил-КоА + CO2 + АТФ малонил-КоА + АДФ + ФН |
 2015-06-16
2015-06-16 2299
2299








