Взаимодействие между молекулами и ионами растворяемого вещества и молекулами растворителя (сольватация) имеет сложный характер и состоит из нескольких стадий, которые протекают одновременно или последовательно: молекулярная диссоциация, образование сольватов, ионизация и электролитическая диссоциация. В зависимости от типа растворяющихся веществ число стадий может изменяться.
В случае растворов неэлектролитов процесс сольватации останавливается на стадии образования сольватированной молекулы:
АВ + (n+m)S «AB(n+m)S,
где (n+m)S – (n+m) молекул растворителя S.
Поэтому в растворе отсутствуют ионы, и раствор не обладает ионной проводимостью.
Если образующийся сольват диссоциирует на сольватированные ионы:
AB(n+m)S «Ар+nS + Bq-mS,
то в растворе протекает электролитическая диссоциация и система относится к растворам электролитов.
Примеры:

Поскольку в результате электролитической диссоциации в растворах электролитов увеличивается число частиц, то наблюдается отклонение от законов Рауля и Вант – Гоффа, поэтому Вант – Гофф ввел в уравнения этих законов изотонический коэффициент:
Dр = i × р0 × х, DТкип = i × Кэ × Сm, DТзам = i × Кк × Сm, 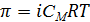 ,
,
Некоторые электролиты диссоциируют неполностью. Степень диссоциации – количественная характеристика электролитической диссоциации, показывает какая доля молекул подверглась электролитической диссоциации
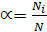 ,
,
Где Ni – число молекул растворенного вещества, распавшихся на ионы,
N – общее число молекул растворенного вещества
Степень диссоциации определяет силу электролита.
Если a < 2 %, то электролит слабый.
Если 2% < a < 30%, то электролит средней силы.
Если a > 30 %, то сильный электролит.
- многие минеральные кислоты: HCl, HBr, HI, HNO3, H2SO4, HClO4, HClO3, HMnO4;
- основания щелочных и щелочноземельных металлов;
- почти все растворимые соли (исключения: HgCl2, CdCl2, CdI2, Fe(CNS)3 и некоторые другие);
Слабые электролиты:
- некоторые минеральные кислоты: H2CO3, H2S, H2SO3, HNO2, HClO;
- H2O;
- NH4OH, основания большинства металлов (кроме щелочных и щелочно-земельных).
Ортофосфорная кислота H3PO4 – электролит средней силы.
В растворах слабых электролитов часть молекул распадается на ионы, т.е. диссоциируют, а часть остается в неизменном виде, поэтому устанавливается динамическое равновесие, которое характеризуется константой равновесия
KtAn + (n+m)H2O «Kt+ nH2O + An- mH2O
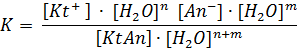
Если в выражении константы равновесия сократить числитель и знаменатель на один и тот же множитель – (H2O)n+m, то мы получим выражение константы диссоциации данного электролита:
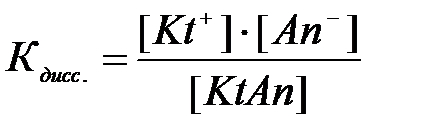
Из данного выражения следует, что Кдисс. будет иметь тем меньшее значение, чем меньше ионов в растворе, т.е. чем слабее электролит.
Константа диссоциации зависит от природы электролита, от природы растворителя, от температуры и не зависит от концентрации, поэтому является более общей характеристикой, чем степень диссоциации. Константа и степень диссоциации связаны между собой законом разбавления Оствальда:
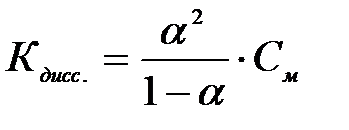
где См – молярная концентрация электролита
Если a<<1, то 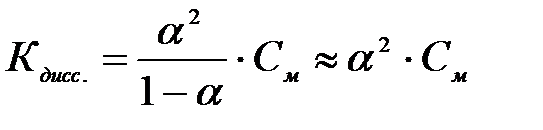
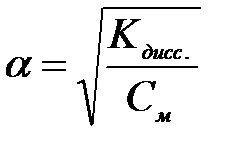
Кроме того, степень диссоциации связана с изотоническим коэффициентом:
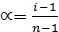 ,
,
где a - степень диссоциации, n – число ионов, образовавшихся при диссоциации электролита (на одну формульную единицу).
Например, для хлорида марганца
MnCl2 «Mn2+ + 2Cl-
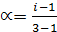 .
.
В растворах слабых электролитов взаимодействие ионов друг с другом относительно невелико из – за их незначительной концентрации. Сильные электролиты в растворах диссоциированы практически полностью
NaCl ® Na+ + Cl-
Поэтому концентрация ионов велика, причем возможно взаимодействие ионов как друг с другом, так и с полярными молекулами растворителя. В связи с этим возникает эффект уменьшения числа ионов, участвующих в реакции. Для учета сил межионного и ион – дипольного взаимодействия вместо концентрации используют активность вещества
 а = f × Cм,
а = f × Cм,
где f – коэффициент активности, выражает отклонение раствора с концентрацией См от поведения очень разбавленного раствора, в котором отсутствует межионное взаимодействие.
Количественной характеристикой межионных электростатитических взаимодействий является ионная сила (I):
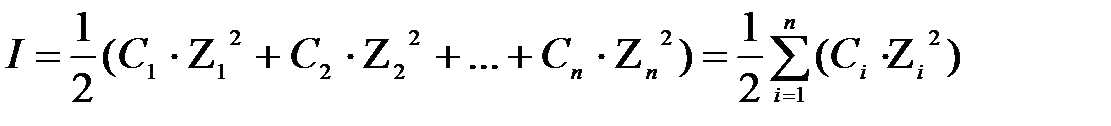
где С1, С2, Сn, Ci – коэффициент ионов;
Z1, Z2, Zn, Zi – заряды ионов.
Для растворов, концентрация которых С £ 10-2 моль/л, можно учесть взаимодействие ионов, используя коэффициент активности f, который зависит от ионной силы раствора I:
При I £ 0,01 моль/л (строго)
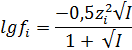
При I > 0,01 моль/л (приближенно)
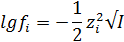
Для более концентрированных растворов необходимо использовать значения коэффициентов активности ионов, приведенные в справочных таблицах.
Коэффициент активности, следовательно, и активность ионов будет тем меньше, чем больше ионная сила раствора.
 2015-08-13
2015-08-13 831
831








