Пример 1. По табличным данным о значении вязкости анилина при разных температурах нужно найти энергию активации вязкого течения анилина.
Решение. Вязкость чистого вещества (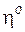 ) зависит от температуры по уравнению Френкеля
) зависит от температуры по уравнению Френкеля
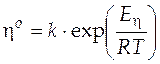 , (2.3)
, (2.3)
где 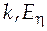 − константы, характерные для каждого индивидуального вещества;
− константы, характерные для каждого индивидуального вещества; 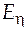 называется энергией активации вязкого течения.
называется энергией активации вязкого течения.
Если уравнение (2.3) прологарифмировать 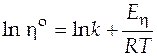 , то получим линейную зависимость
, то получим линейную зависимость 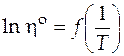 с угловым коэффициентом
с угловым коэффициентом 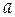 , равным
, равным 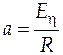 . Расположение экспериментальных точек вдоль прямой линии говорит о соответствии эксперимента данному уравнению. Составим таблицу, включающую справочные данные и расчетные данные (пересчитанные из справочных для получения линейности зависимости).
. Расположение экспериментальных точек вдоль прямой линии говорит о соответствии эксперимента данному уравнению. Составим таблицу, включающую справочные данные и расчетные данные (пересчитанные из справочных для получения линейности зависимости).
Первая и вторая строки табл. 2.1 – это справочные данные, а третья и четвертая строки − это результат вычислений, произведенных по справочным данным, для получения линейной зависимости свойств.
Таблица 2.1
Справочные и расчетные данные для решения задачи
| Величина | Температура, К | ||||
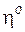 , Па∙с , Па∙с | 10,2×10 −3 | 6,16×10 −3 | 4,40×10 −3 | 3,20×10 −3 | 2,35×10 −3 |
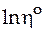 | −4,59 | −5,09 | −5,43 | −5,74 | −6,05 |
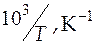 | 3,66 | 3,53 | 3,41 | 3,30 | 3,19 |
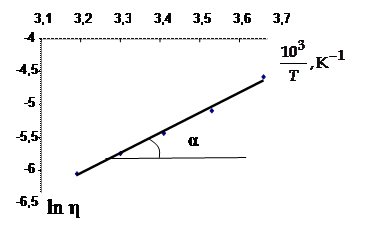 По данным табл. 2.1 построим графическую зависимость
По данным табл. 2.1 построим графическую зависимость 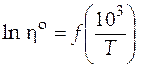 .
.
Рис. 2.1. Зависимость
натурального логарифма
вязкости от обратной
температуры для анилина
Чтобы найти угловой коэффициент, нужно взять на прямой две достаточно удаленные друг от друга точки и определить их координаты. Затем, помня, что угловой коэффициент численно равен тангенсу угла наклона прямой, вычислить его по формуле (пример рассматриваемой задачи)
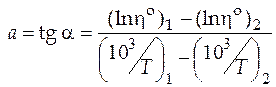 . (2.5)
. (2.5)
В нашем примере угловой коэффициент равен
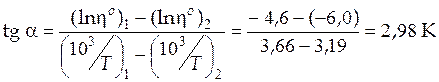 .
.
Вычислим энергию активации вязкого течения
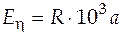 = 8,314 ×103 × 2,98 = 24776 Дж/моль = 24,78 кДж/моль.
= 8,314 ×103 × 2,98 = 24776 Дж/моль = 24,78 кДж/моль.
Рекомендации по построению графических зависимостей
1. Часто при построении графиков более удобно использовать не величину 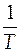 , т.к. значения получаются довольно маленькими, а величину
, т.к. значения получаются довольно маленькими, а величину 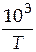 . В таком случае в уравнении (2.4), например, нужно учесть то, что при использовании множителя 103 мы увеличили одно из слагаемых, и чтобы уравнение оставалось правильным, мы запишем его следующим образом:
. В таком случае в уравнении (2.4), например, нужно учесть то, что при использовании множителя 103 мы увеличили одно из слагаемых, и чтобы уравнение оставалось правильным, мы запишем его следующим образом:
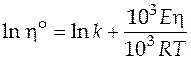 .
.
Тогда графически строим зависимость 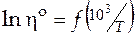 , а энергия активации будет равна
, а энергия активации будет равна 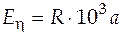 .
.
2. Значения вязкости чистых веществ можно найти во многих справочниках по химии. Ниже приведен фрагмент такой таблицы.
Вязкость чистых веществ при разных температурах
| Вещество | 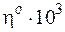 , Па×с, при температуре, К , Па×с, при температуре, К | |||
| Анилин | 10,20 | 6,16 | 4,40 | 3,20 |
Очевидно, что для удобства записи, повторяющийся множитель в значениях вязкости (10−3) был вынесен и записан вместе с 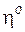 .
.
Чтобы избежать ошибок в расчетах, нужно запомнить, что при считывании значения искомой величины из таблицы возможно два варианта написания внесенной в головку таблицы степени:
а) если в головке таблицы записан символ свойства, умноженный на какую-то степень (как в нашем фрагменте таблицы), то найденное для конкретного вещества значение нужно взять с обратной степенью. Например, значение вязкости при 273 К 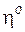 = 10,20 ×10 – 3 Па×с;
= 10,20 ×10 – 3 Па×с;
б) если в головке таблицы записан символ свойства, затем стоит запятая и какая-либо степень, то найденное для конкретного вещества значение из таблицы нужно взять с этой степенью. Например, если в головке таблицы было бы указано 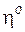 ,10−3, Па×с, то при 273 К мы запишем следующее значение вязкости:
,10−3, Па×с, то при 273 К мы запишем следующее значение вязкости: 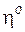 = 10,20×10 – 3 Па×с. Такие же правила выноса повторяющегося множителя справедливы и для рисунков.
= 10,20×10 – 3 Па×с. Такие же правила выноса повторяющегося множителя справедливы и для рисунков.
3.При построении графической зависимости нужно помнить, что этим графиком придется пользоваться для дальнейших расчетов, значит, он должен быть удобен для работы. Поэтому при выборе масштаба не ставьте перед собой цель разместить график на всем пространстве бумаги, отведенном для него. Лучше оставить немного места с боков, сверху и снизу, но сделать разумный масштаб, чем занять всю площадь листа, но с неудобным для работы масштабом. Основа выбора масштаба по осям – те значения данных, которые есть в задаче.Например, в рассматриваемой задаче − по оси ординатменьшее значение −6,05, большее значение −4,59, значит, шкала должна перекрывать нижнее и верхнее значение. Нет необходимости начинать шкалу от нуля, т.к. все данные условия задачи расположены в диапазоне, далеком от нуля. Выберем следующий диапазон шкалы −6,5¸−4,0.
По оси абсциссменьшее значение 3,19, большее – 3,66. Значения таковы, что не имеет смысла начинать шкалу оси абсцисс с нуля, начнем ее со значения 3,1, а закончим значением 3,7.
При правильном выборе масштаба линия зависимости на координатной плоскости будет расположена примерно под углом 45о, т.е. так, что погрешность графического определения величин будет минимальной.
Пример 2. Изобразите графически зависимость мольной изобарной теплоемкости чистого этиленгликоля в интервале температур 100−300 оС.
Решение. Зависимость мольной изобарной теплоемкости веществ от температуры задается температурными рядами вида (Д)-(Ж). Для того чтобы определить значения коэффициентов температурных рядов, нужно обратиться к справочной литературе. Ниже приведены фрагменты двух таблиц, на примере которых рассмотрим особенности работы со справочными материалами. Для удобства работы в этих таблицах представлена только та информация, которая нужна для решения задачи.
Обычно в таблицах термодинамических величин (см. табл. 2.2) содержится еще информация об интервале температур, в которых эмпирические коэффициенты температурного ряда теплоемкости были определены. Температуры в условиях задач выбраны с учетом этих интервалов, поэтому в приведенном фрагменте таблицы столбец, соответствующий данной информации, удален. В табл. 2.2 приведены температурные коэффициенты теплоемкости для двух агрегатных состояний: жидкого и газообразного. Для того чтобы правильно выбрать величины, необходимо уточнить, в каком агрегатном состоянии находится этиленгликоль в определенном интервале температур.
Таблица 2.2
Термодинамические свойства простых веществ и соединений
| Вещество | 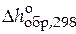 , кДж / моль , кДж / моль | 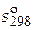 , Дж/(моль∙К) , Дж/(моль∙К) | Коэффициенты уравнения 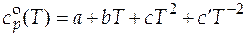 | |||
| а | 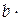 103 103 | c ∙106 | 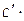 10−5 10−5 | |||
| C4H8 (г) циклобутан | 26,65 | 265,39 | -24,43 | 365,97 | -140,88 | - |
| С4Н10 (г) бутан | -26,15 | 310,12 | 18,23 | 303,56 | -92,65 | - |
| C2H6O2(ж) этиленгликоль | -454,90 | 167,32 | 151,0 | - | - | - |
| C2H6O2(г) этиленгликоль | -389,32 | 323,55 | 46,26 | 200,50 | -77,90 | - |
Для этого обратимся к табл. 2.3, в которой, кроме данных о термодинамических функциях испарения, приведено и значение температуры кипения. Анализ данных табл. 2.3 показывает, что температура фазового перехода этиленгликоль (жидкость) - этиленгликоль (газ) равна 470,39 К. Переводим температуру условия задачи в термодинамическую шкалу - шкалу Кельвина и делаем вывод, что температурный интервал из условия задачи нужно разделить на два интервала. Первый − 373−470,39 К − характеризует состояние этиленгликоля в виде жидкости, и зависимость теплоемкости от температуры будет иметь вид (Е), а второй интервал − 470,39−573 К − будет соответствовать газообразному состоянию этиленгликоля, и зависимость теплоемкости от температуры будет иметь вид уравнения (Ж).
Таблица 2.3
Температуры кипения жидкостей, мольные измерения энтальпии
и энтропии при испарении
| Вещество | Температура кипения, К | 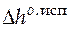 , кДж/моль , кДж/моль | 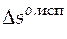 , Дж/(моль·К) , Дж/(моль·К) | |
| C2H6O этанол | 351,47 | 39,3 | 111,8 | |
| C2H6O2 этиленгликоль | 470,39 | 48,6 | 103,4 | |
| C3H6O ацетон | 329,28 | 29,107 | 88,3 |
С учетом величин, приведенных в табл. 2.2, получаем следующую зависимость мольной изобарной теплоемкости этиленгликоля от температуры
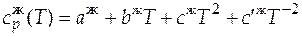 = 151,0 Дж/(моль×К).
= 151,0 Дж/(моль×К).
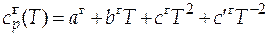 =
=
= 46,26 + 0,2005 T - 77,90×10-6 T 2 Дж/(моль×К).
Еще раз отметим, что нужно внимательно относиться к степеням величин, приведенных в таблицах. Часто степень вносят в головку таблицы. Например, в нашем примере для коэффициента b газообразного этиленгликоля в таблице указано 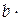 103, и когда мы находим в таблице величины 200,50, то значение b равно 200,50×10-3 , или 0,2005. В данной задаче графическая зависимость теплоемкости будет состоять из двух линий, при температуре фазового перехода одна из них будет заканчиваться, другая начинаться. Задавая произвольные значения температуры в каждом интервале, легко вычислить значения теплоемкости (рис. 2.2).
103, и когда мы находим в таблице величины 200,50, то значение b равно 200,50×10-3 , или 0,2005. В данной задаче графическая зависимость теплоемкости будет состоять из двух линий, при температуре фазового перехода одна из них будет заканчиваться, другая начинаться. Задавая произвольные значения температуры в каждом интервале, легко вычислить значения теплоемкости (рис. 2.2).
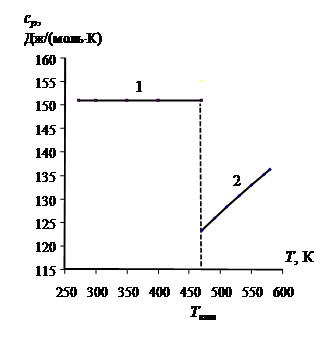
Рис. 2.2. Зависимость
мольной изобарной теплоемкости этиленгликоля от температуры:
линия 1 - теплоемкость жидкого
этиленгликоля;
линия 2 - теплоемкость газообразного этиленгликоля
 2015-09-06
2015-09-06 794
794








