Многие качественные реакции в настоящее время для обнаружения
a-аминокислот и пептидов.
1. Способность к образованию комплексных солей с ионами тяжелых металлов:
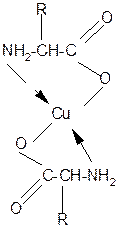 |
··
 2NH2-CH-C=O + Cu2+ +2Н+
2NH2-CH-C=O + Cu2+ +2Н+
½ ½
R OH
··
Комплексная соль Cu2+ хорошо растворима в воде и окрашена в ярко-синий цвет, что может быть использовано как качественная реакция на a- аминокислоты.
2. Образование оснований Шиффа:

 H-C=O + H2N-CH2-COOH H2C-N H -CH2-COOH H2O +
H-C=O + H2N-CH2-COOH H2C-N H -CH2-COOH H2O +
½ глицин ½
H OH
+ CH2=N-CH2-COOH
метилениминокислота
Реакция лежит в основе метода формольного титрования по Зеренсену. Сами аминокислоты вследствие амфотерности не могут быть оттитрованы щелочью. Иминокислота содержит свободную карбоксильную группу и может быть определена количественно титрованием щелочью.
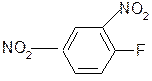
3. Взаимодействие с 2,4-динитрофторбензолом – ДНФБ (реактивом Сенджера):
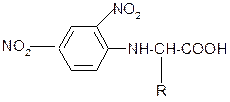 | |||
 | |||
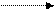 + H2N-CH-COOH
+ H2N-CH-COOH
½ –HF
R
ДНФБ a-аминокислота ДНБ-производное
ДНБ-производное аминокислоты может быть выделено и идентифицировано хроматографически. Метод служит для определения аминокислотной последовательности белка.
4. Нингидриновая реакция обусловлена наличием a- аминогруппы, качественная реакция на a- аминокислоты, пептиды и белки:
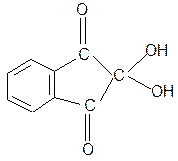 t°
t°
 + NH2-CH-COOH
+ NH2-CH-COOH
2 ½
R
a- аминокислота
нингидрин
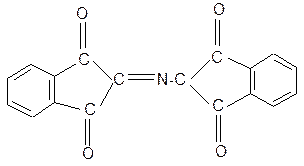 |
 H + CO2 + 3H2O + R-CHO
H + CO2 + 3H2O + R-CHO
продукт сине-фиолетового цвета
Глоссарий
Амфотерность – способность соединения проявлять и кислотные, и основные свойства.
Первичная структура пептидов и белков – это аминокислотная последовательность, т.е. порядок чередования a-аминокислотных остатков в молекуле.
Вторичная структура пептидов и белков – это пространственная ориентация основной полипептидной цепи. Основные виды - a- спираль и b–структура.
Изоэлектрическое состояние молекулы – состояние молекулы аминокислоты, пептида или белка, при котором суммарный заряд на молекуле равен нулю.
Изоэлектрическая точка – значение рН водного раствора аминокислоты, пептида или белка, при котором молекула достигает изоэлектрического состояния.
Пептидная связь (группа) – это группа атомов -СО–NН -, регулярно повторяющаяся в полимерной цепи молекулы.
Тема 8. Углеводы
Цель занятия: закрепить и расширить знания принципов стереоизомерии, таутомерного равновесия и химических свойств, важнейших моно-, ди- и полисахаридов, участвующих в процессах жизнедеятельности, а также приобрести практические навыки идентификации углеводов.
Конкретные задачи
1. Студент должен знать:
– пространственное строение моно-, ди- и полисахаридов;
– виды изомерии и таутомерию углеводов, а также их химические свойства и биологическое значение.
2. Студент должен уметь:
– писать формулы важнейших моно-, ди- и полисахаридов в открытой и циклической формах;
– изображать конформации пиранозного цикла моносахаридов и фрагментов полисахаридов;
– определять по формуле Фишера принадлежность углевода к стереохимическому ряду (D - или L -);
– описывать уравнениями химические свойства моносахаридов;
– доказывать восстанавливающую способность углеводов дисахаридов;
– проводить качественные реакции для обнаружения и доказательства строения глюкозы, фруктозы, мальтозы, сахарозы, крахмала.
Мотивация. Углеводы – один из важнейших классов органических природных соединений, играющий большую роль в процессах, обеспечивающих нормальную деятельность живых организмов. Они принимают участие в энергетическом и пластическом обмене; с углеводами связана специфичность групп крови высших организмов; химия иммунитета. Многие углеводы используются в качестве медицинских препаратов.
Вопросы для самоподготовки
1. Открытые и циклические таутомерные формы глюкозы, галактозы, маннозы,
фруктозы, рибозы, дезоксирибозы и ксилозы.
2. Реакции окисления и восстановления моносахаридов.
3. Гликозиды и их биологическая роль.
4. Сложные эфиры углеводов: моно-, ди- и полисахаридов.
5. Доказательство строения углеводов – моносахаридов.
6. Строение, номенклатура и восстанавливающая способность дисахаридов:
мальтозы, лактозы, целлобиозы.
7. Строение гомополисахаридов: крахмала, гликогена, клетчатки (целлюлозы). Их
гидролиз.
 2015-10-22
2015-10-22 2487
2487
