Водоро́д (Н) — первый элемент периодической системы элементов. Простое вещество водород — лёгкий бесцветный газ. В смеси с воздухом или кислородом горюч и взрывоопасен. Нетоксичен. Растворим в этаноле и ряде металлов: железе, никеле, палладии, титане, платине. Практически не растворим в серебре. Самый лёгкий газ. Молекула водорода двухатомна — Н2.
Химические свойства. Молекулы водорода достаточно прочны, и для того, чтобы водород мог вступить в реакцию, должна быть затрачена большая энергия.
Поэтому при обычных температурах водород реагирует только с очень активными металлами, например, с кальцием, образуя гидрид кальция, и с единственным неметаллом — фтором, образуя фтороводород.
При взаимодействии с активными металлами водород образует гидриды.
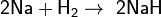
Гидриды — солеобразные, твёрдые вещества, легко гидролизуются. Соединения водорода с металлами и с имеющими меньшую электроотрицательность, чем водород, неметаллами.
Получают:
· Конверсия с водяным паром при 1000 °C.
· Пропускание паров воды над раскалённым коксом при температуре около 1000 °C.
· Электролиз водных растворов солей.
Хим св-ва:
С неметаллами водород образует летучие соединения молекулярного строения. В обычных условиях это газы или летучие жидкости.
1. В периодах слева направо у ионов элементов положительный заряд увеличивается. В связи с этим кислотные свойства летучих водородных соединений элементов в водных растворах усиливаются.
2. В группах сверху вниз отрицательно заряженные анионы все слабее притягивают положительно заряженные ионы водорода Н+. В связи с этим облегчается процесс отщепления ионов водорода Н+ и кислотные свойства водородных соединений увеличиваются.
3. Водородные соединения неметаллов, обладающие в водных растворах кислотными свойствами, реагируют со щелочами. Водородные же соединения неметаллов, обладающие в водных растворах основными свойствами, реагируют с кислотами.
4. Окислительная активность водородных соединений неметаллов в группах сверху вниз сильно увеличивается.
Атомарный водород используется для атомно-водородной сварки.
Химическая промышленность
· При производстве аммиака, метанола, мыла и пластмасс.
· В качестве газа-носителя в газовой хроматографии.
 2018-01-21
2018-01-21 1419
1419
