При проведении анализа возникает необходимость перевести одни малорастворимые соединения в другие. Например, в систематическом ходе анализа катионов III аналитической группы сульфат бария необходимо перевести в карбонат. Осадок BaSO4 обрабатывают при нагревании насыщенным раствором карбоната натрия:
BaSO4(ТВ) + Na2CO3(насыщ.)  BaСO3(ТВ) + Na2SO4.
BaСO3(ТВ) + Na2SO4.
Имеем два равенства:
[Ba2+][SO42–] = ПР BaSO4 = 1,1 · 10–10. (I)
[Ba2+][СO32–] = ПР BaСO3 = 5,1 · 10–9. (II)
Разделим равенство (II) на (I):

Следовательно, для перевода BaSO4 в BaСO3 необходимо, чтобы концентрация карбонат-ионов превысила концентрацию сульфат-ионов в ≈ 46 раз.
VI. Дробное осаждение.
При проведении осаждения приходится учитывать вероятность выпадения в осадок нескольких соединений, поскольку в исследуемом растворе возможно присутствие нескольких ионов, образующих малорастворимые соединения с осадителем.
Важно знать последовательность выпадения веществ в осадок. Согласно правилу произведения растворимости прежде всего должна пойти реакция, при которой образуется осадок, у которого при меньшей концентрации осадителя будет достигнута величина ПР.
Пример 7. Какой из осадков будет выпадать первым, если в раствор, содержащий сульфат- и хромат-ионы в концентрации 0,1 моль/л, добавить ацетат свинца (II)?
Решение:
Pb2+ + SO42– = PbSO4 ↓  = 1,6 · 10–8
= 1,6 · 10–8
Pb2+ + CrO42– = PbCrO4 ↓  = 1,8 · 10–14
= 1,8 · 10–14
Выпадение PbSO4 начнется при:
[Pb2+] = 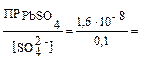 1,6 · 10–7 моль/л.
1,6 · 10–7 моль/л.
Образование PbCrO4 начнется при:
[Pb2+] = 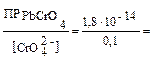 1,8 · 10–13 моль/л.
1,8 · 10–13 моль/л.
Расчет показал, что первым в осадок выпадать будет хромат свинца (II), поскольку для достижения его произведения растворимости требуется меньшая концентрация катионов свинца.
По величине ПР можно судить о последовательности выпадения осадков в том случае, когда электролиты однотипны и исходные концентрации осаждаемых ионов одинаковы.
Контрольные вопросы
1. Способы выражения растворимости малорастворимых сильных электролитов.
2. Произведение растворимости малорастворимого электролита. Как взаимосвязаны растворимость и произведение растворимости?
3. Условия образования осадков. Перевод одних малорастворимых электролитов в другие.
4. Влияние добавок посторонних электролитов на растворимость малорастворимых сильных электролитов. Солевой эффект.
5. Дробное осаждение и дробное растворение осадков.
6. Термодинамическая и концентрационная величина произведения растворимости. Как связаны эти величины?
 2020-06-08
2020-06-08 1251
1251








