1. Актуальность темы:
Живой организм является не только системой, в которой возникает биоэлектричество, но и пассивным проводником электрического тока, возникающего в организме или приложенного извне. В организме происходит ряд окислительно-восстановительных реакций, которые при соответствующих условиях могут служить источником э.д.с. Многие вещества, находясь в виде ионов, перераспределяются и транспортируются в виде зарядов, что служит причиной возникновения биоэлектрических потенциалов. Окислительно-восстановительные реакции позволяют координировать на уровне организма функции органов, тканей, клеток и субклеточных структур. Возможно их применение для диагностики и лечения заболеваний. Окислительно-восстановительные реакции лежат в основе методов оксидиметрии (перманганатометрия, йодометрия), которые применяют в клиническом анализе для определения, например, содержания мочевой кислоты в моче, кальция в сыворотке крови и т.д.
2. Цель обучения:
Знать классификацию электродов и их устройство, устройство и принцип действия гальванических элементов, механизмы возникновения электродных, окислительно-восстановительных, диффузионных и мембранных потенциалов. Уметь составлять схемы гальванических элементов, прогнозировать направление протекания окислительно-восстановительных реакций, рассчитывать окислительно-восстановительные потенциалы, рассчитывать ЭДС гальванического элемента.
1. Понятие об окислительно-восстановительных процессах. Окислители и восстановители.
2. Электродные потенциалы, механизмы их возникновения. Формула Нернста для расчета величины электродного потенциала.
3. Виды электродов. Нормальный (стандартный) электродный потенциал.
4. Гальванические элементы, их классификация. Устройство и принцип работы биметаллических и концентрационных элементов.
5. Понятие об ЭДC гальванических элементов. Уравнение Нернста.
6. Виды биологических потенциалов, механизмы их возникновения:
a) диффузный; б) мембранный (потенциал покоя и повреждения); в) потенциал течения; г) окислительно-восстановительный (редокс-потенциал).
7. Взаимосвязь между ЭДС, Kр, ∆G. Направленность окислительно-восстановительных реакций.
8. Значение окислительно-восстановительных потенциалов в механизмах процессов биологического окисления.
9. Методы оксидиметрии: перманганатометрия и йодометрия, их применение в лабораторно-клиническом анализе.
| № задачи | Текст задания: |
| 1. | Вычислить потенциал оловянной пластинки, опущенной в раствор соли олова с концентрацией 0,001моль/л. |
| 2. | Рассчитать э.д.с. гальванического элемента в стандартных условиях: (-) Zn ï Zn(NO3)2 (0,1 М) ïï Pb (NO3)2 (1М) ï Pb (+) |
| 3. | Рассчитать ЭДС гальванического элемента: Сu ï Cu(NO3)2 (0,1 М) ïï Cu (NO3)2 (1 M) ï Cu |
| 4. | В каком направлении возможно самопроизвольное протекание реакции Na2SO4 + MnO2 + KOH " Na2SO3 + KMnO4 + H2O в стандартных условиях, если 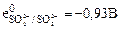 , ,  |
| № задачи | Эталоны ответов: |
| 1. | Электрод первого рода, схема записи Sn2+|Sn, уравнение электродной реакции: Sn2+ + 2e ↔ Sn Уравнение Нернста для электрода: 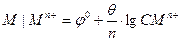 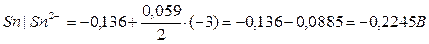 |
| 2. | 1 способ решения: Zn – 2ē " Zn+2 eo = -0,76 B окисление, анод Pb+2 + 2ē " Pb eo = -0,13 B восстановление, катод Суммарное уравнение: Zn + Pb+2 " Zn+2 + Pb 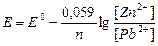 , где Ео = ео катода – ео анода Eо = eо (Pb+2/Pb) – eо (Zn+2/Zn) = - 0,13 – (-0,76) = +0,63 B , где Ео = ео катода – ео анода Eо = eо (Pb+2/Pb) – eо (Zn+2/Zn) = - 0,13 – (-0,76) = +0,63 B 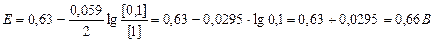 2 способ решения: Рассчитываем значение электродного потенциала для каждого элемента отдельно: Катод: 2 способ решения: Рассчитываем значение электродного потенциала для каждого элемента отдельно: Катод: 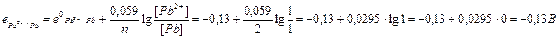 Анод: Анод: 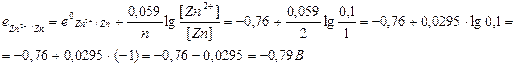 Е0 = е0катода – е0анода = -0,13 – (-0,79) = 0,66 В. Е0 = е0катода – е0анода = -0,13 – (-0,79) = 0,66 В. |
| 3. | Cu - 2ē " Cu+2 eo = 0,34 B окисление, анод Cu+2 + 2ē " Cu eo = 0,34 B восстановление, катод Суммарная реакция: Cu + Cu+2 (1M) " Cu+2 (0,1M) + Cu E = Eо - 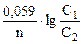 , где Ео = ео катода – ео анода = 0,34 – 0,34 = 0 В E = , где Ео = ео катода – ео анода = 0,34 – 0,34 = 0 В E = 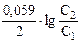 = 0,0295 ´ lg = 0,0295 ´ lg  , E = 0,0295 ´ lg10 = 0,0295 B , E = 0,0295 ´ lg10 = 0,0295 B |
| 4. | 3Na2SO4 + 2MnO2 + 2KOH " 3Na2SO3 + 2KMnO4 + H2O   S+6 +2ē " S+4 6 3 восстановление, катод, eo = -0,93 B Mn+4 -3ē " Mn+7 2 окисление, анод, eo = 0,6 B Ео = ео катода – ео анода = -0,93 – 0,6 = -1,53 В Eo< 0 Þ DG > 0 Данная реакция самопроизвольно протекает в обратном направлении. S+6 +2ē " S+4 6 3 восстановление, катод, eo = -0,93 B Mn+4 -3ē " Mn+7 2 окисление, анод, eo = 0,6 B Ео = ео катода – ео анода = -0,93 – 0,6 = -1,53 В Eo< 0 Þ DG > 0 Данная реакция самопроизвольно протекает в обратном направлении. |
5. Вспомогательные материалы по самоподготовке:
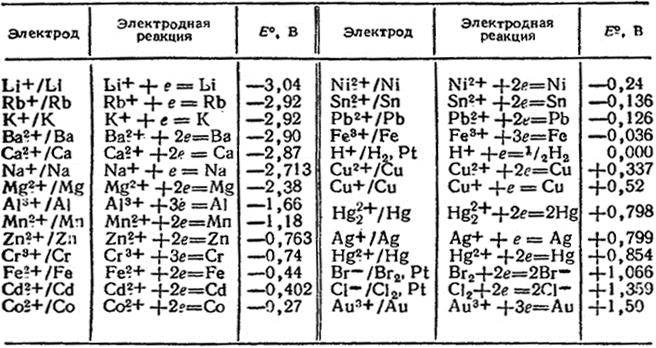
Таб. 1. Стандартные электродные потенциалы в водных растворах при 25°С
6. Выполнить тестовые задания (письменно):
| 4. | Что называется электродным потенциалом? | |
| А | разница электрических потенциалов в растворе электролита | |
| В | скачок потенциала на границе раствор-газ | |
| С | скачок потенциала на границе металл-раствор электролита | |
| D | потенциал электрода при условии, что активности компонентов, участвующих в электродной реакции равны единице | |
| 5. | Положение металла в электрохимическом ряду напряжений характеризует… | |
| А | восстановительную способность металла и окислительную способность его ионов при любых условиях | |
| В | каталитическую активность металла при любых условиях | |
| С | только восстановительную активность металла при любых условиях | |
| D | только окислительную активность ионов металла в водных растворах при стандартных условиях | |
| 6. | Какой процесс происходит по схеме S-2 ® S+6 и сколько электронов принимают в нем участие? | |
| А | восстановление, 8 электронов | |
| В | окисление, 6 электронов | |
| С | окисление, 8 электронов | |
| D | восстановление, 6 электронов | |
| 4. | Газовый электрод (инертный металл, насыщенный газом и погруженный в раствор, содержащий ионы газообразного вещества) принадлежит к электродам: | |
| А | I – рода | |
| В | II – рода | |
| С | окислительно-восстановительным | |
| D | ионоселективным | |
| 5. | В качестве стандартного электрода для измерения электродных потенциалов используется: | |
| А | каломельный электрод | |
| В | водородный электрод | |
| С | хингидронный электрод | |
| D | стеклянный электрод | |
| 6. | Для расчета величины электродного потенциала при 298 К пользуются уравнением: | |
| А | Е = Е0 + 0,059 lg a Men+ | |
| В | Е = 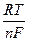 lg a Men+ lg a Men+ | |
| С | Е = Е0 + 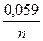 lg a Men+ lg a Men+ | |
| D | Е = Е0 + 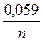 lg lg 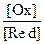 | |
| 7. | В схемах гальванических элементов двумя вертикальными чертами условно обозначается… | |
| А | внутренняя цепь элемента | |
| В | граница электрода | |
| С | двойной электрический слой | |
| D | солевой мостик | |
| 8. | Окислительно-восстановительные электроды – электроды... | |
| А | на которых протекает ОВР реакция | |
| В | состоящие из металла, который не принимает участие в электродной реакции, а только переносит электроны от восстановителя к окислителю | |
| С | состоящие из металла, покрытого слоем его труднорастворимой соли и погруженного в раствор, содержащей анионы этой соли | |
| D | состоящие из металла, погруженного в раствор собственной соли | |
| 9. | Стандартный электрод (водородный) работает при условии: | |
| А | a H+ = 1; P(Н2) = 101,3 кПа; Е H2 / 2H+ = 0 | |
| В | a H+ = 0,1; P(Н2) = 101300 Па; Е H2 / 2H+ = 0 | |
| С | a H+ = 1; P(Н2) = 1 атмосфера; Е H2 / 2H+ = 0 | |
| D | T = 298 K; P(Н2) = 101,3 кПа; Е H2 / 2H+ = 0 | |
| 10. | Мембранный потенциал клетки преимущественно определяется соотношением концентраций… | |
| А | ионов Са2+ и Mg2+ | |
| В | фруктозы и глюкозы | |
| С | ионов К+ и Na+ | |
| D | кислорода и углекислого газа | |
| 11. | Электроды первого рода: | |
| А | медный электрод в растворе сульфата цинка | |
| В | серебряный электрод в растворе нитрата серебра | |
| С | цинковый электрод в растворе сульфата меди | |
| D | серебряный электрод в растворе хлорида серебра | |
| 12. | При механическом повреждении клеточных мембран возникает потенциал: | |
| А | диффузионный | |
| В | окислительно-восстановительный | |
| С | мембранный | |
| D | термодинамический | |
| 13. | Единицы измерения электродного потенциала: | |
| А | В/м (вольт/метр) | |
| В | Вт (ватт) | |
| С | В (вольт) | |
| D | кДж/моль | |
| 14. | Как изменится масса железной пластинки, опущенной в раствор СaCl2? | |
| А | Увеличится | |
| В | Уменьшится | |
| С | Не изменится | |
| 15. | Что такое гальванические элементы? | |
| А | приспособления для превращения тепловой энергии в работу | |
| В | устройства для превращения химической энергии в электрическую | |
| С | установки для превращения электрической энергии в химическую | |
| 16. | На аноде гальванического элемента происходит процесс: | |
| А | окисление | |
| В | присоединение электронов | |
| С | восстановление | |
| 17. | Для экспериментального измерения э.д.с. гальванических элементов используют метод: | |
| А | рефрактометрии | |
| В | потенциометрии | |
| С | калориметрии | |
| 18. | В основе работы цинк-никелевого гальванического элемента лежит реакция: | |
| А | Ni2+ + Zn ↔ Ni + Zn2+ | |
| В | Ni + Zn2+↔ Ni2++Zn | |
| С | Zn2+- 2e-↔ Zn | |
| D | Ni2+- 2e-↔ Ni | |
| 19. | В основе работы элемента Якоби-Даниэля лежит реакция: | |
| А | Cu2+ + Fe→ Fe2+ + Cu | |
| В | Cu2+ + Zn→ Zn2+ + Cu | |
| С | Cd2+ + Zn→ Zn2+ + Cd | |
| D | Ni + Zn2+↔ Ni2++Zn | |
| 20. | Если в ротовой полости находятся протезы, сделанные из золота и железа, то происходит… | |
| А | окисление золота | |
| В | окисление железа | |
| С | растворение обоих металлов | |
| D | растворение золота |
6. Задачи для самостоятельного решения (выполнить письменно):
| 1. | Уравнять окислительно-восстановительную реакцию методом электронного баланса, определить окислитель и восстановитель: FeСО3 + КMnО4 + H2SO4 = Fe2(SO4)3 + CО2 + MnSO4 + K2SO4 + H2O | |
| 2. | Рассчитать электродный потенциал серебряного электрода в 0,1 M растворе AgNO3. ео(Ag+/Ag) = 0,799 B. | |
| 3. | Определите ЭДС гальванического элемента Al/Al3+ // Cu2+/Cu, если С (Al3+) = 10ˉ3 моль/л, еo(Al3+/Al) = –1,66 B C (Cu2+) = 10ˉ2 моль/л, еo(Cu2+/Cu) = 0,337 B | |
| 4. | Возможно ли самопроизвольное протекание окислительно-восстановительной реакции при стандартных условиях? K2Cr2O7 + КI + H2SO4 → Cr2(SO4)3 + I2 + K2SO4 + H2O еo(Cr2O72ˉ/2Cr3+) = 1,33 B; еo(I2 /2 Iˉ) = 0,54 B Уравнять реакцию. | |
| 5. | Рассчитать ЭДС концентрационного гальванического элемента, состоящего из медных электродов, опущенных в растворы Cu(NO3)2 с соответствующей концентрацией электролита С1 = 0,01 М и С2 = 0,1 М? Записать схему электрохимической цепи (гальванического элемента). |
 2020-10-10
2020-10-10 863
863








