Постулаты Бора.
Принципиальный отказ от механической трактовки атома сделал датский физик Нильс Бор в 1913 г, когда он сформулировал два постулата.
Постулат 1. Электроны в атоме могут находиться не на любых энергетических уровнях, допускаемых классической механикой. Они могут находиться лишь на определённых стационарных уровнях, на которых орбитальный момент импульса электрона L кратен величине? = hç 2 π: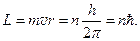
Правило квантования орбит, п = 1, 2. 3, (2.1)
Атом в стационарном состоянии не излучает и не поглощает энергии.
Постулат 2. Переход электрона с одного уровня на другой сопровождается излучением или поглощением кванта энергии 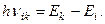
Правило частот Бора (2.2)
Здесь Ek и Ei – энергия атома с электроном на k -том и i -том уровнях, nik – частота излучаемого или поглощаемого света при переходе электрона с одного уровня на другой.
2. Основания постулатов лежат в опытных фактах.
Первый постулат, признающий существование в атомах стационарных энергетических уровней электронов, представляет собой опытный закон природы. Поскольку атомы существуют длительное время, то существуют и их состояния, в которых атомы не излучают и не поглощают. То, что классическая электродинамика не может объяснить этот факт, следует рассматривать как ограниченность электродинамики, неприменимость её для описания внутриатомных процессов.
Основанием второго постулата являются фотоэффект, тепловое излучение и сериальные закономерности в спектре атома водорода. При фотоэффекте свет поглощается квантами hn. Из законов теплового излучения следует, что излучается свет также квантами hn. Но это значит, что и спектральные линии в излучении атома водорода формируются квантами с энергией hn. Если умножить формулу Бальмера (1.6) на hc, где с – скорость света в вакууме, то получаем: 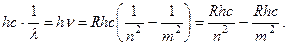 (2.3)
(2.3)
Слева стоит энергия hν кванта излучаемого атомом света, а справа – разность каких-то двух величин с размерностью энергии. Можно предположить, что выражение Rhcçn 2, где n = 1, 2, 3, 4, пропорционально энергии атома водорода в стационарных состояниях.
В качестве обоснования условия квантования момента импульса электронов на стационарных уровнях в виде L = nhç 2 π отметим пока лишь то, что именно при таком квантовании из теории Бора вытекает формула Бальмера.
3. Опыты Франка и Герца.
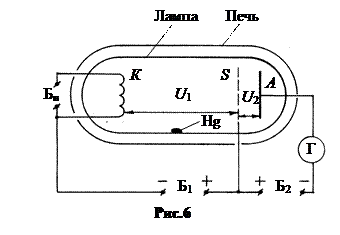
Основное положение Бора о дискретности значений энергии атома доказали экспериментально немцы Джеймс Франк и Густав Герц в 1913-14 и 1919-20 годах. Их установка представляла собой эвакуированную лампу с внесённой в неё каплей ртути (рис.6). Лампа помещалась в печь. Изменяя температуру в печи, можно было менять давление ртутных паров в лампе. В большинстве опытов давление составляло от 1 до 30 мм Hg.
Лампа включала в себя три электрода: катод К, сетку S и анод А. Батарея Бн обеспечивала регулируемый накал катода, батарея Б1 создавала ускоряющее напряжение U 1 между катодом и сеткой. Батарея Б2 создавала тормозящее напряжение U 2 между сеткой и анодом. Ток через пары ртути между сеткой S и анодом А измерялся гальванометром Г. Процесс измерений сводится к построению вольтамперной характеристики лампы. Постепенно увеличивалось напряжение U 1 между катодом К и сеткой S и записывался ток i по гальванометру Г между сеткой S и анодом А при постоянном задерживающем напряжении U 2» 0,5 В.
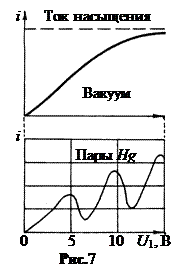
Если бы в лампе был вакуум, то вольтамперная характеристика представляла бы собой монотонную кривую, показанную на рис.7 вверху. При больших напряжениях U 1>> U 2 ток i стремится в вакууме к току насыщения.
В парáх ртути на вольтамперной кривой появляются впадины, начинающиеся при напряжениях ускоряющего поля U 1 = 4,9; 9,8; 14,7 В (рис.7 внизу). Их можно объяснить так. До напряжения 4,9 В электроны испытывают лишь упругий удар с атомами ртути. Поскольку масса атомов ртути в 400 000 раз больше массы электронов, а тепловая скорость атомов ртути по сравнению со скоростью электронов пренебрежимо мала, то электроны сталкиваются с атомами как с неподвижной стенкой. Скорость электронов меняется лишь по направлению, но не по величине.
При U 1 > U 2 кинетическая энергия электронов eU 1 оказывается достаточной для преодоления задерживающего поля U 2. С увеличением U 1 всё большая часть испущенных катодом электронов попадает на анод. Ток растёт. Но вот при напряжении 4,9 В энергия электронов оказывается равной тому кванту энергия атома ртути, который необходим для перехода атома из одного стационарного состояния в другое. При этом напряжении возле сетки S возникает зона неупругих столкновений электронов с атомами. Электроны гасят свою скорость у самой сетки S и потому не могут пройти на анод А из-за тормозящего поля U 2. Возникает первый спад тока i.
С дальнейшим ростом U 1 зона неупругих столкновений постепенно перемещается влево. Она оказывается посредине между катодом К и сеткой S при напряжении 9,8 В. Затормозившиеся здесь электроны вновь успевают разогнаться до энергии 4,9 эВ, у сетки S появляется вторая зона неупругих столкновений, и на кривой i (U 1) появляется второй спад.
Третий спад на кривой появляется при напряжении 14,7 В, когда у сетки S появляется третья зона неупругих столкновений.
Из результатов опытов следовало, что атомы ртути поглощают лишь строго определённую порцию энергии, равную e Δ U 1 = 4,9 эВ. Поглотив эту энергию, атомы ртути должны перейти на более высокий энергетический уровень, иначе, должны возбудиться. Рано или поздно, возвращаясь в основное (не возбуждённое) состояние, атомы ртути должны сбрасывать эту энергию в виде кванта hn ЭМ волны. Фотографирование спектра излучения паров Hg показало, что при напряжении U 1 > 4,9 В пары Hg действительно излучают УФ волну с λ = 253,7 нм. Если верны постулаты Бора, то энергия излучаемых фотонов hn равна энергии электронов при резонансном поглощении. 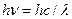
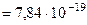 Дж. Разделив это число на заряд электрона 1,6·10-19 Кл, получаем энергию фотона в электрон-вольтах, hn = 4,9 эВ. Это как раз энергия электронов e Δ U 1 при резонансном поглощении.
Дж. Разделив это число на заряд электрона 1,6·10-19 Кл, получаем энергию фотона в электрон-вольтах, hn = 4,9 эВ. Это как раз энергия электронов e Δ U 1 при резонансном поглощении.
4. Теория водородоподобного атома по Бору.
Рассмотрим основные параметры атома, построенного в соответствии с постулатами Бора. Будем говорить в общем случае о водородоподобном атоме, имеющем ядро с зарядом ze +, вокруг которого движется один электрон. Это, например, атом водорода, z = 1; однократно ионизированный атом гелия (ион гелия He+), z = 2; двукратно ионизированный атом лития (ион лития Li++), z = 3 и т.д. В соответствии с результатами опытов Резерфорда полагаем, что взаимодействие электрона с ядром подчиняется закону Кулона.
Электрон в атоме Бора движется вокруг ядра под действием кулоновских сил. В первом приближении можно считать, что масса ядра бесконечно велика по сравнению с массой электрона. В этом случае ядро остаётся неподвижным, а электрон движется по круговым орбитам. Уравнение его движения можно записать так: 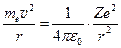 . (2.4)
. (2.4)
Здесь r – радиус орбиты электрона, me – масса покоя электрона.
Добавив условие квантования момента импульса круговых орбит из первого постулата Бора, получаем систему двух уравнений 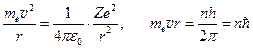 , (2.5), (2.6)
, (2.5), (2.6)
где 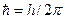 - перечёркнутая или дираковская постоянная Планка.
- перечёркнутая или дираковская постоянная Планка.
Радиусы разрешённых уровней энергии найдём, выразив из уравнения (2.6) скорость движения электрона 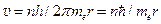 и подставим в первое уравнение.
и подставим в первое уравнение.
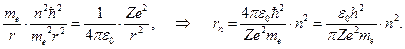 (2.7)
(2.7)
Здесь rn – радиус n- й орбиты, n = 1, 2, 3, …. Число n называют главным квантовым числом.
При z = 1 и n = 1 получаем радиус самого низкого энергетического уровня атома водорода (боровский радиус), r 1 = 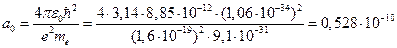 м.
м.
Диаметр атома водорода в основном состоянии равен 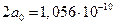 м.
м.
В атомной физике широко используется внесистемная единица длины ангстрём (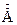 ),
), 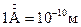 приблизительно равен поперечнику атома водорода в основном состоянии.
приблизительно равен поперечнику атома водорода в основном состоянии.
Радиусы других водородоподобных атомов удобно записывать так: 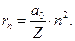 (2.8)
(2.8)
Итак, радиусы rn разрешённых уровней в водородоподобных атомах растут по квадратичному закону с ростом номера энергетического уровня n. Они тем меньше, чем больше порядковый номер элемента z в таблице Менделеева.
Скорость движения электронов на разрешённых уровнях найдём, подставив rn из формулы (2.7) в уравнение (2.6), 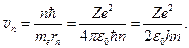 (2.9)
(2.9)
Чем выше энергетический уровень, тем меньше на нём скорость движения электрона. На первом уровне в атоме водорода скорость электрона составляет 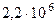 м ç с, что совпадает со значением, вычисленным на стр.7. На втором уровне, n = 2, скорость в 2 раза меньше,
м ç с, что совпадает со значением, вычисленным на стр.7. На втором уровне, n = 2, скорость в 2 раза меньше, 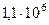 м ç с, на третьем, n = 3, скорость в 3 раза меньше и т.д.
м ç с, на третьем, n = 3, скорость в 3 раза меньше и т.д.
Энергия атома на разрешённых уровнях слагается из кинетической энергии электрона E к и потенциальной энергии E п взаимодействия электрона с ядром. Кинетическую энергию можно выразить из уравнения (2.5): 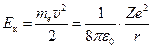 . (2.10)
. (2.10)
Потенциальная энергия электрона в поле ядра 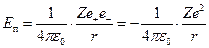 . (2.11)
. (2.11)
Здесь 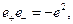 где e+ > 0 - заряд протона, e – < 0– заряд электрона, отрицательное число.
где e+ > 0 - заряд протона, e – < 0– заряд электрона, отрицательное число.
Отсюда находится полная энергия атома . (2.12)
. (2.12)
Подставив сюда rn из (2.7), получаем: 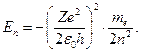 (2.13)
(2.13)
Здесь me – масса электрона, n = 1, 2, 3, – главное квантовое число.
Электрон притягивается к ядру, поэтому полная энергия системы ядро-электрон отрицательна. С ростом n энергия атома, уменьшаясь по абсолютной величине, растёт. При 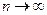
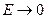 из области отрицательных значений.
из области отрицательных значений.
Для графического отображения энергетических уровней атома обычно откладывают по вертикальной оси значения энергии En, отмечая их отрезками горизонтальных прямых.

Система стационарных уровней атома показана на рис.8.
Низший уровень (n = 1) с минимальным значением энергии атома является самым устойчивым. Это основное состояние атома. Для перехода атома на уровни n = 2, 3, 4, атом должен получить извне соответствующую порцию энергии. Поэтому состояния с 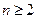 называют возбуждёнными.
называют возбуждёнными.
5. Излучение атома водорода.
Рассмотрим, как объясняет теория Бора сериальные закономерности в спектре атома водорода. Схема на рис.8 делает механизм излучения атома наглядным. Чтобы испустить квант энергии hn, электрон в атоме должен перейти с более высокого уровня на низкий. Для краткости говорят атом переходит с одного уровня на другой.
При переходе атома водорода (z = 1) из состояния m в состояние n излучается фотон с энергией 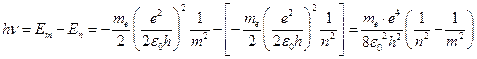 . (2.14)
. (2.14)
Разделив на hс, получаем формулу Бальмера 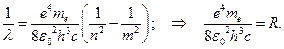 (2.15)
(2.15)
Если теоретические построения в теории Бора справедливы, то коэффициент перед скобками должен быть равен постоянной Ридберга. Из спектроскопии (опыт) 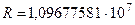 м–1. Вычисленное из (2.15)
м–1. Вычисленное из (2.15) 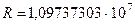 м–1. Совпадение теории с опытом с точностью до 4-х знаков можно считать большим успехом теории Бора.
м–1. Совпадение теории с опытом с точностью до 4-х знаков можно считать большим успехом теории Бора.
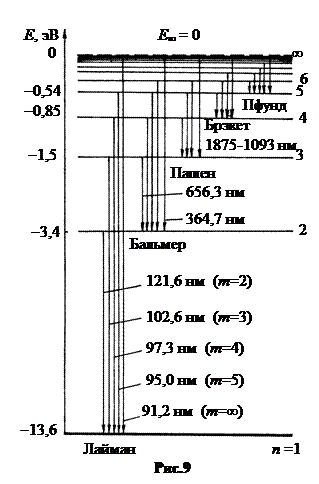
Из энергетической диаграммы, показанной на рис.9, становится понятным механизм появления спектральных серий. УФ серия Лаймана появляется при переходах атома водорода из любых возбуждённых состояний на низший энергетический уровень с n = 1. Здесь могут быть самые большие энергетические ступени, и потому самые малые длины волн λ.
Серия Бальмера образуется при переходе возбуждённого атома на уровень n = 2. Энергетические ступени здесь меньше, и серия Бальмера попадает в видимый диапазон. Энергетические ступени в сериях Пашена, Брэкета и Пфунда становятся ещё меньше. Поэтому каждая последующая серия уходит всё дальше в ИК диапазон.
6. Потенциалы возбуждения атома водорода – это те напряжения U электрического поля, в котором должен разогнаться электрон, чтобы его энергия оказалась равной кванту энергии, поглощаемой или излучаемой атомом. 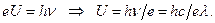 (2.16)
(2.16)
Поскольку невозбуждённое состояние атома соответствует n = 1, то все потенциалы возбуждения вычисляются из формулы Бальмера для серии Лаймана. Выразив 1 çl из (1.2) и подставив в (2.16), получаем: 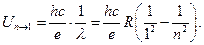 (2.17)
(2.17)
При n = 2 получаем 1-й потенциал возбуждения атома водорода.
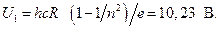 При n = 3 получаем 2-й потенциал возбуждения атома водорода U 2 = 12,12 В. Подставляя n = 4, 5, 6, и т.д., можно вычислить все последующие потенциалы возбуждения U 3 = 12,79 В, U 4 = 13,09 В…
При n = 3 получаем 2-й потенциал возбуждения атома водорода U 2 = 12,12 В. Подставляя n = 4, 5, 6, и т.д., можно вычислить все последующие потенциалы возбуждения U 3 = 12,79 В, U 4 = 13,09 В…
При n = ¥ получается такой квант энергии, при поглощении которого электрон уходит из атома. Атом превращается в ион. Потенциал ионизации атома водорода U ¥ = 13,6 В.
7. Магнитный момент электрона.
Электрон – электрически заряженная частица. Поэтому наряду с механическим орбитальным моментом 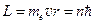 электрон в атоме обладает орбитальным магнитным моментом.
электрон в атоме обладает орбитальным магнитным моментом.
Магнитный момент кругового тока M = iS, где i – ток, протекающий по замкнутому витку, а S – площадь витка. Циркулирующий по круговой орбите электрон создаёт ток i = en = evç 2 pr, где n – частота обращения электрона. Выразив скорость v орбитального движения электрона через механический момент импульса v = Lçmer, и подставив, получаем: i = evç 2 pr = eLç 2 mepr 2. Площадь «витка» S = pr 2, где r – радиус орбиты. Отсюда орбитальный магнитный момент электрона 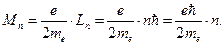 (2.18)
(2.18)
Получаем, что орбитальный магнитный момент электрона тоже квантован и кратен минимальному магнитному моменту электрона в атоме водорода в основном состоянии: 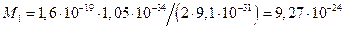 Дж ç Тл. Его называют магнетон Бора.
Дж ç Тл. Его называют магнетон Бора.
8. Принцип соответствия.
В 1923 г. Нильс Бор сформулировал постулат, названный им принципом соответствия. Суть его в том, что устанавливается количественный критерий, позволяющий решать, какими моделями – квантовыми или классическими – лучше описывается в данном явлении физическая система.
Например, электрон в атоме в рамках классической ЭМ теории должен падать с верхних энергетических уровней на нижние непрерывно. В квантовой теории электрон переходит скачками, причём с увеличением квантового числа n величина энергетических скачков постепенно уменьшается. В результате при больших значениях числа n изменение энергии электрона в атоме будет происходить практически непрерывно, а само явление можно рассматривать в рамках классической физики (См. подробнее с.3).
Принцип соответствия понимают часто в более широком смысле. Любая новая теория, претендующая на более глубокое описание физической реальности и на более широкую область применимости, чем старая, должна включать старую теорию как предельный случай.
Например, релятивистская механика включает в себя механику Ньютона как предельный случай малых скоростей, когда (v/c) → 0, оптика включает в себя геометрическую как предел при (λ/a) → 0, где λ – длина волны света, a – характерный размер препятствия.
9. Достоинства теории Бора, как крупного шага в развитии теории строения атома.
а. Объяснила сериальные закономерности в спектрах атома водорода. Вычисленная на её основе постоянная Ридберга с точностью до 4-х знаков совпадает с опытным значением. Это совпадение оказывается ещё лучше, если в уравнении движения электрона учесть, что он движется не вокруг ядра, а вместе с ядром движется вокруг общего центра масс.
б. Объяснила сериальные закономерности в спектрах водородоподобных атомов. Ещё в 1897 г. американский астроном Эдвард Пикеринг обнаружил в спектрах некоторых звёзд серию, напоминающую серию Бальмера, но немного смещённую в фиолетовую область спектра. Число линий в серии Пикеринга было больше, чем в серии Бальмера. Избыточные линии соответствовали дробным значениям числа n и не поддавались никаким объяснениям. Применение теории Бора показало, что серия Пикеринга принадлежит излучению однократно ионизированных атомов гелия и определяется формулой:
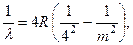 где m = 5, 6, 7, … Серия Пикеринга (2.20)
где m = 5, 6, 7, … Серия Пикеринга (2.20)
Смещение линий в фиолетовую область объяснилось тем, что постоянные Ридберга для гелия и водорода несколько отличаются из-за различия в массах ядер атомов.
Исследование спектров двукратно ионизированного лития Li++ и трёхкратно ионизированного бериллия Be+++ показали, что и для них применима обобщённая формула Бальмера, а все сдвиги спектров объяснялись теорией Бора.
в. Успехи теории Бора в объяснении спектра водородных и водородоподобных атомов показали, что классическая физика неприменима к описанию внутриатомных процессов. Теория Бора явилась толчком к большому числу экспериментальных работ, давших много важных результатов.
10. Недостатки теории Бора.
Главные из них:
а. Не позволяет определять интенсивность спектральных линий. Известно, что линии в спектрах имеют разную яркость. Очевидно, дело в том, что с одного и того же энергетического уровня одни переходы совершаются относительно чаще, другие – реже. Но почему это происходит, теория Бора не даёт объяснения. В её рамках нет даже базы для постановки такого вопроса.
б. Теория Бора не работает в атомах, следующих за водородом. Нет механизма формирования структуры атомов в таблице Менделеева. Теория Бора не объясняет природу химических связей. Не позволяет объяснить спектры многоэлектронных атомов.
в. Теория Бора логически противоречива. Она не является ни классической, ни квантовой. В системе двух уравнений, лежащих в её основе, одно – уравнение движения электрона – классическое, другое – условие квантования орбит – квантовое.
Но исторически теория Бора сыграла исключительно важную роль. Она явилась переходным этапом от классической к последовательно квантовой теории.
 2014-02-02
2014-02-02 12529
12529








