РЕАКЦИИ КАРБАНИОНОВ
1) Рекомбинация с положительно заряженными частицами, обычно с протоном, или другой частицей, имеющей вакантную орбиталь на внешней оболочке (реакция между кислотой и основанием Льюиса):
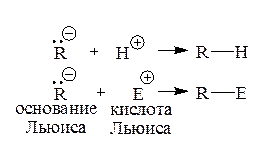
Пример: SE1-замещение (мономолекулярное) в алифатическом ряду. В качестве Е+ может выступать карбониевый ион.
См. также Пальм, стр. 315-316.
Пример: SN2-замещение (бимолекулярное) в алифатическом ряду – когда карбанион (нуклеофил) более или менее синхронно замещает уходящую группу (нуклеофуг) при насыщенном углеродном атоме:
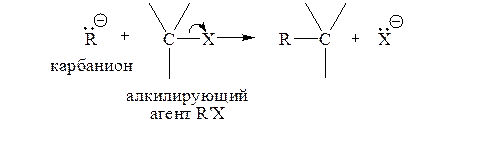
К этому типу реакций относится представительная группа реакций алкилирования атомов углерода, соединенных с «активным» (подвижным) водородом:
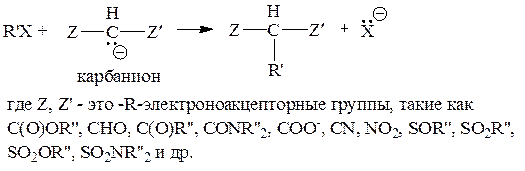
Примерами таких реакций являются:
а) Синтезы на основе ацетоуксусного эфира
Z = COOEt, Z' = COCH3
(i)
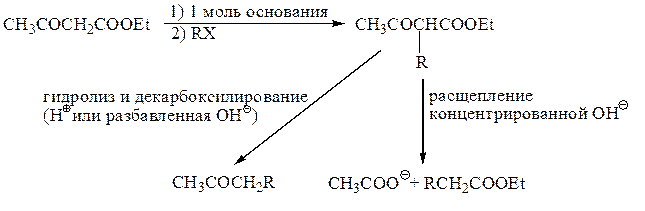
(ii) Если нужно проалкилировать менее кислый реакционный центр, то следует отщепить от АУЭ два протона, добавив два эквивалента основания; при обработке полученного дианиона одним эквивалентом алкилирующего агента проалкилируется более нуклеофильный (менее кислый, более основный) анионный центр:
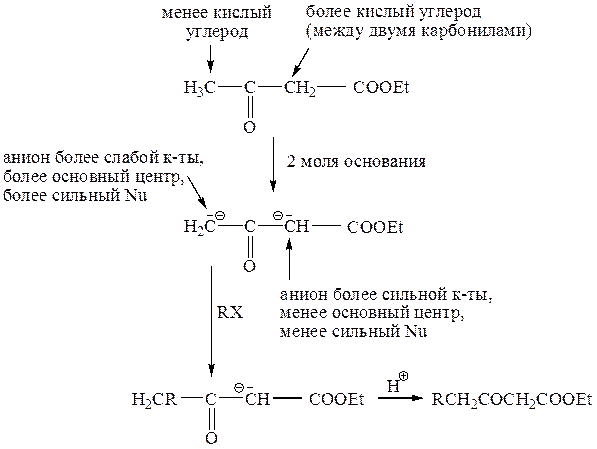
б) Синтезы на основе малонового эфира
Z = Z' = COOEt
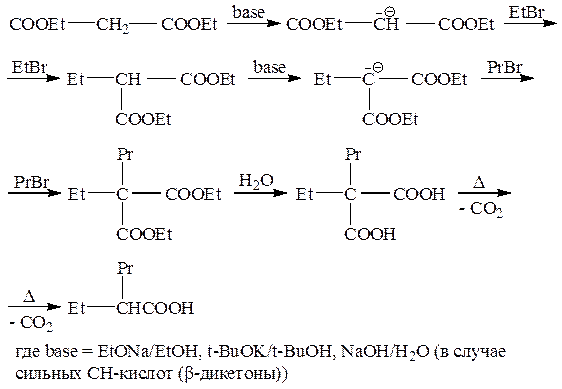
Можно также алкилировать в α-положение по отношению к С=О кетоны, сложные эфиры, соли карбоновых кислот, а также в α-положение по отношению к группе С≡N – нитрилы.
в) Сочетание алкилгалогенидов (реакция Вюрца)
В этой реакции велика роль побочных процессов (элиминирование, перегруппировки), поэтому она редко используется в синтетических целях.

 2014-02-02
2014-02-02 1227
1227
