Постулаты Бора. Первый постулат: в атоме существуют стационарные (не изменяющиеся со временем) состояния, находясь в которых атом не излучает энергии. Стационарным состояниям атома соответствуют стационарные орбиты, на которых находятся электроны. В стационарном состоянии атома для электрона на круговой орбите значения момента импульса могут принимать только определенный набор дискретных значений, удовлетворяющих условию:
 (n = 1, 2, 3, …), где
(n = 1, 2, 3, …), где
me –масса электрона, υn – скорость электрона на n -ой орбите радиуса rn,
n – номер орбиты, ħ = h/2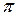 (h – постоянная Планка).
(h – постоянная Планка).
Радиус n -ой орбиты для атома водорода: 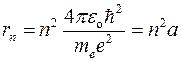 , где
, где
где e – заряд электрона, ε o – электрическая постоянная,
а – радиус первой орбиты (n = 1), называемый первым боровским радиусом.
Второй постулат: при переходе электрона с одной стационарной орбиты на другую излучается (или поглощается) один фотон с энергией hν, равной разности энергий соответствующих стационарных состояний En и Еm:
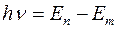 .
.
При переходе атома из состояния большей энергии в состояние меньшей энергии происходит излучение фотона, а при поглощении фотона происходит переход атома из состояния меньшей энергии в состояние большей энергии.
Дискретность набора значений энергии стационарных состояний En и Еm предопределяет дискретность набора возможных частот ν квантовых переходов между этими состояниями, что обусловливает линейчатость спектра атома.
По теории Бора полная энергия электрона на n -ой орбите атома водорода:
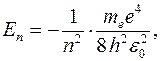 (n = 1, 2, 3, …),
(n = 1, 2, 3, …),
Из приведенной формулы следует, что энергетические состояния атома образуют последовательность уровней, энергия которых изменяется в зависимости от значения числа n, называемое главным квантовым числом. Энергетическое состояние с n = 1 является основным состоянием, а состояния с n >1 являются возбужденными с остояниями.
Согласно второму постулату Бора, при переходе атома водорода из состояния n в состояние т с меньшей энергией испускается фотон с энергией hν:
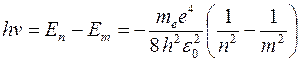 ,
,
откуда частота ν квантового перехода в спектре испускания атома водорода:
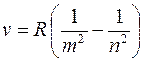 , где R – постоянная Ридберга (
, где R – постоянная Ридберга (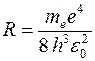 ).
).
Числа m (m = 1, 2, 3 …) и n (n = m + 1, m + 2, m + 3, …) определяют номера электронных орбит в атоме, между которыми происходит квантовый переход.
Приведенная формула описывает серии линий в спектре испускания атома водорода (рис. 31), где m определяет серию (m = 1, 2, 3…), а n определяет отдельные линии соответствующей серии (n = m + 1, m + 2, m + 3, …).
Спектр испускания атома водорода.
В ультрафиолетовой области спектра атома водорода наблюдается
серия Лаймана (m = 1): 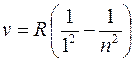 (n = 2, 3, 4, …).
(n = 2, 3, 4, …).
В видимой области спектра атома водорода наблюдается
серия Бальмера (m = 2): 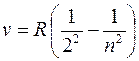 (n = 3, 4, 5, …).
(n = 3, 4, 5, …).
В инфракрасной области спектра атома водорода наблюдаются:
серия Пашена (m = 3): 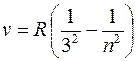 (n = 4, 5, 6, …);
(n = 4, 5, 6, …);
серия Брэкета (m = 4): 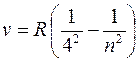 (n = 5, 6, 7, …);
(n = 5, 6, 7, …);
серия Пфунда (m = 5): 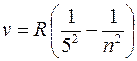 (n = 6, 7, 8, …);
(n = 6, 7, 8, …);
серия Хэмфри (m = 6): 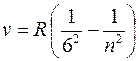 (n = 7, 8, 9, …).
(n = 7, 8, 9, …).
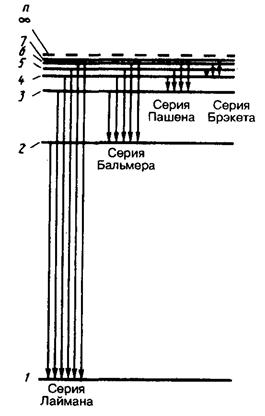

Рис. 31.
Таким образом, квантовая теория атома, созданная Бором, позволила описать экспериментально наблюдаемые атомные спектры поглощения и испускания.
 2014-02-02
2014-02-02 6670
6670
