При повышении температуры скорость большинства химических реакций существенно увеличивается, причем для гомогенных реакций при нагревании на каждые десять градусов скорость реакции возрастает в 2-4 раза.
В соответствие с правилом Вант-Гоффа для каждой реакции можно применять так называемый температурный коэффициент 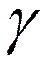 , который показывает, во сколько раз возрастает константа скорости реакции при повышении температуры на 10 0С.
, который показывает, во сколько раз возрастает константа скорости реакции при повышении температуры на 10 0С.
Зная температурный коэффициент можно по приведенной ниже формуле рассчитать изменение скорости реакции при увеличении температуры от t1 до t2
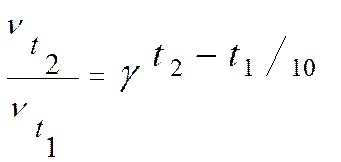 ,
,
где ut2 и ut1 - скорости реакции при температурах t2 и t1 соответственно; 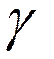 - температурный коэффициент скорости данной реакции.
- температурный коэффициент скорости данной реакции.
Например, если температурный коэффициент реакция
γ = 2, то при увеличении температуры на 100 градусов скорость реакции должна увеличиться: V398/V298 = 210 = 1024 раза.
Правило Вант-Гоффа применимо только в узком интервале температур.
При увеличении температуры скорость реакции увеличивается в значительно большей степени в сравнении с увеличением скорости движения реагирующих частиц. Причина сильного влияния температуры на скорость заключается в первую очередь в увеличении доли активных (реакционноспособных) частиц.
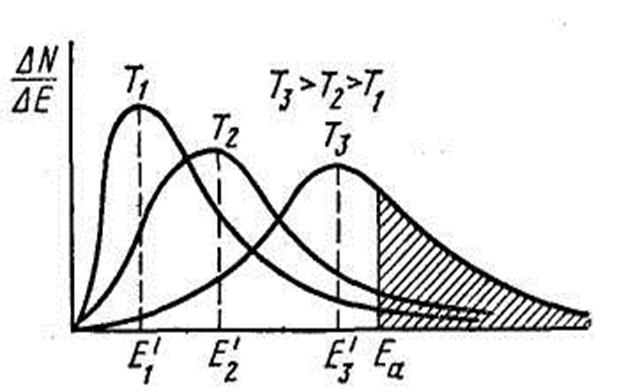 В молекулярно-кинетической теории газов распределение частиц по значениям энергии в зависимости от температуры описывается так называемой Гаусовской кривой, общий вид которой для трех различных температур приведен на рисунке 2.
В молекулярно-кинетической теории газов распределение частиц по значениям энергии в зависимости от температуры описывается так называемой Гаусовской кривой, общий вид которой для трех различных температур приведен на рисунке 2.
Рисунок 2. Распределение частиц по кинетической энергии при различных температурах:
где Т1, Т2 и Т3 значения температур, при этом Т1 < Т2 < Т3,
Е1, Е2 и Е3 – наиболее вероятные значения энергии при температурах соответственно Т1, Т2 и Т3,Еа – энергия активации.
Общее число частиц в системе (N) равно площади под кривой. Общее число частиц с энергией большей, чем Еа – равно заштрихованной площади.
Из рисунка 2 видно, что при увеличении температуры распределение частиц по энергии меняется так, что увеличивается доля частиц с более высокой энергией. Таким образом важным понятием для химической реакции является энергия активации.
Энергию активации – это энергия которой должны обладать частицы, чтобы взаимодействие их привело к химической реакции. Энергия активации выражается в кДж/моль. Для реакций, протекающих с заметной скоростью, энергия активации не превышает 50кДж/моль (для реакций ионного обмена Ea» 0); если Ea > 100 кДж/моль, то скорость реакции неизмеримо мала.
В 1889 г. С.Аррениус привел уравнение зависимости константу скорости химической реакции от температуры:
k = Ae – Ea/RT
где, A – предэкспотенциальный множитель, зависящий от природы реагирующих веществ;
R – газовая постоянная = 8,314 Дж/(моль? К);
Ea – энергия активации.
Из уравнения Аррениуса следует, что чем выше энергия активации, тем в большей степени необходимо повышать температуру для поддержания необходимой скорости реакции.
На рисунке 3 показана зависимость изменения потенциальной энергии реагирующей системы от пути протекания реакции. Из приведенного рисунка видно, что для экзотермической реакции (идущей с выделением теплоты) убыль активных молекул восполняется за счет энергии, выделяющейся в ходе реакции. В случае эндотермической реакции для поддержания необходимой скорости реакции требуется подвод тепла.
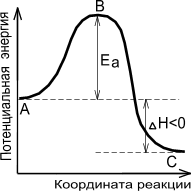 | 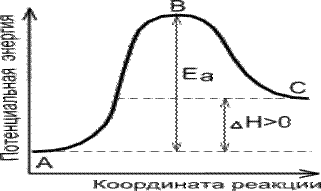 |
| Экзотермическая реакция | Эндотермическая реакция |
Рисунок 10.3 Энергетическая диаграмма химической реакции
А - реагенты, С - продукты.
2.4 Влияние посторонних веществ
Посторонние вещества в зависимости от оказываемого воздействия могут ускорять реакции – катализаторы или замедлять – ингибиторы.
Катализаторы – это вещества ускоряющие химические реакции, но сами после реакции остаются в неизменном виде.
Ингибиторы – это вещества замедляющие реакцию.На практике иногда необходимо замедлять реакции (коррозия металлов и др.) это достигается введением в реакционную систему ингибиторов. Например, нитрит натрия, хромата и дихромата калия снижают скорость коррозии металлов.
Промоторы – вещества, повышающие активность катализатора. При этом промоторы могут сами и не обладать каталитическими свойствами.
Каталитические яды – посторонние примеси в реакционной смеси, приводящие к частичной или полной потере активности катализатора. Так, следы мышьяка, фосфора вызывают быструю потерю активности катализатором V2O5 при контактном способе получения H2SO4.
3. Химическое равновесие
В химических реакциях исходные вещества не всегда полностью превращаются в продукты реакции. Это происходит потому, что по мере накопления продуктов реакции могут создаваться условия для протекания обратной реакции. Большинство химических реакций являются обратимыми.
В качестве примера проанализируем крайне важную для промышленности обратимую реакцию синтеза аммиака из азота и водорода:
прямая реакция – 2N2 + 3H2 → 2NH3,
обратная реакция – 2NH3 → N2 + 3H2,
обратимая реакция – 2N2 + 3H2 «2NH3.
Прямая и обратная реакции являются отдельными реакциями с соответствующими им кинетическими уравнениями, предэкспотециальными множителями, энергиями активаций и т.д
Важной количественной характеристикой обратимых реакций является константа равновесия, которая определяется при достижении системой химического равновесия – состояния при котором скорости прямой и обратной реакций равны. Примеры применения закона действующих масс (з.д.м.).
Выведем константу равновесия на примере реакции синтеза аммиака.
Кинетическое уравнение прямой реакции
N2+3H2 → 2NH3
имеет вид Vпр = Кпр [N2][H2]3.
Кинетическое уравнение обратной реакции
2NH3→ N2 + 3H2
имеет вид Vобр = Кобр[NH3]2.
В состоянии химического равновесия Vпр = Vобр.
Подставляя в условие химического равновесия выражения скоростей прямой и обратной реакций получаем следующее равенство Кпр [N2][H2]3 = Кобр[NH3]2.
После преобразования получаем
 .
.
4. Принцип Ле-Шателье
Если на систему, находящуюся в состоянии химического равновесия, оказывается какое-либо внешнее воздействие, то равновесие в результате протекающих в системе процессов сместится таким образом, что оказанное воздействие уменьшится.
4.1 Влияние изменения концентраций на равновесие
При увеличении концентрации какого-либо из веществ, участвующих в реакции, равновесие смещается в сторону расходования этого вещества, а при её уменьшении – в сторону образования этого вещества.
Пример 1. Если в равновесную систему
2N2 + 3H2 «2NH3
добавить N2 или H2, то в соответствии с принципом Ле–Шателье для уменьшения концентраций данных веществ, равновесие должно сместится вправо, выход NH3 увеличится. При увеличении концентрации NH3 равновесие соответственно сместится влево.
4.2 Влияние изменения давления на равновесие
Давление в замкнутой реакционной системе обусловлено наличием в ней газообразных веществ: чем их больше, тем больше давление. Поэтому изменение внешнего давления повлияет на равновесие только в тех случаях, когда в нем участвуют газообразные вещества, причем количество их в прямой и обратной реакциях разное.
Если в системе, находящейся в состоянии химического равновесия увеличить давление, то преимущественно будет протекать реакция, в результате которой уменьшается количество газообразных веществ; при уменьшении давления преимущественно протекает реакция, в результате которой увеличивается количество газообразных продуктов.
Пример 1. Можно ли изменением давления увеличить выход продуктов в реакции CO2(г) + H2(г) «CO(г) + H2O(г).
Решение: Реакционная смесь включает газообразные реагенты, но количество их в реакции не меняется: из одного моля CO2(г) и одного моля H2(г) получаются по одному молю CO(г) и H2O(г). По этой причине изменение давления на состояние равновесия не влияет.
Пример 2. Как изменятся равновесные концентрации реагентов при увеличении давления в системе N2 + 3H2 «2NH3?
Из уравнения реакции видно, что из 4 моль газа исходных продуктов образуется 2 моль газа продуктов реакции. Таким образом при увеличении давления равновесие сместится прямой реакции, так как она приводит к уменьшению давления.
4.3 Влияние изменения температуры на химическое равновесие
Большинство химических реакций протекают с выделением или поглощением тепла. В первом случае температура смеси увеличивается, во втором – уменьшается.
Если реакционную смесь, находящуюся в состоянии химического равновесия, нагреть, то в соответствии с принципом Ле Шателье должна протекать преимущественно реакция, в результате которой тепло будет поглощаться, т.е. эндотермическая реакция; при охлаждении смеси должна протекать преимущественно реакция, в результате которой тепло будет выделяться, т.е. эндотермическая реакция.
Если в системе, находящейся в состоянии химического равновесия, увеличить температуру, то равновесие смещается в сторону эндотермической реакции, а при понижении температуры – в сторону экзотермической реакции.
Пример: 2N2 + 3H2 «2NH3, 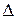 H0 = – 92 кДж
H0 = – 92 кДж
Реакция экзотермическая, поэтому при увеличении температуры равновесие сдвигается влево, а при понижении температуры – вправо.
Из этого следует, что для увеличения выхода аммиака температуру необходимо понижать. На практике выдерживают температуру 500 0С, так как при более низкой температуре резко снижается скорость прямой реакции.
Химическое равновесие имеет динамический характер: прямая и обратная реакции при равновесии не прекращаются.
Константа равновесия зависит от температуры и природы реагирующих веществ. Чем больше константа равновесия, тем больше равновесие сдвинуто в сторону образования продуктов прямой реакции
Принцип Ле Шателье универсален, так как применим не только к чисто химическим процессам, но и к физико-химическим явлениям, таким, как кристаллизация, растворение, кипение, фазовые превращения в твердых телах.
 2014-02-09
2014-02-09 20296
20296








