1. Масса растворителя, г.
2. Температура замерзания растворителя t0, 0С.
3. Определите моляльную концентрацию раствора электролита
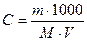
4. Вычислите понижение температуры замерзания раствора неэлектролита такой же концентрации
Δ t = К∙С.
5. Найдите понижение температуры замерзания раствора электролита
Δ t′ = tзам – t′зам.
6. Подсчитайте изотонический коэффициент
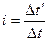
7. Определите кажущуюся степень диссоциации электролита
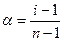
8. Вычислите относительную ошибку в процентах (см. предыдущий опыт).
Вопросы и задачи.
1. Что такое криоскопическая постоянная и каков ее физический смысл?
2. Как влияет электролитическая диссоциация растворенного вещества на понижение температуры замерзания раствора?
3. Какими методами определяется степень диссоциации электролита?
4. Найдите молекулярную массу вещества, если 2 г его растворены в 200 г воды и раствор замерзает при температуре –0,547 0С.
5. Определите температуру замерзания 0,25 н. раствора NaOH, плотность которого равна 0,01 г/мл, а степень диссоциации 0,8 %.
6. Какова температура замерзания раствора неэлектролита, содержащего 2,02∙1023 молекул в 1 литре воды?
7. Понижение температуры замерзания раствора, содержащего 0,052 г камфоры в 26 г бензола, равно 0,067 0С. Рассчитайте молекулярную массу камфоры.
8. Вычислите температуру замерзания раствора, содержащего 20 г сахара С12Н22О11 в 400 г воды.
9. При какой температуре будет замерзать 25 %-ный раствор этилового спирта в воде?
10. Изотонический коэффициент 6,8 %-ного водного раствора HCl равен 1,66. Вычислите температуру замерзания этого раствора.
11. Раствор, содержащий 6,15 г растворенного вещества в 150 г воды, замерзает при температуре –0,93 0С. Определите молекулярную массу растворенного вещества.
12. Определить температуру замерзания раствора Na2CO3, содержащего 0,265 г соли на 100 г воды, если известно, что степень диссоциации его равна 95 %.
Работа № 8
 2015-01-07
2015-01-07 1134
1134








