При обычных условиях различные газы смешиваются друг с другом в любых соотношениях.
При этом каждый газ, входящий в состав смеси, характеризуется своим парциальным давлением.
Оно представляет собой то давление, которое производило бы имеющееся в смеси количество данного газа, если бы оно одно занимало при той же температуре весь объем, занимаемый смесью.
Установленный Дальтоном закон парциальных давлений гласит: «Давление смеси газов, химически не взаимодействующих друг с другом, равно сумме парциальных давлений газов, составляющих смесь».
В условиях покоя организм потребляет 250 мл О2, в 1 мин., а при значительной физической нагрузке эта величина может возрасти до 2500 мл/мин.
Каков механизм доставки О2 к тканям?
Кислород в крови находится в двух видах — физически растворенный в плазме и химически связанный с гемоглобином (НЬ).
Для определения клинической значимости каждого из этих двух видов существования О2 требуется провести несложные расчеты.
Нормальный минутный объем сердца (МОС) равен 5 л/мин., из этой величины примерно 60% (3 л) приходится на плазму.
Коэффициент растворимости кислорода в плазме при t = 38°С и при 760 мм рт. ст. равен 0,024 мл/мл, следовательно, в 3 л плазмы может быть растворено (3000 х 0,024) 72 мл кислорода.
В крови парциальное давление О2 во много раз меньше и составляет 80—90 мм рт. ст., а так как известно, что любой газ растворяется в жидкостях пропорционально своему парциальному давлению, то несложно рассчитать, что в 3 л циркулирующей в организме плазмы крови будет находиться не 72, а 8 мл растворенного кислорода, что составляет приблизительно всего 3% от минимальной потребности организма, равной 250 мл/мин.
Полученная нами расчетная величина полностью совпадает с данными, выявленными Cuenter С. А. (1977).
Эта величина (3%) настолько мала, что ею в дальнейшем можно пренебречь и не обсуждать значение физически растворенного О2 для жизнедеятельности организма.
Исходя из вышеизложенного, становится ясным, что единственным реальным переносчиком кислорода в организме может быть только гемоглобин.
Его молекула состоит из четырех полипептидных цепей, каждая из которых связана с гемом (сложное небелковое соединение, содержащее в своем составе железо).
При присоединении кислорода к гемоглобину последний превращается в оксигемоглобин.
Объем переносимого кислорода зависит, в свою очередь, от суммарного количества циркулирующего гемоглобина и его кислородной емкости, что, в конечном итоге, определяет кислородную емкость крови — это то количество кислорода, которое одномоментно находится в связанном виде с НЬ в артериальной крови.
Кислородная емкость 1 г гемоглобина при условии 100% насыщения крови кислородом составляет 1,34 мл, следовательно, должная величина кислородной емкости крови будет равна Нb • 1,34, или при Нb, равном 150 г/л, 150 г умножаем на 1,34 мл и получается, что в одном литре крови будет находиться 201 мл связанного кислорода, или 20,1% по объему. Это и есть величина кислородной емкости крови.
Приведенные цифры носят академический характер.
На самом деле в нормальных условиях кислородная емкость артериальной крови составляет 18-19, а венозной крови — 12—14% по объему.
Разница между этими величинами носит название артериовенозной разницы по кислороду (А—В).
В норме эта величина равна 5—6% по объему.
Исходя из приведенных цифр, можно легко рассчитать, что организм в нормальных условиях утилизирует только 25% имеющегося в артериальной крови кислорода.
Оставшиеся невостребованными 75% служат для обеспечения так называемого «запаса прочности» организма по кислороду.
Уровень насыщения гемоглобина кислородом (sO2) зависит не только от суммарного количества гемоглобина, но и от парциального давления кислорода в крови (рО2), рН внутренней среды и температуры тела.
Графическая зависимость между sO2 и рО2 носит характер S-образной кривой и отражает степень насыщения гемоглобина кислородом; иначе она называется кривой диссоциации оксигемоглобина (КДО)
S-образный характер КДО имеет важное физиологическое значение.
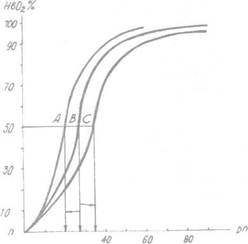
Рис. 1. Смещение кривой диссоциации гемоглобина.
А — влево; В — норма; С— вправо.
Такой характер кривой обеспечивает возможность адекватного насыщения крови при изменениях рО2 в довольно широких пределах.
Так, при снижении рО2 во вдыхаемом воздухе до 60—70 мм рт. ст. (это соответствует подъему на высоту 3—3,5 км над уровнем моря), кривая КДО смещается влево, и значительных признаков гипоксемии у человека не наблюдается.
С другой стороны, даже при значительном увеличении рО2 выше 80 мм рт. ст. (например, в условиях эксперимента в барокамере создали РaО2, равное 600 мм рт. ст.), sO2 достигает своего верхнего физиологического предела, но не превышает его.
Другое дело, что при таком высоком давлении возрастет примерно на 11% содержание физически растворенного в плазме кислорода (с 1,6 до 1,8 мл/л), но это имеет весьма косвенное отношение к КДО.
Численно сродство гемоглобина к кислороду принято выражать величиной Р50.
Она равна такому парциальному напряжению кислорода, при котором весь гемоглобин, имеющийся в артериальной системе организма (при рН 7,4 и 37°С), на 50% насыщается кислородом.
В норме Р50 равно 30 мм рт. ст. (см. рис. 1).
Смещение кривой насыщения НЬ вправо означает уменьшение способности гемоглобина связывать кислород и, следовательно, сопровождается повышением P50.
Напротив, смещение кривой влево свидетельствует о повышенном сродстве гемоглобина к кислороду, и величина Р50 будет снижена.
Помимо вышеуказанных факторов, КДО зависит и от рН.
На тканевом уровне, чем дальше от легких, тем рН тканей становится меньше (один из компонентов закисления — накопление избытка углекислого газа), а это уменьшает сродство гемоглобина к кислороду; благодаря этому артериальная кровь легко отдает его тканям на уровне системы микроциркуляции.
Обратным током кровь, ставшая к этому моменту уже венозной, попадает в сеть легочных капилляров, где рН значительно выше, чем в венозной сети.
В результате этого сродство гемоглобина к кислороду восстанавливается, и процесс переноса кислорода возобновляется.
Характер КДО зависит и от температуры тела.
Чем она выше, тем меньше будет сродство гемоглобина к кислороду и наоборот.
Знание этого фактора дает объяснение одной из причин возникновения признаков острой дыхательной недостаточности у больных с высокой температурой.
Кроме вышеуказанных факторов, на транспортную функцию кислорода существенную роль оказывает и внутриклеточный органический фосфат — 2,3-дифосфоглицерат (2,3-ДФГ).
Он непосредственно образуется в эритроцитах, находится в молекуле гемоглобина и влияет на ее сродство к кислороду.
Повышение уровня 2,3-ДФГ в эритроцитах уменьшает сродство гемоглобина к кислороду, а понижение концентрации 2,3-ДФГ приводит к увеличению его сродства к O2.
Ряд патологических синдромов может сопровождаться выраженными изменениями уровня 2,3-ДФГ как в сторону его увеличения, так и снижения.
При наличии легочных заболеваний, сопровождающихся развитием хронической гипоксии, содержание 2, 3-ДФГ повышается и, соответственно, уменьшается сродство Нb к О2, что вызывает улучшение снабжения тканей кислородом.
При кетоацидотической коме наблюдается обратный процесс.
Осложняющий ее течение декомпенсированный метаболический ацидоз нарушает образование 2,3-ДФГ в эритроцитах, вследствие чего сродство гемоглобина к кислороду возрастает, и нарушаются условия его отдачи на тканевом уровне.
В консервированной крови, особенно с длительным сроком хранения, уровень 2, 3-ДФГ снижается, поэтому при ее переливании нарушается отдача кислорода тканям.
Следовательно, смещение КДО является важнейшим физиологическим процессом, обеспечивающим транспорт кислорода в организме.
К факторам, приводящим к возрастанию сродства Нb к О2 и смещению КДО влево при падении Р50, относятся:
— увеличение рН;
— уменьшение рСО2;
— уменьшение концентрации 2,3-ДФГ и неорганического фосфата;
— снижение температуры тела;
— алкалоз.
С другой стороны, уменьшение рН, увеличение рСО2, концентрации 2,3-ДФГ и неорганического фосфата, а также повышение температуры и ацидоз приводят к уменьшению сродства Нb к О2 и смещению КДО вправо при возрастании Р50.
Потребление кислорода, кроме функционального состояния гемоглобина, в определенной мере отражает компенсаторную роль гемодинамики.
Увеличение минутного объема кровообращения (МОК) может компенсировать недостаток кислорода в крови.
Транспорт углекислого газа (СО2)
Конечным продуктом аэробного гликолиза является углекислый газ.
Он образуется в клетках и реагирует с водой, в результате чего получается угольная кислота, которая, в свою очередь, диссоциирует на ионы водорода и НСО3-.
Эта реакция происходит во всех водных секторах и эритроцитах.
Катализирует ее карбоангидраза.
Далее углекислота диффундирует через клеточные мембраны и попадает в венозную кровь.
В состоянии покоя за 1 мин. в тканях образуется и выделяется легкими примерно 180 мл СО2.
Данную величину легко рассчитать.
Ввиду того, что дыхательный коэффициент (ДК — отношение количества выведенной углекислоты к количеству поглощенного кислорода) в норме составляет 0,85, при поглощении организмом за одну мин. 250 мл О2 должно будет выделиться 210 мл СО2.
Каковы механизмы выведения углекислого газа из организма?
Часть углекислого газа физически растворена в плазме крови.
Хотя растворимость СО2 в плазме в 40 раз выше растворимости О2, тем не менее, небольшая артериовенозная разница по парциальному напряжению углекислого газа между венозной и артериальной кровью делает возможным перенос физически растворенного газа не более 6—7% от его суммарного количества.
Примерно 3—10% углекислого газа из тканей к легким транспортируется в виде карбаминовой формы.
Что это такое?
Рядом исследований было доказано, что СО2 может присоединяться к гемоглобину посредством карбаминовой связи, образуя карбогемоглобин (синоним — карбаминогемоглобин).
Данное соединение химически очень нестойко и в системе легочных капилляров легко диссоциирует с отщеплением СО2.
Основное количество углекислого газа (более 80%) транспортируется из тканей к легким в форме бикарбоната, важнейшая роль в этом механизме принадлежит гемоглобину и его способности к процессам оксигенации и деоксигенации.
Оксигенированный гемоглобин (НbО2) является более сильной кислотой, чем деоксигенированный, благодаря этому обеспечивается связывание СО2 в тканевых капиллярах и освобождение его в легочных.
 2015-01-13
2015-01-13 2779
2779








