Диффузией называется самопроизвольный процесс перемещения вещества в растворе, приводящий к выравниванию его концентрации.
В ходе диффузии некоторая первоначальная упорядоченность в распределении вещества (высокая концентрация вещества в одной части системы и низкая – в другой) сменяется полной беспорядоченностью распределения вещества в объеме, при этом энтропия системы возрастает. Когда концентрация раствора во всем объеме выравнивается, энтропия достигает максимального значения, и диффузия прекращается. Скорость диффузии при постоянных температуре и вязкости среды зависит от величины и формы растворяющихся частиц.
Диффузия наблюдается как в жидкостях и газах, так и в твердых веществах. Мерой диффузии является масса вещества 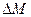 , продиффундировавшего за единицу времени через единицу площади поверхности соприкасающихся веществ. Величина
, продиффундировавшего за единицу времени через единицу площади поверхности соприкасающихся веществ. Величина 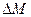 тем больше, чем больше изменяется концентрация на единицу длины вдоль направления, в котором происходит диффузия. Скорость диффузии увеличивается с ростом температуры, что связано с увеличением скорости движения частиц.
тем больше, чем больше изменяется концентрация на единицу длины вдоль направления, в котором происходит диффузия. Скорость диффузии увеличивается с ростом температуры, что связано с увеличением скорости движения частиц.
При гетерогенном катализе химическая реакция протекает на поверхности твердого тела, поэтому процессы транспорта веществ к поверхности и от нее играют важную роль. Если химическое превращение идет гораздо медленнее процессов массообмена, то кинетика реакции определяется процессами на поверхности твердого тела. Если реакция очень быстрая, то кинетика зависит от процессов массообмена.
Рассмотрим диффузию вещества из объема на поверхность реагирующих веществ или на поверхность катализатора, если таковой имеется. Пусть превращение вещества – реакция первого порядка со скоростью, равной
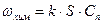 (46)
(46)
где ωхим – количество вещества, реагирующего у поверхности S в единицу времени, Сп – концентрация реагента у поверхности.
В результате превращения Сп становится меньше концентрации вещества в объеме раствора Соб.
Всю реагирующую смесь можно разделить на две области:
1. область постоянной концентрации вдали от поверхности реакции;
2. область быстрого изменения концентрации непосредственно вблизи этой поверхности.
Экспериментально установлено, что на всех твердых поверхностях, с которыми граничит движущаяся жидкость, скорость движения жидкости равна нулю. Транспорт вещества происходит через неподвижный слой жидкости, прилегающий к поверхности твердого тела, в результате диффузии реагирующих веществ. Этот неподвижный слой называется слоем Нернста, его толщина зависит от свойств растворителя и растворенного вещества, скорости перемещения и т.д. Например, для жидкости толщина этого слоя δ составляет примерно 0.02 – 0.05 мм и меньше. За его пределами движение жидкости приводит к выравниванию концентрации в объеме раствора. Перенос массы в результате диффузии описывается уравнением Фика:
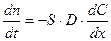 (47)
(47)
где dn/dt – количество вещества, диффундирующего за единицу времени через фиксированную поверхность S в сторону возрастающих значений x; x – направление диффузии; D – коэффициент диффузии; знак «-» означает, что поток вещества идет в направлении убыли концентрации, поэтому для 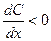 всегда
всегда 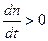 .
.
Существует и другая запись уравнения диффузии при Т = Const:
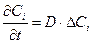 (48)
(48)
Градиент концентрации (gradC) в диффузионном слое постоянен, поэтому выражение (47) можно записать следующим образом:
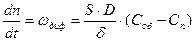 (49)
(49)
Когда в установившемся стационарном режиме скорость подвода вещества к реагирующей поверхности равна скорости химической реакции, поверхностную концентрацию можно представить как:
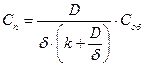 (50)
(50)
при wy = wxи
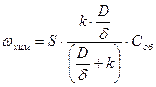 (51)
(51)
Для быстрой реакции, когда k>>D/d скорость процесса определяется диффузией. В случае медленной реакции, когда k<<D/d, то скорость процесса определяется скоростью химической реакции. Можно вывести формулу для эффективной константы скорости процесса:
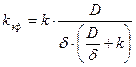 (52)
(52)
Интенсивное перемешивание раствора снижает толщину диффузионного слоя, что приводит к увеличению константы скорости диффузии. Так как константа скорости химической реакции в большей степени зависит от температуры, нежели коэффициент диффузии, то при низкой температуре процесс лимитируется скоростью химической реакции.
Моделирование гетерогенно-каталитических реакций.
Обычно гетерогенно-каталитические процессы протекают в жидкой, газовой или паровой фазе при участии твердого катализатора. В случае газовой гетерогенно-каталитической реакции исходные реагенты и продукты реакции являются газами. При их участии в реакции каждая молекула реагента последовательно проходит следующие стадии процесса:
- диффузионный перенос из газовой среды к поверхности катализатора;
- адсорбцию на его поверхности;
- химическое превращение в адсорбированном слое;
- десорбцию продуктов реакции;
- диффузионный перенос продуктов реакции от поверхности катализатора в газовую фазу.
На скорость гетерогенно-каталитической реакции большое влияние оказывает площадь активной поверхности твердого катализатора. Для ее увеличения катализаторы обычно выполняют в виде зерен с сильно развитой поверхностью. При этом кажущаяся поверхность зерен ничтожна по сравнению с поверхностью внутренних пор и каналов в зерне. Значения длины и диаметра внутренних каналов и пор должны исключать сильное торможение диффузионно-транспортных стадий процесса. Наиболее выгоден режим, при котором лимитирующей стадией процесса является собственно химическое превращение. В этом случае говорят, что процесс идет в кинетической области, однако, не всегда удается устранить диффузионное торможение.
Обычно скорость химической реакции определяется по уравнению (47). Если гетерогенная каталитическая реакция является многокомпонентной, кинетическая формула может оказаться достаточно громоздкой. Рассмотрим кинетические уравнения, выведенные из предположения об ограниченной активности поверхности катализатора. Предполагается, что химическое превращение может происходить только на участках молекул, попавших за счет адсорбции на активный центр катализатора.
Сорбцией называется любой процесс поглощения одного вещества другим независимо от механизма поглощения. В зависимости от механизма сорбции различают:
- адсорбцию – изменение концентрации вещества на границе раздела фаз. Адсорбция происходит на любых межфазовых поверхностях, и адсорбироваться могут любые вещества. Адсорбционное равновесие, т.е. равновесное распределение вещества между пограничным слоем и граничащими фазами, является динамическим равновесием и быстро устанавливается. Адсорбция с повышением температуры уменьшается;
- абсорбцию – поглощение одного вещества другим происходит во всем объеме сорбента (например, растворение газа в жидкостях);
- хемосорбцию – поглощение одного вещества другим сопровождается химическими реакциями;
- капиллярную конденсацию – происходящую вследствие того, что давление паров над вогнутым мениском жидкости в смачиваемых ею узких капиллярах меньше давления насыщенного пара над плоской поверхностью жидкости при той же температуре.
Положительная адсорбция, приводящая к повышению концентрации вещества в пограничном слое, возможна только при уменьшении величины поверхностного натяжения, т.е. все самопроизвольные процессы на границе раздела фаз происходят в направлениях уменьшения свободной поверхностной энергии.
Статическая сорбция наблюдается в том случае, когда поглощаемое вещество контактирует с неподвижным сорбентом. Статическая активность сорбента характеризуется количеством поглощаемого вещества на единицу массы сорбента в определенных условиях.
Динамическая сорбция наблюдается при фильтрации поглощаемого вещества через слой сорбента.
В случае гетерогенно-каталитических реакций считается, что число активных центров на единицу поверхности катализатора ограниченно. Кроме того, для упрощения считается, что каждый активный центр может удержать лишь определенное количество молекул или атомов реагирующего вещества (чаще всего одну). При таких предположениях скорость химического превращения оказывается пропорциональной концентрациям реагирующих веществ, адсорбированным на поверхности катализатора, т.е. поверхностным концентрациям. Для описания зависимости поверхностной концентрации некоторого вещества от его концентрации в объеме окружающего газа используется уравнение изотермы адсорбции Ленгмюра. Для упрощения принимают условия равновесия адсорбции и десорбции. Скорость адсорбции ra (или uадс) некоторого компонента можно принять пропорциональной его давлению Р и концентрации свободных активных центров, определяемой как разность между полной концентрацией активных центров Са и концентрацией занятых центров С:
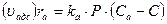 (53)
(53)
Скорость десорбции rд (uдес) пропорциональна концентрации занятых активных центров С:
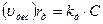 (54)
(54)
Предполагая равновесие между адсорбцией и десорбцией, т.е. приняв rа = rд (uадс = uдес) получим:
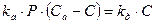 (55)
(55)
Следовательно, концентрация занятых активных центров равна:
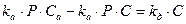
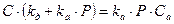
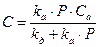
введем замену 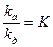 -константа равновесия адсорбции (56)
-константа равновесия адсорбции (56)
В случае равенства kа = kдесK=1, тогда получим:
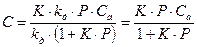 (57)
(57)
На рис.3 приведен пример изотермы адсорбции.
Адсорбция газов и паров на поверхности твердых тел также происходит в результате уменьшения свободной поверхностной энергии. На практике об адсорбции судят по количеству адсорбированного вещества, которое тем больше, чем больше поверхностный слой адсорбента, соответственно. Поэтому, для осуществления адсорбционных процессов необходимо использовать адсорбенты с высокоразвитой поверхностью. Важнейшими пористыми сорбентами являются активированный уголь и селикагель.
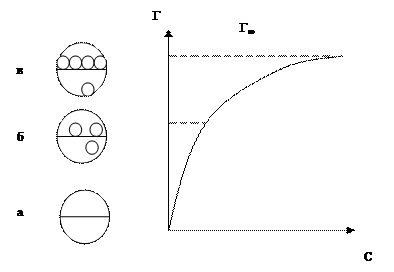
Рис. 3 Изотерма адсорбции.
Г – поверхностный избыток
а – чистый компонент
б – ненасыщенный мономолекулярный (в одну молекулу толщиной слой)
в – насыщенный мономолекулярный слой
Повышение температуры и понижение давления приводят к десорбции газов и паров. Вследствие этого сорбционные методы широкого использования в промышленности для извлечения различных веществ из воздушной среды и для разделения газов и паров.
Адсорбция растворенных веществ из растворов на твердых сорбентах всегда в большей или меньшей степени включает в себя адсорбцию растворителя. Изотермы адсорбции из растворов имеют вид, аналогичный изотермам адсорбции из газовой фазы.
В практике моделирования гетерогенно-каталитческих процессов вместо поверхностных концентраций активных центров используют относительные концентрации 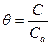 , называемые обычно степенью заполнения активных центров. Уравнение (57) можно переписать, заменив в нем концентрации на степень заполнения активных центров:
, называемые обычно степенью заполнения активных центров. Уравнение (57) можно переписать, заменив в нем концентрации на степень заполнения активных центров:
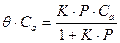 (58)
(58)
Если процесс адсорбции сопровождается обратимой диссоциацией на n частиц, то скорости адсорбции и десорбции являются функциями n-степени от соответствующих концентраций:
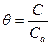 Þ
Þ 
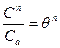 , тогда
, тогда
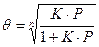 или же
или же
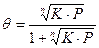 (59)
(59)
Если газовая фаза содержит несколько компонентов, адсорбируемых поверхностью катализатора, необходимо вычислить степень заполнения поверхности каждым компонентом.
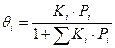 º
º 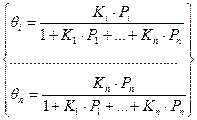
Необходимо учесть, что концентрация свободных мест определяется разностью между полной концентрацией активных центров и суммой центров, занятых всеми компонентами. Например, для двухкомпонентной системы:
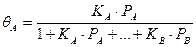 (60)
(60)
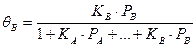 (61)
(61)
В случае диссоциации компонента А на две частицы получаем:
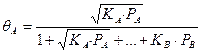 (62)
(62)
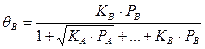 (63)
(63)
Если в газовой среде присутствует инертный компонент, не участвующий в химической реакции, но адсорбируемый поверхностью, в знаменатель выражений (59-63) соответствующее слагаемое, например:
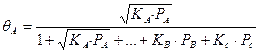 (64)
(64)
Так как скорость химического превращения пропорциональна поверхностным концентрациям реагирующих компонентов, т.е.
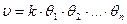 (65)
(65)
К примеру, для реакции типа А + В ® М при отсутствии диссоциации реагентов и без участия инертного компонента получается следующее выражение для скорости химического превращения:
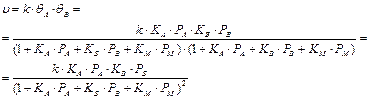 (66)
(66)
Степень в знаменателе выражения (66) равна количеству компонентов химической системы.
Если адсорбционные свойства компонентов реакции значительно разнятся, то вид уравнения Ленгмюра изменится. Пусть имеется реакция вида А ® Р, тогда
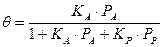
Рассмотрим различные варианты процесса:
1. Если реагирующий газ А адсорбируется слабо, а продукт реакции – умеренно, то 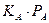 «
«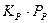 «1, то получим уравнение:
«1, то получим уравнение:
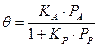
И тогда кинетическое уравнение примет вид:
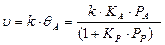
Произведение 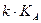 называется кажущейся константой скорости реакции.
называется кажущейся константой скорости реакции.
2. В случае сильной адсорбции реагирующего вещества и продукта реакции 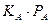 и
и 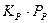 значительно больше единицы, тогда уравнение для скорости реакции запишется как:
значительно больше единицы, тогда уравнение для скорости реакции запишется как:
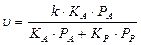
3. При слабой адсорбции реагирующего вещества и сильной адсорбции продукта реакции, 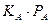 «1 и
«1 и 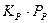 » 1, получим выражение:
» 1, получим выражение:
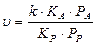
4. При сильной адсорбции реагента и слабой адсорбции продукта получаем выражение:
(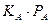 » 1 и
» 1 и 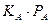 »
» 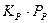 )
)
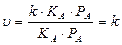
5. Если существует химическое взаимодействие адсорбированных молекул реагентов между собой (предположительно), то общий вид кинетического уравнения будет следующим:
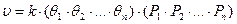 (67)
(67)
Для практических расчетов в ограниченной области режимных параметров часто используют аппроксимирующие степенные кинетические выражения:
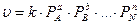 (68)
(68)
где a, b,…,n – частные порядки реакции.
К примеру, скорость окисления водорода до воды H2 + O2 → H2O на палладиевом катализаторе при малой концентрации может быть описана уравнением:
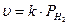 (69)
(69)
Надо добавить, что при моделировании в неизотермических условиях необходимо учитывать зависимость коэффициентов адсорбции и константы скорости от температуры. Что значительно усложняет модель.
Как видно, моделирование гетерогенных каталитических реакций – более сложный процесс по сравнению с моделированием гомогенных реакций, что связано с сильной нелинейностью получаемых уравнений.
 2015-01-21
2015-01-21 8449
8449
