Биофармация является теоретической основой технологии лекарств. Сам термин «биофармацня» появился впервые в научной формации США в начале 60-годов текущего столетия и вскоре получил международное признание. Этим коротким словом удачно и достаточно полно определен комплекс зависимостей, связывающий между собой лекарственное средство и лечебный (профилактический) эффект приготовленного лекарства.
Необходимый лечебный эффект достигается сложным путем, который должно пройти любое лекарственное вещество в организме. Упрощенно схему этого пути можно представить в следующем виде.

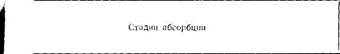 |
Факторы, влияющие на
скорость и полноту
абсорбции
 I. Лекарство (препарат в лекарственной форме) ^_ в месте введения (применения)
I. Лекарство (препарат в лекарственной форме) ^_ в месте введения (применения)
Фармацевтические
 II. Лекарственное вещество в биожидкости на ч_ месте абсорбции
II. Лекарственное вещество в биожидкости на ч_ месте абсорбции
Фармацевтические и физиологические
III. Лекарственное вещество (или метаболиты) в крови (или в тканях)
Физиологические и биохимические
IV. Элиминация продуктов биотрансформации ле
карственного вещества (почки, желудочно-ки- ■*-
шечпый тракт, легкие, потовые железы)___________
Биохимические
Первой стадией является путь введения лекарства — пероральный, ректальный, нанесение на кожу или слизистую оболочку, инъекционный и т. д. На этой стадии лекарственное вещество должно высвободиться из формы, в которую оно облечено (таблетки, суппозитории, мази, инъекции и др.) и продиффундировать (пройти путь) до назначенного места абсорбции (всасывания).
На второй стадии лекарственное вещество, перешедшее в биологическую жидкость, всасывается, подчиняясь законам диффузии. На кинетику диффузии оказывают влияние как фармацевтические, так и физиологические растворы. К числу первых нужно отнести влияние сопровождающих веществ, например поверхностно-активных, повышающих кинетику диффузии, а также.'влияние технологических факторов, например механической прочности таблеток на скорость растворения веществ, в них находящихся. Кинетика диффузии одновременно зависит от свойств и состояния клеточных мембран, ферментной активности клетки, ее гидратированности и др.
Важное значение для всасывания имеют несомненно такие физиологические факторы, как возраст, пол и состояние организма. Физиологическим факторам принадлежит основная роль на третьем этапе всасывания, когда лекарственное вещество или его метаболиты распределяются в организме — в кровяном русле или тканях.
На заключительном этапе движения лекарственного вещества в организме доминирующими являются биохимические факторы, обусловливающие биотрансформацию лекарственных веществ и их метаболитов и элиминацию ('выведение) конечных веществ нз организма через почки, желудочно-кишечный тракт, легкие, потовые железы.
Анализируя схему, нетрудно представить, что количественная сторона процесса абсорбции лекарственных веществ лимитируется прежде всего эффективностью (кинетикой) их высвобождения на начальной стадии абсорбции. Эффективность высвобождения лекарственных веществ находится в прямой зависимости от фармацевтических факторов п их последовательного использования для продвижения действующего вещества по схеме: 1) выбор химического состояния; 2) выбор физического состояния; 3) влияние вспомогательных веществ; 4) влияние одновременно принятых медикаментов; 5) выбор лекарственной формы; 6) выбор пути введения; 7) установление точной дозировки; 8) влияние фармакотехнологических факторов; 9) определение роли физиологических факторов, свойственных отдельным лицам.
Изучение влияния указанного комплекса факторов, способствующих транспорту лекарственных веществ в организме и проявлению их лечебной активности, является основным содержанием биофармации. Однако изучение фармацевтических факторов неразрывно связано с воздействием на продвижение лекарственных веществ в организме (начиная частично уже со второй стадии абсорбции) физиологических и биохимических факторов, которые изучаются другой близкой областью научных знаний — фармакокинетикой. Таким образом, полное представление о взаимосвязях между лекарственным веществом — лекарством и лечебным эффектом дает биофармация в сочетании с фармакокинетикой. Значение элементов фармакокинетики поможет технологу в оптимальном варианте применить знание биофармации для создания эффективного лекарства.
Исследования последних трех десятилетий, проведенные отечественными и зарубежными учеными с привлечением современных физико-химических, фармакологических и биохимических методов, позволили достаточно глубоко и достоверно разобраться в тех сложных взаимоотношениях, которые сложились между лекарством как особой физико-химической системой, и макроорганизмом как биологической системой тех факторов, которые обусловливают эти взаимоотношения.
Биофармацевтическим вопросам в нашей стране уделяется большое внимание. В каждом научно-исследовательском институте, где изыскиваются новые лекарственные средства, имеются специальные лаборатории технологии лекарственных форм, в задачу которых входит разработка для нового лекарственного препарата рациональной формы
его применения. Применение ни одного нового препарата не разрешается, если для него не предложена разумная лекарственная форма, если не решены вопросы по композиции основообразующих и других вспомогательных веществ, если не найдены наиболее совершенные методы производства лекарства.
В СССР создан Всесоюзный биофармацевтический центр (во ВНИИФ), в задачу которого входят координирование научных исследований по биофармации, апробация результатов исследований и методик, рекомендации по внедрению их в практику здравоохранения.
Значение физико-химических свойств и физического состояния лекарственных веществ
Первопричиной лечебной или профилактической активности любого лекарственного вещества является его химическое строение. Однако на лечебную активность лекарственного вещества оказывают существенное влияние и его вторичные свойства, вызванные направленным технологическим вмешательством при приготовлении из него лекарства (изменение степени дисперсности, форма частичек, растворимость и др.).
Полиморфизм. Первичные свойства самой лекарственной субстанции далеко не всегда одинаковы и постоянны. Это относится прежде всего к органическим веществам, которые могут существовать в двух и более кристаллических модификациях. Такое явление, называемое полиморфизмом лекарственных препаратов, особенно распространено среди салицилатов, барбитуратов, сульфамидов, гормональных препаратов. Например, ацетилсалициловая кислота встречается в шести кристаллических формах, кортизон-ацетат—в пяти и т. д. Получение той или иной кристаллической модификации обусловливается комплексом условий, при которых протекает синтез (или выделение из природного сырья), и в большей степени — от условий, в которых протекает кристаллизация субстанции (температурный фактор, природа растворителя, давление и т. д.).
Полиморфные модификации одного и того же препарата обладают различной растворимостью, температурой плавления, стойкостью к окислению и другим деструктивным процессам и т. д., а следовательно, неодинаковыми поверхностными свойствами, от которых зависит как скорость абсорбции лекарственных веществ, так и их стабильность в лекарственных формах.
Менее стабильные кристаллические модификации обычно более растворимы в биологических жидкостях и, следовательно, лучше всасываются. Например, одна из модификаций (метастабильная) растворяется в концентрации 1200 мг/л, а другая (стабильная) —только 60 мг/л.
Полиморфные превращения лекарственных веществ возможны не только лри их получении (выделении) очистке и сушке, но и при приготовлении лекарственных форм, а также в процессе хранения последних. В последнем случае полиморфные превращения зависят от условий и сроков хранения, а также от вида применяемых при изготовлении лекарственных форм вспомогательных веществ.
Химическое состояние. Одно и то же вещество может быть использовано в качестве лекарственного средства в разных химических состояниях. В простейших случаях это может касаться солеобразования того или иного активного вещества. Например, алкалоид хинин из основания может быть переведен в разные соли: сульфат, хлорид, бромид. Его растворимость будет равна соответственно 1: 800, 1:34,
1: 16. При сохранении основной функции хинина эти его соли как обладающие разной растворимостью будут иметь разную кинетику вса-сывания.
Еще более разителен следующий пример. При замене иона водорода в аскорбиновой кислоте на ион натрия препарат при сохранении основной функции витамина С приобретает новые, не характерные для аскорбиновой кислоты свойства — способность изменять электролитный баланс организма в большей степени, чем аскорбиновая кислота, угнетать функцию инсулярного аппарата у больных сахарным диабетом.
Продолжая примеры, можно напомнить, что производство буровской жидкости основывается на получении только однозамещенного ацетата алюминия, а не каких-либо других солей, поскольку антисептическое действие свойственно только этому соединению.
При переходе через липоидный барьер (стенка желудка, кишечника) большую роль играет степень ионизации. Препараты могут иметь кислый или щелочной характер. В зависимости от рН они могут быть в ионизированной или в неионизированной форме. Концентрация водородных ионов влияет также на растворимость, коэффициент распределения лекарственных веществ, а также на мембранный потенциал и поверхностную активность.
Дисперсность. Дисперсность частиц лекарственного вещества имеет не только технологическое значение, существенно влияя на сыпучесть порошкообразных материалов, насыпную массу, однородность смещения, точность дозирования и т. д. Особенно важным является то, что от размера частиц в большей степени зависят скорость и полнота всасывания лекарственного вещества при любых способах его назначения, исключая, конечно, внутрисосудистый. Таким образом, столь тривиальная технологическая операция, как измельчение, имеет непосредственное отношение к фармакотераневтическому эффекту лекарств.
Например, установлено, что при назначении сульфадимезина в виде порошка обычной степени измельчения и сверхтонкого измельчения (микроннзировашюго) в крови людей максимальная концентрация сульфаниламида достигается на 2 ч раньше в случае использования микронизированного препарата. При этом пиковые (максимальные) концентрации препарата оказываются на 40% выше, а общее количество всасывающегося сульфадимезина на 20% больше, чем при назначении порошка препарата обычной степени измельчения.
Солюбилизация. Многие вновь вводимые в лекарственный каталог вещества обладают плохой растворимостью в воде. Повысить их растворимость, а следовательно, ускорить резорбцию можно, использовав эффект солюбилизации. Солюбилизация является важным свойством растворов поверхностно-активных веществ, которое связано с их ми-целлярной структурой. В присутствии достаточных количеств поверхностно-активных веществ плохо растворимые и даже практически нерастворимые в воде органические лекарственные вещества приобретают способность коллоидно растворяться, или с о л ю б и-л а з и р о в а т ь с я. Па кафедре технологии лекарств Пятигорского фармацевтического института изучена возможность солюбилизации гидрокортизона и преднизолона и нитрофурановых производных с помощью водных растворов глицирама (моноаммонийная соль тритер-пенового сапонина глицирризиновой кислоты). Установлено, что 0,1% раствор глицирама повышает растворимость гидрокортизона и преднизолона более чем в 100 раз. При использовании 0,2% раствор глицирама в щелочной среде (1,6% NaHCO3) растворимость фурагина была повышена в 300 раз, а фурадонина — в 75 раз. В результате предложена новая водорастворимая лекарственная Форма фурагина.
 Изучалась также возможность получения водных растворов нерастворимых в воде препаратов — синтетических аналогов половых гормонов синэстрола, октэстрола, диэтилстилвбэстрола, диэтилстильбэст-рола пропионата, метилтестостерона. В качестве солюбилизатора использовались твин-80, глицирам, ОЭСШВ-35, ОЭЦС-20 и др. Результаты исследований свидетельствуют о том, что с помощью твина-80 можно повысить растворимость синэстрола в 31 раз, метилтестостерона— в 22 раза, диэтилстильбэстрола — в ПО раз.
Изучалась также возможность получения водных растворов нерастворимых в воде препаратов — синтетических аналогов половых гормонов синэстрола, октэстрола, диэтилстилвбэстрола, диэтилстильбэст-рола пропионата, метилтестостерона. В качестве солюбилизатора использовались твин-80, глицирам, ОЭСШВ-35, ОЭЦС-20 и др. Результаты исследований свидетельствуют о том, что с помощью твина-80 можно повысить растворимость синэстрола в 31 раз, метилтестостерона— в 22 раза, диэтилстильбэстрола — в ПО раз.
Солюбилизация противоопухолевых препаратов в 5% водных растворах индивидуальных и 5% бинарных водных смесях твина-80 ОП-71, ОП-10, глицирама и суммы сапонинов солодки щетинистой показала возможность получения солюбилизированных 0,5% водных растворов асалея, астирона и пальфицерина с использованием ОП-10, асалея и астирона — с твином-80. Растворимость веществ с 1:10 000 повысилась до 1: 200, т. е. в 50 раз.
Значение лекарственной формы
Лекарственное лечение неразрывно связано с вопросом выбора рациональной формы, в которой лекарственное вещество или комплекс веществ должны дать лечебный (или профилактический) эффект. Очевидно, что одновременно с расширением и изменением каталога лекарственных веществ и совершенствованием методов лечения расширялась номенклатура лекарственных форм и совершенствовалась их технология.
Очевидно, что чем большими преимуществами обладает та или иная лекарственная форма, тем большую ценность она представляет как структурная единица фармакотерапии и как промышленная единица. Лекарственная форма — это материальная форма проявления диалектического единства действующих и вспомогательных веществ и соответствующих технологических операций. Биофармация, обосновав научную трактовку лекарственной формы, требует тщательного исследования соответствия указанных компонентов (действующие и вспомогательные вещества, методы приготовления) в лекарственной форме для обеспечения оптимального действия препарата, иными словами, получения для нужд клиник наиболее рациональных лекарственных форм. В настоящее время не подлежит сомнению, что оптимальная активность лекарственного вещества достигается только назначением его в рациональной, научно обоснованной лекарственной форме.
Выбор лекарственной формы одновременно определяет и способ (путь) введения лекарства в организм. Совершенно очевидно, что скорость действия лекарственного вещества зависит от того, какой путь для его применения избран. Например, при ректальном способе лекарственное вещество может всосаться примерно через 7 мин, а при перо-ральном только через 30 мин (в среднем). Если же это вещество ввести внутривенно, то его действие проявится уже через 1—2 мин. Эффективность лекарственного вещества зависит от того, какой путь совершит лекарство до того, как оно попадает в кровь. При ректальном способе введения часть лекарственных веществ проникает в кровяное русло, минуя печень, и не подвергается химическому воздействию ее ферментов, а также желудочного сока, желчи и сока поджелудочной железы. Следовательно, сила воздействия лекарственного
 1 ОП-7 и ОП-10 — поверхностно-активные вещества, представляющие собой моно-или дналкилполнгликолевые эфиры с различным содержанием в молекуле звена (СН2—СН2О)„; у ОП-7 п = 7, у ОП-10 п=10.
1 ОП-7 и ОП-10 — поверхностно-активные вещества, представляющие собой моно-или дналкилполнгликолевые эфиры с различным содержанием в молекуле звена (СН2—СН2О)„; у ОП-7 п = 7, у ОП-10 п=10.
вещества в этом случае больше, чем при пероральном применении. При выборе пути введения учитывается также, какой характер действия ожидается от лекарственного вещества (преимущественно местное или общее, на весь организм). Все эти вопросы находят должное освещение при разборе элементов фармакокинетики.
При изучении введения цистамина гидрохлорида в организм в таблетках и суппозиториях оказалось, что препарат из суппозиториев всасывается быстрее и полнее, чем из таблеток. Было установлено, что через час после введения цистамина гидрохлорида животным из суппозиториев всасывается 85,3%, а из таблеток только 58% препарата.
Изучение биологической доступности пенных лекарственных форм препаратов солодкового корня (глицирам и др.) по сравнению с мазями на эмульсионных основах показало, что пенные аэрозоли позволяют ускорить процесс всасывания лекарственного препарата в 2—3 раза. Кроме того, препараты солодкового корня и их лекарственные формы способствуют более быстрому регрессу контактного дерматита и более выраженной тенденции к восстановлению функционального состояния кожи у животных. Препараты солодкового корня оказывают также более выраженное нормализующее влияние на метаболизм аскорбиновой кислоты и сульфгидрильных групп по сравнению с 0,5% прсднпзолоновой мазью и кремом Унны.
Значение вспомогательных веществ
С Онофармацевтической точки зрения изучение фармакологического действия любого лекарственного вещества бессмысленно, если оно не проводится в присутствии тех вспомогательных веществ, которые в дальнейшем будут составлять композицию конкретной лекарственной формы данного препарата.
Иначе говоря, вспомогательное вещество должно применяться не вообще, но конкретно с индивидуальным препаратом. Необоснованное применение вспомогательных веществ может привести к снижению, извращению или полной потере лечебного действия лекарственного вещества. Это происходит главным образом вследствие взаимодействия лекарственных и вспомогательных веществ при изготовлении лекарств в самой лекарственной форме или, чаще, после ее назначения больному. В основе подобных взаимодействий лежат преимущественно явления комплексообразования и адсорбции, способные резко изменить скорость и полноту всасывания действующих веществ.
Среди работ, посвященных изучению влияния вспомогательных веществ, особенно много внимания уделяется мазевым и суппозиторным основам. За последние десятилетия лечение мазями существенно изменились с введением в практику новых лекарственных средств, потребовавших новых мазевых основ. Большую часть последних стали составлять эмульсионные основы, применение которых обеспечивает более легкую диффузию лекарственных веществ в кожу и расширяет возможности введения лекарственных веществ как в масляную, так и в волную фазу. Значительное применение находят теперь также гидрофильные мазевые основы, хорошо переносимые больными и полно отдающие лекарственные вещества без нарушения перспирации кожи. Дифф\зшо лекарственных веществ усиливают добавками поверхностно-активных веществ, набор которых все расширяется.
Среди суппозиторных основ все большое распространение получают гидрогенизаты жирных масел, которые в сочетании с добавками поверхностно-активных веществ обеспечили не только необходимые для суппозиториев структурно-механические свойства, но и должную скорость высвобождения лекарственных веществ.
 Значение технологических факторов
Значение технологических факторов
Процесс превращении исходных лекарственных веществ (препаратов) в лекарство - это прежде всего технологический процесс. Вряд ли кто будет оспаривать тот факт, что способ получения лекарственных форм во многом определяет стабильность препарата, скорость его высвобождения нз лекарственной формы, интенсивность его всасывания и, в конечном итоге, его терапевтическую эффективность. Например, от избранного способа эмучьгировапня касторового масла зависит степень его дисперсности, а следовательно, и скорость омыления масла в щелочной среде кишечника и последующий послабляющий эффект.
Выбор способа гранулирования при получении таблеток обусловливается сохранностью многих лекарственных веществ в готовой лекарственной форме.
Значение технологических факторов особенно ярко проявилось в пролонгировании и дифференцированном проявлении лечебного эффекта. Это оказалось возможным в результате освоения техники изготовления многослойных таблеток и наложения на таблетки и драже покрытий разного назначения. Перспективными оказались проводимые на кафедре технологии лекарств Пятигорского фармацевтического института исследования по созданию лекарственных форм пролонгированного действия в виде спансул ■ (желатиновые капсулы, наполненные гранулами). Гранулы могут быть без покрытия (для немедленного всасывания и оказания начального эффекта), а также с покрытием различной толщины и растворимости. Разработка технологии этих гранул открывает широкие пути для сочетания лекарственных веществ и в других лекарственных формах (например, в таблетках).
Приведение примеров мы на этом ограничиваем, поскольку основная цель технологии лекарств — максимальное использование фармацевтических факторов для обеспечения высокого качества изготавливаемых лекарств1.
 2015-02-27
2015-02-27 992
992








