В различных веществах, а также в различных формах одного и того же вещества, энергетические зоны располагаются по-разному. По взаимному расположению этих зон вещества делят на три большие группы
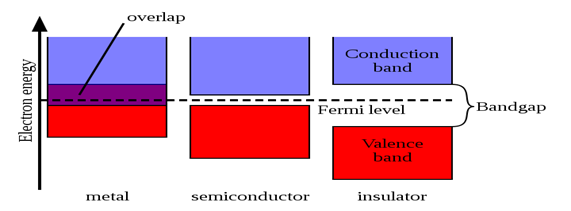
® Electron energy- энергетические зоны
® overlap- перекрытие
® conduction band-зона проводимости
® fermi level- уровень Ферми
® bandgap- ширина зазора
® valence band- валентная зона
® metal-металл
® semiconductor- полупроводник
® insulator-диэлектрик
- проводники — зона проводимости и валентная зона перекрываются, образуя одну зону, называемую зоной проводимости, таким образом, электрон может свободно перемещаться между ними, получив любую допустимо малую энергию. Таким образом, при приложении к телу разности потенциалов, электроны свободно движутся из точки с меньшим потенциалом в точку с большим, образуя электрический ток. К проводникам относят все металлы;
- полупроводники — зоны не перекрываются, и расстояние между ними (ширина запрещённой зоны) составляет менее 3,5 эВ. При абсолютном нуле температуры в зоне проводимости нет электронов, а валентная зона полностью заполнена электронами, которые не могут изменить свое квантомеханическое состояние, то есть не могут упорядоченно двигаться при приложении электрического поля. Поэтому при нулевой температуре собственные полупроводники не проводят электрический ток. При повышении температуры за счет теплового движения часть электронов, нарастающая при повышении температуры, «забрасывается» из валентной зоны в зону проводимости и собственный полупроводник становится электропроводным, причём его проводимость нарастает при увеличении температуры, так как растёт концентрация носителей заряда — электронов в зоне проводимости и дырок в валентной зоне. У полупроводников ширина запрещённой зоны относительно невелика, поэтому для перевода электронов из валентной зоны в зону проводимости требуется энергия меньшая, чем для диэлектрика, именно поэтому чистые (собственные, нелегированные) полупроводники обладают заметной проводимостью при ненулевой температуре;
- диэлектрики — зоны как и у полупроводников не перекрываются, и расстояние между ними составляет, условно, более 3,5 эВ. Таким образом, для того, чтобы перевести электрон из валентной зоны в зону проводимости требуется значительная энергия (температура), поэтому диэлектрики ток при невысоких температурах практически не проводят.
Разделение веществ на полупроводники и диэлектрики весьма условно, потому материалы с шириной запрещённой зоны более 3—4 эВ и менее 4—5 эВ иногда относят к широкозонным полупроводникам — материалам, совмещающим свойства и диэлектриков и полупроводников. К широкозонным полупроводникам относят алмаз (5—6 эВ), GaN (3,4 эВ), ZnS (3,56 эВ), ZnO (3,4 эВ). В то же время, к диэлектрикам обычно относят TiO2 (3,0 эВ), Та2О5 (4,4 эВ), Al2O3 (~7 эВ), SiO2 (~9 эВ), HfO2 (~5,4 эВ) и мн. др. При достаточно высоких температурах все диэлектрики приобретают полупроводниковый механизм электропроводности. Отнесение вещества к тому или иному классу больше зависит от способа использования или предмета изучения вещества тем или иным автором. Иногда, в классе полупроводников выделяют подкласс узкозонных полупроводников — с шириной запрещённой зоны менее 1 эВ.
Зонная теория является основой современной теории твёрдых тел. Она позволила понять природу и объяснить важнейшие свойства проводников, полупроводников и диэлектриков. Величина запрещённой зоны между зонами валентности и проводимости является ключевой величиной в зонной теории, она определяет оптические и электрические свойства материала.
Поскольку одним из основных механизмов передачи электрону энергии является тепловой, то проводимость полупроводников очень сильно зависит от температуры. Также проводимость можно увеличить, создав разрёшенный энергетический уровень в запрещённой зоне путём легирования. C помощью легирования создаются все полупроводниковые приборы: солнечные элементы (преобразователи света в электричество), диоды, транзисторы, твердотельные лазеры и другие.
Переход электрона из валентной зоны в зону проводимости называют процессом генерации носителей заряда (отрицательного — электрона, и положительного — дырки), обратный переход — процессом рекомбинации.
Вопрос 36. Теплопроводность многослойной плоской стенки.
Если с одной стороны многослойной стенки, состоящей из n слоев, поддерживается температура tв, а с другой стороны tн< tв, то возникает тепловой поток q, Вт/м2 (рис. 6).
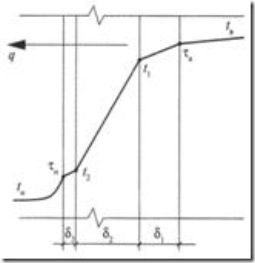
Рис.6. Распределение температуры при теплопередаче через многослойную стенк
Этот тепловой поток движется от среды с температурой tв, оС, к среде с температурой tн, оС, проходя последовательно от внутренней среды к внутренней поверхности с температурой τв, оС:
q= (1/ Rв).(tв - τв), (2.17)
затем от внутренней поверхности сквозь первый слой с термическим сопротивлением R Т,1 к стыку первого и второго слоев:
q= (1/ RТ,1).(τв- t1 ), (2.18)
после этого через все остальные слои
q= (1/ R Т,i).(ti-1 - ti ), (2.19)
и, наконец, от наружной поверхности с температурой τн к наружной среде с температурой tн:
q= (1/ R н).(τн- tн ), (2.20)
где R Т,i – термическое сопротивление слоя с номером i, м2.оС/Вт;
Rв, Rн – сопротивления теплообмену на внутренней и наружной поверхностях, м2.оС/Вт;
ti-1 - температура, оС, на стыке слоев с номерами i-1 и i;
ti - температура, оС, на стыке слоев с номерами i и i+1.
Переписав (2.16) – (2.19) относительно разностей температуры и сложив их, получим равенство:
tв- tн = q.(Rв+R Т,1+R Т,2+…+R Т,i+….+R Т,n+Rн) (2.21)
Выражение в скобках – сумма термических сопротивлений плоскопараллельных последовательно расположенных по ходу теплового потока слоев ограждения и сопротивлений теплообмену на его поверхностях называется общим сопротивлением теплопередаче ограждения Ro, м2.оС/Вт:
Ro=Rв+ΣR Т,i+Rн, (2.22)
а сумма термических сопротивлений отдельных слоев ограждения – его термическим сопротивлением RТ, м2.оС/Вт:
RТ = R Т,1+R Т,2+…+Rв.п+….+R Т,n, (2.23)
где R Т,1, R Т,2,…, R Т,n – термические сопротивления отдельных плоскопараллельных последовательно расположенных по ходу теплового потока слоев слоев ограждающей конструкции, м2.оС/Вт, определяемые по формуле (2.4);
Rв.п – термическое сопротивление замкнутой воздушной прослойки, м2.оС/Вт, по п. 2.1.4.
По физическому смыслу общее сопротивление теплопередаче ограждения Ro – это разность температуры сред по разные стороны ограждения, которая формирует проходящий через него тепловой поток плотностью 1 Вт/ м2, в то время как термическое сопротивление многослойной конструкции - разность температуры наружной и внутренней поверхностей ограждения, которая формирует проходящий через него тепловой поток плотностью 1 Вт/ м2,
Из (2.22) следует, что тепловой поток q, Вт/м2, проходящий через ограждение, пропорционален разности температуры сред по разные стороны ограждения (tв- tн) и обратно пропорционален общему сопротивлению теплопередаче Ro
q= (1/ Rо). (tв- tн), (2.24)
вопрос 37. Фазовые превращения. Переход из газообразного состояния в жидкое. Уравнение Клапейрона-Клаузиуса. Кристаллизация и плавление. Кристаллизация и сублимация. Фазовые диаграммы.
Любое вещество при определенных условиях может находиться в различных агрегатных состояниях – твердом, жидком и газообразном. Переход из одного состояния в другое называется фазовым переходом
Фа́зовый перехо́д (фазовое превращение) в термодинамике — переход вещества из одной термодинамической фазы в другую при изменении внешних условий. С точки зрения движения системы по фазовой диаграмме при изменении её интенсивных параметров (температуры, давления и т. п.), фазовый переход происходит, когда система пересекает линию, разделяющую две фазы. Поскольку разные термодинамические фазы описываются различными уравнениями состояния, всегда можно найти величину, которая скачкообразно меняется при фазовом переходе.
Наиболее часто рассматриваются фазовые переходы при изменении температуры, но при постоянном давлении (как правило равном 1 атмосфере). Именно поэтому часто употребляют термины «точка» (а не линия) фазового перехода, температура плавления и т. д. Разумеется, фазовый переход может происходить и при изменении давления, и при постоянных температуре и давлении, но и при изменении концентрации компонентов (например, появление кристалликов соли в растворе, который достиг насыщения).
ФАЗОВЫЕ ПЕРЕХОДЫ
Плавление — переход из твердого кристаллического состояния в жидкое.
Кристаллизация (затвердевание) — переход вещества из жидкого в кристаллическое (твердое) состояние.
Сублимация (возгонка) — переход из твердого кристаллического состояния в газообразное.
Конденсация — переход из газообразного состояния в жидкое или твердое.
Конденсация- происходит как при увеличении давления, так и при понижении температуры
Испарение — переход из жидкого состояния в газообразное.
Все реальные газы (кислород, азот, водород и т. д.) при определенных условиях способны превращаться в жидкость. Однако такое превращение может происходить только при температурах ниже определенной, так называемой критической температуры Tкр. Например, для воды критическая температура равна 647,3 К, для азота 126 К, для кислорода 154,3 К. При комнатной температуре (≈ 300 К) вода может находиться и в жидком, и в газообразном состояниях, а азот и кислород существуют только в виде газов.
С точки зрения молекулярно-кинетической теории, испарение – это процесс, при котором с поверхности жидкости вылетают наиболее быстрые молекулы, кинетическая энергия которых превышает энергию их связи с остальными молекулами жидкости. Это приводит к уменьшению средней кинетической энергии оставшихся молекул, т. е. к охлаждению жидкости (если нет подвода энергии от окружающих тел).
Конденсация– это процесс, обратный процессу испарения. При конденсации молекулы пара возвращаются в жидкость.
Нам также известно, что для перевода вещества из жидкого в газообразное состояние нужно затратить некоторую энергию. Эта энергия называется теплотой испарения или теплотой парообразования. Уравнение Клапейрона—Клаузиуса как раз и описывает отношение между теплотой испарения H, давлением пара p и температурой T вещества:
ln p = H/RT + константа
где ln p — натуральный логарифм, взятый от величины давления пара, а R — постоянная Ридберга. Температура T измеряется в кельвинах.
Первым эту зависимость в 1834 году вывел инженер-конструктор паровых машин Бенуа Клапейрон. Естественно, в силу его специальности, Клапейрона интересовала прежде всего теплота парообразования, и он использовал свое уравнение преимущественно в инженерно-прикладных целях. Для науки же уравнение теплоты фазового перехода было повторно открыто почти два десятилетия спустя Рудольфом Клаузиусом, автором формулировки второго начала термодинамики.
Чаще всего уравнение Клапейрона—Клаузиуса используется для простого расчета или измерения теплоты испарения различных веществ. Измеряя давление пара при различных температурах и нанося его на график, по одной оси которого откладывается значение lnp, а по другой — величина 1/Т, ученые по полученной линейной зависимости (углу наклона прямой) определяют теплоту испарения вещества.
Переход кристаллического тела в жидкое состояние происходит при определенной для каждого вещества температуре и требует затраты некоторого количества тепла, называемого теплотой плавления. Если веществу, первоначально находившемуся в кристаллическом состоянии, сообщать каждую секунду одно и то же количество тепла, то температура тела со временем будут меняться. Температура растет до значения Тпл температуры плавления, при дальнейшем подводе тепла температура перестает изменяться. Одновременно начинается процесс плавления твердого тела, в ходе которого все новые и новые порции вещества превращаются в жидкость. После того как процесс плавления будет закончен и все вещество полностью перейдет в жидкое состояние, температура снова начнет повышаться. Температура плавления зависит от давления. Таким образом, переход из кристаллического в жидкое состояние происходит при вполне определенных условиях, характеризуемых значениями давления и температуры.
Обратный плавлению процесс кристаллизации протекает следующим образом. При охлаждении жидкости до температуры, при которой твердая и жидкая фазы могут находиться в равновесии при данном давлении (т. е. до той же температуры, при которой происходило плавление), начинается одновременный рост кристалликов вокруг так называемых зародышей или центров кристаллизации. Разрастаясь все более, отдельные кристаллики в конце концов смыкаются друг с другом, образуя поликристаллическое твердое тело.
Центрами кристаллизации могут служить взвешенные в жидкости твердые частицы. Тщательно очищенную от таких частиц жидкость можно охладить ниже температуры кристаллизации без того, чтобы началось образование кристалликов. Состояние такой переохлажденной жидкости является метастабильным. Обычно достаточно попасть в такую жидкость пылинке, для того чтобы она распалась на жидкость и кристаллы, находящиеся при равновесной температуре. Однако в некоторых случаях при больших переохлаждениях подвижность молекул жидкости оказывается столь незначительной, что метастабильное состояние может сохраняться очень долго. Жидкость в таких случаях обладает весьма малой текучестью и представляет собой аморфное твердое тело.
Процесс кристаллизации сопровождается выделением такого же количества тепла, которое поглощается при плавлении.
Как в жидкостях, так и в твердых телах всегда имеется некоторое число молекул, энергия которых достаточна для преодоления притяжения к другим молекулам и которые способны оторваться от поверхности жидкости или твердого тела и перейти в окружающее их пространство. Этот процесс для жидкости называется испарением (или парообразованием), для твердых тел — сублимацией (или возгонкой). Для большинства твердых тел процесс сублимации при обычных температурах незначителен и давление пара над поверхностью твердого тела мало; оно повышается с повышением температуры. Интенсивно сублимируют такие вещества, как нафталин, камфора, что обнаруживается по резкому, свойственному им запаху. Особенно интенсивно сублимация происходит в вакууме — этим пользуются для изготовления зеркал. Известный пример сублимации — превращение льда в пар — мокрое белье высыхает на морозе.
фазовая диаграмма иначе диаграмма состояния (англ. phase diagram) — графическое изображение состояний термодинамической системы в пространстве основных параметров состояния — температуры T, давления p и состава x.
Описание
Фазовые диаграммы позволяют узнать, какие фазы (т. е. однородные подсистемы, отличающиеся строением и/или свойствами от других) могут присутствовать в данной системе при данных условиях и составе. Для сложных систем, состоящих из многих фаз и компонентов, построение диаграмм состояния по экспериментальным данным и данным термодинамического моделирования является важнейшим способом предсказания поведения в ходе различных процессов. Анализ относительного расположения полей, разделяющих их поверхностей и линий, а также точек сочленения последних позволяет однозначно и наглядно определять условия фазовых равновесий, появления в системе новых фаз и химических соединений, образования и распада жидких и твердых растворов и т. п.
Диаграммы состояния используют в материаловедении, металлургии, нефтепереработке, химической технологии (в частности, при разработке методов разделения веществ), производствах электронной техники и микроэлектроники и др. С их помощью подбирают условия промышленного синтеза веществ, определяют направленность процессов, связанных с фазовыми переходами, осуществляют выбор режимов термообработки, отыскивают оптимальные составы фаз и т. п.
Фазовые диаграммы однокомпонентных систем изображаются на плоскости в координатах p–T. На них присутствуют поля, отвечающие существованию той или иной фазы вещества (газообразной, жидкой, различных твердых модификаций), разделенные линиями фазового равновесия, вдоль которых возможно сосуществование граничащих фаз. Места, где сходятся три различные линии фазовых равновесий, образуют так называемые тройные точки, в которых могут сосуществовать три фазы. Это максимальное число фаз, способных равновесно сосуществовать в однокомпонентных системах.
вопрос 38. Возникновение электродинамики.
К концу XVIII века в активе физики электромагнитных явлений были уже теория атмосферного электричества Франклина и закон Кулона. Стараниями Гаусса и Грина электростатика была в основном разработана. Для опытов использовали электризацию трением, лейденскую банку и электростатическую машину, изобретённую в 1775 году Алессандро Вольта.
Новый мощный источник электричества был случайно открыт врачом Луиджи Гальвани и описан им в трактате, изданном в 1791 году; он заметил, что при контакте лапки лягушки с двумя разнородными металлами происходят судороги мышц. Гальвани дал этому явлению ошибочное объяснение («животное электричество»). Правильное объяснение дал Вольта: при контакте некоторых разнородных металлов с электролитом возникает электродвижущая сила.
В 1800 году Вольта собрал первый «вольтов столб», при помощи которого исследовал ток в замкнутых цепях. Опубликование письма Вольты президенту Лондонского Королевского общества Бэнксу произвело сенсацию; Наполеон пригласил Вольту в Париж, лично присутствовал на демонстрации опыта, осыпал наградами и почестями.
Благодаря этим первым батареям постоянного тока были сделаны два выдающихся открытия:
- электролиз: в том же 1800 году Никольсон и Карлайл разложили воду на водород и кислород, а Дэви в 1807 году открыл металлический калий.
- электрическая дуга 1802: В. В. Петров и Дэви.
Но главные сенсационные события начались в 1820 году, когда Эрстед обнаружил на опыте отклоняющее действие тока на магнитную стрелку. Первые теории, связывающие электричество и магнетизм, построили в том же году Био, Савар и позже Лаплас (см. Закон Био — Савара — Лапласа).
Незамедлительно последовал новый каскад открытий:
- первый электродвигатель (1821, Фарадей)
- термоэлемент (1821, Зеебек)
- закон Ома (1827).
Ампер предложил термин «электродинамика» и в 1826 году издал монографию «Теория электродинамических явлений, выведенная исключительно из опыта». Он открыл электромагнит (соленоид), предсказал электрический телеграф (реализован Морзе в 1835 году). Формула Ампера для взаимодействия двух элементов тока вошла в учебники.
Силы, введенные Ампером, как и у Ньютона, считались дальнодействующими. Это положение решительно оспорил Майкл Фарадей, который в 1831 году открыл электромагнитную индукцию. В результате серии опытов он сформулировал (словесно) свойства электромагнитного поля, позже математически отражённые Максвеллом: изменение магнитного потока генерирует электродвижущую силу и вихревое электрическое поле.
Фарадей показал, что все известные тогда виды электричества тождественны, открыл законы электролиза, ввёл термины: ион, катод, анод, электролит, диамагнетизм, парамагнетизм и др. Фарадей отстаивал физическую реальность силовых линий; однако учёные того времени, уже свыкшиеся с дальнодействием ньютонового притяжения, теперь уже к близкодействию относились с недоверием.
В 1845 году Фарадей обнаружил поворот плоскости поляризации света в магнитном поле. Это означало, что свет и электромагнетизм тесно связаны.
Позже Фарадей исследовал самоиндукцию, открытую в 1832 году американским учёным Генри, свойства диэлектриков, разряды в газах и др.
1866: запущен трансатлантический электротелеграф.
1870-е годы: изобретен телефон.
1880-е годы: лампа накаливания.
вопрос 39. Физические процессы в проводниках и их свойства. Проводники I и II рода. Физическая природа электропроводности в металлах (классическая теория Друде-Лоренца).
1. Общие сведения о проводниках
Проводниками электрического тока могут служить твердые тела, жидкости, а при соответствующих условиях газы.
Твердыми проводниками являются металлы, металлические сплавы, некоторые модификации углерода. Среди металлических проводников различают материалы, обладающие высокой проводимостью и металлы и сплавы, обладающие высоким сопротивлением. К жидким проводникам относятся расплавленные металлы и различные электролиты (растворы кислот, щелочей, солей, расплавы ионных соединений).
Прохождение тока через электролиты связано с переносом вместе с электрическими зарядами частей молекул (ионов), в результате чего состав электролита постепенно изменяется, а на электродах выделяются продукты электролиза.
Все газы и пары, в том числе и пары металлов, при низких напряженностях электрического поля не являются проводниками. Однако при напряженности поля выше критического значения, газ может стать проводником, обладающим электронной и ионной электро-проводностью.
К проводникам относятся все металлы и их сплавы, а также электротехнический уголь(каменный уголь, графит, сажа, смола и т.д.)
К жидким проводникам относятся:вода, раствор солей, кислот и щелочей.
К газообразным относятся ионизированные газы.
Электрический ток в твердых проводниках-это направленное движение свободных электронов под действием ЭДС.
ЭДС-электронно-движущая сила.
 2015-02-18
2015-02-18 5402
5402
