Скорость химической реакции (V) прямо пропорциональна произведению молярных концентраций (С) реагирующих веществ в степенях, соответствующих их стехиометрическим коэффициентам (закон действия масс).
Для гомогенной реакции вида mA + nB = pC + qD
V = kс · CAm · CBn,
где kс – константа скорости. kс зависит от природы реагирующих веществ и температуры и не зависит от концентрации. V= kс при единичных концентрациях взаимодействующих веществ.
Для газовой системы 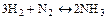 скорость прямой реакции можно записать двояко:
скорость прямой реакции можно записать двояко: 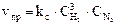 и
и 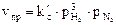 , где рН2 и рN2 – парциальные давления водорода и азота.
, где рН2 и рN2 – парциальные давления водорода и азота.
Выполнение опыта. В пробирку поместить 3 - 5 капель 1 н. раствора тиосульфата натрия Na2S2O3 и добавить 2 - 3 капли 2 н. раствора серной кислоты H2SO4.
Через некоторое время наблюдать помутнение раствора, вызванное выделением свободной серы. Реакция идет по уравнению:
Na2S2O3 + H2SO4 = Na2SO4 + SO2 + H2O + S¯.
Время, которое проходит от момента сливания растворов до появления заметного помутнения, характеризует скорость реакции.
Повторить опыт, используя большие количества реагентов. Для этого в три большие пробирки налить разбавленный (1:200) раствор Na2S2O3: в первую – 5 мл, во вторую – 10 мл, в третью – 15 мл. В первую пробирку добавить 10 мл воды, во вторую – 5 мл воды.
В три другие пробирки налить по 5 мл разбавленной (1:200) серной кислоты.
В пробирки с Na2S2O3 прилить при помешивании по 5 мл приготовленной H2SO4 и точно отметить (по секундной стрелке часов или секундомеру), через сколько секунд после приливания кислоты наблюдается образование мути в каждой пробирке.
Результаты записать в форме таблицы:
| Номер пробирки | Объем раствора Na2S2O3, мл | Объем раствора H2SO4, мл | Объем H2O, мл | Время появления мути t, с | v = 1/t |
Результаты опыта представить графически, отложив скорость реакции V = 1/t на оси ординат, а концентрации растворов – на оси абсцисс.
 2015-04-01
2015-04-01 2027
2027
