Практический тепловой баланс в общем случае определяется простым уравнением
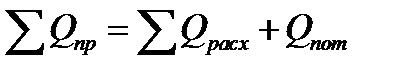
где Qпр - физическое тепло, вносимое в аппарат реагентами, материалом аппарата (для периодических процессов), тепло фазовых переходов, тепло реакции и т.д.; Qрасх - физическое тепло, уносимое из аппарата продуктами реакции;
Qпот - тепло, теряемое в окружающую среду.
При неизвестных размерах аппарата точное определение величин тепла, теряемого в окружающую среду, невозможно. В этом случае принимают Qпот равным 3-5% от максимального значения суммы вносимого или уносимого тепла. Если геометрические размеры аппарата известны, то можно оценить потери тепла по уравнению теплоотдачи
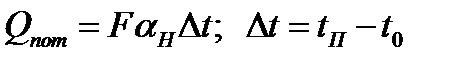
где Qпот - поток потерянного тепла, Вт; F - наружная поверхность теплообмена аппарата, м2; αн - наружный коэффициент теплоотдачи. Вт/(м2∙К); tП - температура наружной поверхности аппарата, 0С; t0 - температура окружающей среды, 0С.
Температура наружной поверхности аппарата либо определяется из санитар-
ных условий (<50°С), либо задается условиями работы аппарата. Температура ок-
ружающей среды выбирается минимальной для данного помещения или района (при установке оборудования на открытом воздухе). Наружный коэффициент теп-
лоотдачи рассчитывается по двум составляющим:
αн= αк + αл
где αк - коэффициент теплоотдачи конвекцией; αл - коэффициент теплоотдачи лучеиспусканием.
Конвективный коэффициент теплоотдачи зависит от места установки оборудования и от его положения в пространстве.
Горизонтальные трубопроводы и оборудование внутри помещений:
при ∆t∙d3 > 9,8∙10 -2 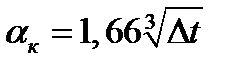
при 9,8∙10-2 ≥ ∆t∙d3>6,5∙10-6 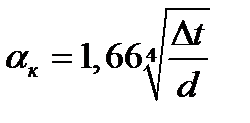
где d - наружный диаметр аппарата.
Для вертикальных аппаратов и трубопроводов внутри помещения:
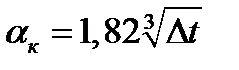 .
.
При установке оборудования на открытом воздухе:
для плоских стенок
αк = (5,95 + 1,5∙t0/100)(w0,6/l0,2)
где w - скорость ветра, м/с; l - длина стенки по направлению ветра, м;
для аппаратов αк = (5,1 + 0,3∙t0/100)(w0,6/d0,4)
для горизонтальных трубопроводов
αк = 3,9(w0,6/d0,4)
Коэффициент теплоотдачи лучеиспусканием (температура в К)
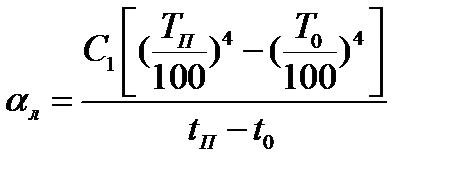
где С1 - степень черноты поверхности аппарата или трубопровода.
В случае расчета теплоизоляции аппарата или трубопровода, величина Q будет допустимой потерей тепла в окружающую среду. Тогда толщину слоя теплоизоляции можно рассчитать по формуле
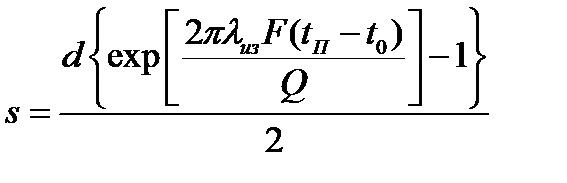
где λиз - коэффициент теплопроводности материала изоляции.
Пример 9.2. Определить температуру реакционной смеси процесса окисления метанола до формальдегида на входе в реактор, полагая температуру на выходе из реакционной зоны, равной 800 °С. Результаты материальных расчетов взять из примера 8.3. Теплоемкости компонентов реакции принять средними при температуре 650 °С.
Решение: Определим теплоемкости компонентов процесса. Из справочника выпишем стандартные энтальпии образования и температурные зависимости теплоемкостей всех веществ, участвующих в процессе (табл.9.1).
Таблица 9.1. Энтальпии образования и температурные
зависимости теплоемкости
| Компонент | ∆Н0, кДж/моль | Теплоемкость, Дж/(моль∙К) | |||
| а | b103 | с 106 | с' 105 | ||
| Кислород | 31,46 | 3,30 | - | -3,77 | |
| Азот | 27,87 | 4,27 | - | - | |
| СО | -110,5 | 28,41 | 4,10 | - | -0,46 |
| СО2 | -393,51 | 44,14 | 9,04 | - | -8,53 |
| Водород | 27,28 | 3,26 | - | 0,502 | |
| Вода | -241,84 | 30,00 | 10,71 | - | 0,33 |
| Метанол | -201,2 | 15,28 | 105,2 | -31,04 | - |
| Метан | -74,85 | 17,45 | 60,46 | 1,117 | - |
| СН2О | -115,9 | 18,82 | 58,38 | -15,61 | - |
| НСООН | -376,7 | 19,4 | 112,8 | -47,5 | - |
Для всех реакций процесса рассчитаем энтальпию реакции, кДж/моль
реакция (1) - 115,9 - 241,84 + 201,2 + 0,5 0 = -156,54;
реакция (2) - 115,9 - 0 + 201,2 = 85,3;
реакция (3) - 110,5 -2 0 + 201,2 = 126,35,
реакция (4) - 74,85 - 241,84 + 201,2 = -115,49;
реакция (5) - 376,7 - 241,84 + 115,9 = -502,64;
реакция (6) - 393,51 - 241,84+ 115,9 + 1,5 0 = 519,45.
Тогда уравнения реакций с термохимическим правилом знаков (тепловой
эффект в кДж/моль) примут вид:
СН3ОН + 0,5О2 = СН2О + Н2О + 156,54; (1)
СН3ОН = СН2О + Н2 - 85,3; (2)
СН3ОН = СО + 2Н2 - 126,35, (3)
СН3ОН + Н2 = СН4 + Н2О + 115,49; (4)
СН3ОН + О2 = НСООН + Н2О + 502,64; (5)
СН3ОН + 1,5О2 = СО2 + 2Н2О - 519,45. (6)
На основании материального баланса рассчитаем мольный расход метанола по каждой из реакций системы, а затем и количество выделяемого или поглощаемого тепла (см. табл. 9.2), откуда тепловой эффект процесса будет равен
604,8 кВт.
Составим тепловой баланс процесса окисления метанола, предварительно рассчитав теплоемкости компонентов при заданной температуре 650 °С по уравнениям
Ср =а + bТ + с'(1/T2); Ср=а + bТ + сТ2.
Таблица 9.2. К расчету суммарного теплового эффекта процесса
| Номер реакции | Расход метанола, кмоль/ч | Тепло реакции, кДж/моль | Расход тепла. кВт |
| (1) | 23,95 | 156,54 | |
| (2) | 16,75 | -85,3 | -397 |
| (3) | 0,154 | -126,35 | 5,4 |
| (4) | 0,456 | 115,49 | -14,6 |
| (5) | 2,75 | 502,64 | -384 |
| (6) | 2,45 | -519,45 | |
| Итого | 63,93 | 604,8 |
Данные расчета занесены в табл. 9.3.
Таблица 9.3. Средние теплоемкости компонентов реакции
| Компонент | Теплоемкость, Дж/(моль∙К) | Теплоемкость, Дж/(кг∙К) |
| Кислород | 31,46 | |
| Азот | 27,87 | |
| СО | 28,41 | |
| СО2 | 44,14 | |
| Водород | 27,28 | |
| Вода | 30,00 | |
| Метанол | 15,28 | |
| Метан | 17,45 | |
| СН2О | 18,82 | |
| НСООН | 19,4 |
Физическое тепло, вносимое компонентами в реактор, кВт:
с метанолом 1860∙2,44∙t/3600 = 1,2607∙t;
с кислородом 586∙1,05∙t/3600 = 0,1709∙t;
с азотом 1920∙1,12∙t/3600 = 0,5973∙t.
Всего на входе в реактор - 2,0289
Физическое тепло, уносимое компонентами из реакционной зоны, кВт:
с формальдегидом 1220∙1,82∙800/3600 = 493,4;
с метанолом 372∙2,44∙800/3600 = 201,7;
с водяным паром 572∙2,13∙800/3600 = 207,7;
с уксусной кислотой 126,5∙1,7∙800/3600 = 47,8;
с диоксидом углерода 108∙1,13∙800/3600 = 27,1;
с оксидом углерода 4,3∙1,13∙800/3600 = 1,1;
с метаном 7,3∙4,05∙800/3600 = 6,6;
с водородом 34,1∙14,5∙800/3600 = 109,9;
с азотом 1920∙1,12∙800/3600 = 477,9;
Всего на выходе - 1573,2.
Примем потери тепла в количестве 5% от его расхода. Составим уравнение теплового баланса, из которого определим температуру на входе в реактор:
2,0289∙t + 604,8 = 1573,2 + 0,05∙1573,2.
t= (1,05∙1573,2 - 604,8)/2,0289 = 516 °С.
Занесем результаты расчета в табл. 9.4.
Таблица 9.4. Тепловой баланс процесса получения формальдегида
| Приход тепла | Расход тепла | ||||
| кВт | % | кВт | % | ||
| Спирто-воздуш- ная смесь: | Формальдегид Метанол | 493,4 201,7 | 29,87 12,21 | ||
| метанол | 650,5 | 39,38 | Водяной пар | 207,7 | 12,57 |
| кислород | 88,2 | 5,34 | НСООН | 47,8 | 2,89 |
| азот | 308,2 | 18,66 | CO2 | 27,1 | 1,64 |
| Тепло реакции | 604,8 | 36,61 | CO | 1,1 | 0,07 |
| Ошибки округления | 0,2 | 0,01 | Метан Водород | 6,6 6,6 | 0,40 6,65 |
| Азот | 477,9 | 28,93 | |||
| Потери тепла | 78,7 | 4,77 | |||
| Итого | 1651,9 | Итого | 1651,9 |
Пример 9.3. Произвести тепловой расчет и составить тепловой баланс колонны синтеза аммиака в соответствии с исходными данными:
температура в зоне реакции t = 500 °С;
количество газовой смеси на входе в колонну V1 = 119025 нм3/ч;
температура газовой смеси на входе t1 = 35 °С;
количество газовой смеси на выходе из колонны V2 - 102329 нм3/ч;
температура газовой смеси на выходе t2 - 110 °С.
Состав газовой смеси, % (по объему):
На входе На выходе
Водород 74,1 62,06
Азот 24,7 20,7
Аммиак 1,2 17,24
Количество образующегося аммиака GNНз = 12500 кг/ч.
Рабочее давление в аппарате Pр = 30 МПа.
Температура воды: на входе 200 °С; на выходе 374 °С.
Решение: Составим уравнение теплового баланса
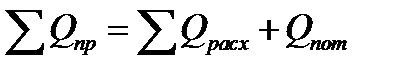
Приход тепла в колонну синтеза аммиака (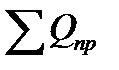 ).
).
1) С газовой смесью
Q1 = G1Cp1t1
где G1 - количество поступающей газовой смеси, кмоль/ч; Сρ1 - ее мольная теплоемкость, Сρ1 = 31,0 кДж/(кмоль∙К).
Откуда Q1 = 30,0∙35∙119025/ 22,4 3600 = 1550 кВт.
2) Тепловой эффект реакции синтеза аммиака при высоком давлении.
Определяется по уравнению
qp = 38332 + (2,281∙10-5 + 3,519∙10-2/T + 19240/T3)∙30 000 000 +
+ 22,38∙T +1,057∙10-3∙T2 - 7,087∙10-6∙T3
где qр - тепловой эффект реакции, кДж/кмоль; Ризб - избыточное давление в реакторе, Па; Т - температура, К.
В данном случае Т= 273 + 500 = 773 К; Р = 30∙106 Па.
Откуда
qp = 38332 + (2,281∙10-5 + 3,519∙10-2/773 + 19240/7733)∙30 000 000 +
+ 22,38∙773 +1,057∙10-3∙7732 - 7,087∙10-6∙7733 = 53000 кДж/кмоль.
Общее количество тепла, выделяющееся при синтезе аммиака, будет равно
Qp =qp∙GNH3/MNH3 = 53000∙12500/17,03∙3600 = 10 806 кВт
3) С охлаждающей водой на входе
QB1 = i'W,
где i' - энтальпия воды на входе при температуре 200 °С, равная 853 кДж/кг;
W - расход охлаждающей воды, кг/с.
QB1 = 853W
Общий приход тепла в колонну синтеза аммиака
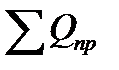 = 1550 + 10806 + 853W = 12356 + 853W, кВт.
= 1550 + 10806 + 853W = 12356 + 853W, кВт.
Расход тепла в колонне синтеза аммиака.
1) Расход тепла, уносимого с газовым потоком, равен
Qp = G2Cp2t2
где G2 - количество уходящей газовой смеси, кмоль/ч; Ср2 - ее мольная теплоемкость, Ср2 = 33,1 кДж/(кмоль∙К).
Q2 = 33,1∙110∙(102329/(22,4∙3600) = 4620 кВт.
2) Тепло, уносимое охлаждающей водой,
Qв2 =i"W,
где i" - энтальпия воды на выходе при температуре 374 °С; i" = 2100 кДж/кг
QB2 = 2100W.
3) Потери тепла в окружающую среду можно принять равными 5% от тепла, вносимого в колонну синтеза аммиака
Qпот = 0,05(12356 + 853 W) кВт.
Общий расход тепла
Qрас = 4620 + 2100W + 0,05 (12356 + 853W) = 5247 + 2143W кВт.
Уравнение теплового баланса
12356 + 853W = 5238 + 2143 W.
Pасход охлаждающей воды будет равен
W = 7118/1290 = 5,518 кг/с
Составим таблицу теплового баланса (табл. 9.5).
Таблица 9.5. Тепловой баланс колонны синтеза аммиака
| Приход тепла | Расход тепла | ||
| Статьи прихода | кВт | Статьи расхода | кВт |
| Газовая смесь Реакция синтеза Охлаждающая вода | 1550 10806 4706 | Газовая смесь Охлаждающая вода Потери тепла | 4620 11588 854 |
| Итого |
 2015-04-30
2015-04-30 2235
2235
