Пример 1. Вычислите молярную концентрацию, молярную концентрацию эквивалентов и моляльность CuSO4 в растворе CuSO4 с концентрацией w 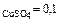 , плотность которого
, плотность которого 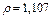 г/см3.
г/см3.
Решение. Найдем значение молярной массы и молярной массы эквивалентов CuSO4:
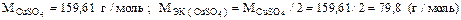 В 100г раствора с w
В 100г раствора с w 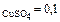 содержится 10г CuSO4 и 90г Н2O.
содержится 10г CuSO4 и 90г Н2O.
Следовательно, моляльность CuSO4 в растворе будет равна
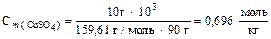 .
.
Найдём массу 1л раствора:
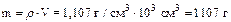 .
.
В этой массе раствора содержится
1107 г × 0,1=110,7 г СuSO4.
Следовательно, молярная концентрация CuSO4 в растворе будет равна
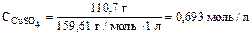 ,
,
а молярная концентрация эквивалентов CuSO4 в растворе составляет
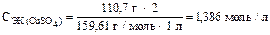 .
.
Примечание.
Можно использовать следующие сокращённые записи для обозначения состава данного раствора:
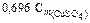 – означает, что в растворе на каждый килограмм воды как растворителя приходится 0,696 моль CuSO4.
– означает, что в растворе на каждый килограмм воды как растворителя приходится 0,696 моль CuSO4.
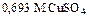 – означает, что в 1 л раствора содержится 0,693 моль CuSO4.
– означает, что в 1 л раствора содержится 0,693 моль CuSO4.
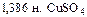 – означает, что в 1 л раствора содержится 1,386 моль эквивалентов CuSO4
– означает, что в 1 л раствора содержится 1,386 моль эквивалентов CuSO4
Пример 2. Какой объем воды нужно прибавить к 200 мл раствора NaOH с концентрацией wNaOH=0,3 и с плотностью 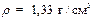 для получения раствора NaOH с концентрацией wNaOH=0,1.
для получения раствора NaOH с концентрацией wNaOH=0,1.
Решение. Масса 200 мл исходного раствора NaOH равна 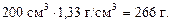
В этом растворе содержится 30 % NaOH, т.е. 266 г × 0,3=79,8 г.
По условию задачи эта масса составляет 10 % от общей массы разбавленного раствора. Тогда масса полученного раствора будет равна
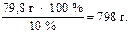
Следовательно, к исходному раствору нужно прибавить Н2O:
798 г–266 г=532 г.
Пример 3. Определите молярную концентрацию эквивалентов NaOH в растворе, если на нейтрализацию 0,035л 0,3н. раствора H3PO4 израсходовано 0,02л раствора NaОН.
Решение. Произведение молярной концентрации эквивалентов вещества В на объем раствора VР равно количеству эквивалентов этого вещества. Поэтому для реакции, в которой участвуют равные количества эквивалентов веществ А и В, можно записать: 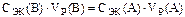 .
.
В нашем случае 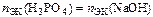 .
.
Следовательно, 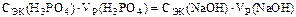 .
.
Находим СЭК(NaOH):
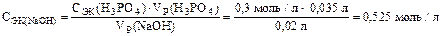
Пример 4. Какой объем раствора H2SO4 с концентрацией W 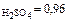 и с плотностью r=1,84 г/см3 потребуется для приготовления 3л 0,4н. раствора H2SO4?
и с плотностью r=1,84 г/см3 потребуется для приготовления 3л 0,4н. раствора H2SO4?
Решение. Молярная масса эквивалентов H2SO4 равна
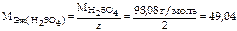 г/моль.
г/моль.
Для приготовления 3л 0,4н. раствора H2SO4 требуется H2SO4:
49,04 г/моль × 0,4 моль/л × 3 л=58,848 г.
Масса 1см3 раствора H2SO4 с концентрацией w 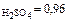 равна 1,84 г.
равна 1,84 г.
В этом растворе содержится 1,84 г × 0,96= 1,766 г H2SO4.
Отсюда для приготовления 3 л 0,4 н. раствора H2SO4 нужно взять
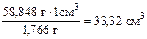 исходного раствора H2SO4.
исходного раствора H2SO4.
Контрольные вопросы
151. Сколько граммов Na2SO3 потребуется для приготовления 5л раствора с концентрацией w 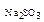 =0,08 и плотностью 1,075 г/см3? Ответ: 430 г.
=0,08 и плотностью 1,075 г/см3? Ответ: 430 г.
152. Из 400 г раствора H2SO4 с концентрацией w 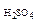 =0,5 выпариванием удалили 100 г воды. Чему равна массовая доля H2SO4 в оставшемся растворе? Ответ: 66,7 %.
=0,5 выпариванием удалили 100 г воды. Чему равна массовая доля H2SO4 в оставшемся растворе? Ответ: 66,7 %.
153. Сколько граммов раствора NaCl с концентрацией w 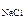 =0,3 нужно добавить к 300 г H2O, чтобы получить раствор с концентрацией w
=0,3 нужно добавить к 300 г H2O, чтобы получить раствор с концентрацией w 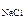 =0,1? Ответ:150 г.
=0,1? Ответ:150 г.
154. Сколько граммов HCl содержится в 0,25 л раствора HCl с концентрацией wHCl=0,1052 и с плотностью 1,05 г/см3? Ответ: 27,6 г.
155. Вычислите молярную концентрацию K2SO4 в растворе, если в 0.02 л этого раствора содержится 2,74 г растворенного K2SO4. Ответ: 0.786 моль/л.
156. Раствор KOH с концентрацией wKOH=0,26 имеет плотность 1.24 г/см3. Какое количество вещества KOH содержится в 5 л этого раствора? Ответ: 28,7 моль.
157. Водный раствор содержит 577 г H2SO4 в одном литре. Плотность раствора равна 1,335 г/см3. Вычислить массовую долю, молярную концентрацию, молярную концентрацию эквивалентов и моляльность H2SO4 в растворе. Ответ: 43,22 %; 5,88 моль/л; 11,76 моль/л; 7,76 моль/кг.
158. Плотность 0,8 М раствора Fe2(SO4)3 равна 1 г/см3. Определите молярную концентрацию эквивалентов, моляльность, массовую долю Fe2(SO4)3 в растворе. Чему равен титр этого раствора? Ответ: 4,8 моль/л; 1,18 моль/кг; 32 %; 0,32 г/мл.
159. Вычислите массовую долю и моляльность HNO3 в 8н. растворе HNO3 с плотностью 1,246 г/см3. Ответ: 40,45 %; 10,8 моль/кг.
160. Сколько граммов Na2CO3 содержится в 500 мл 0,25н. раствора? Ответ: 6,63 г.
161. Сколько литров 0,1н. раствора HNO3 можно приготовить из 0,07 л раствора HNO3 с концентрацией w 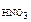 =0,3 и с плотностью 1,18 г/см3? Ответ: 3,93 л.
=0,3 и с плотностью 1,18 г/см3? Ответ: 3,93 л.
162. Из 5 л раствора KOH с концентрацией WKOH=0,5 и с плотностью 1,538 г/см3 надо приготовить раствор с концентрацией WKOH=0,18. Сколько литров H2O потребуется для этого? Ответ: 13,67 л.
163. Сколько литров 5н. раствора NaOH можно приготовить из 4 л раствора NaOH с концентрацией wNaOH=0,5 и с плотностью 1,525 г/см3? Ответ: 15,25 л.
164. Сколько миллилитров 0,5 М раствора H2SO4 можно приготовить из 15 мл 2,5 М раствора? Ответ: 75 мл.
165. В каком объеме 1 М раствора и в каком объеме 1н. раствора содержится 114 г Al2(SO4)3? Ответ: 0,333 л; 2 л.
166. Какой объем 6,0 М раствора HCl нужно взять для приготовления 25 мл 2,5 М раствора HCl? Ответ: 10,4 мл.
167. Сколько миллилитров концентрированной соляной кислоты с плотностью 1,19 г/см3 и с концентрацией wHCl=0,38 нужно для приготовления 1 л 2н. раствора? Ответ: 161,5 мл.
168. Сколько миллилитров раствора H2SO4 с концентрацией w 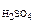 =0,1 и с плотностью 1,07 г/см3 потребуется для нейтрализации раствора, содержащего 16 г NaOH? Ответ: 183,2 мл.
=0,1 и с плотностью 1,07 г/см3 потребуется для нейтрализации раствора, содержащего 16 г NaOH? Ответ: 183,2 мл.
169. Какой объем 0,2н. раствора щелочи потребуется для осаждения в виде Fe(OH)3 всего железа, содержащегося в 100 мл 0,5н. раствора FeCl3? Ответ: 0,25 л.
170. Для нейтрализации 20 мл 0,1н. раствора кислоты потребовалось 8 мл раствора NaOH. Сколько граммов NaOH содержит 1 л этого раствора? Ответ: 10 г.
171. К 1 л раствора КОН с концентрацией wKOH=0,1 и с плотностью 1,092 г/см3 прибавили 0,5 л раствора КОН с концентрацией wKOH=0,05 и с плотностью 1,045 г/см3. Объем смеси довели до 2-х литров. Вычислите молярную концентрацию КОН в полученном растворе. Ответ: 1,2 моль/л.
172. На нейтрализацию 31 см3 0,16н. раствора щелочи требуется 217 см3 раствора H2SO4. Чему равны молярная концентрация эквивалентов H2SO4 в растворе и титр раствора H2SO4? Ответ: 0,023 моль/л; 1,12×10–3 г/мл.
173. Какой объем 0,3н. раствора кислоты требуется для нейтрализации раствора, содержащего 0,32 г NaOH в 40 см3? Ответ: 26,6 см3.
174. На нейтрализацию 40 мл раствора щелочи израсходовано 25 мл 0,5н. раствора H2SO4. Какова молярная концентрация эквивалентов щелочи в растворе? Какой объем 0,5н. раствора HCl потребовался бы для той же цели? Ответ: 0,3 моль/л; 24 мл.
175. Для осаждения в виде AgCl всего серебра, содержащегося в 100 см3 раствора AgNO3, потребовалось 50 см3 0,2н. раствора HCl. Какова молярная концентрация эквивалентов AgNO3 в растворе? Какая масса AgCl выпала в осадок? Ответ: 0,1 моль/л; 1,433 г.
 2015-05-14
2015-05-14 11777
11777
