Инфекционный эндокардит (ИЭ) — полипозно-язвенное поражение клапанного аппарата сердца или пристеночного эндокардита (реже эндотелия аорты или крупной артерии), вызванное различными патогенными микроорганизмами или грибами и сопровождающееся тромбоэмбо-лиями, а также системным поражением сосудов и внутренних органов на фоне измененной реактивности организма.
Термин «инфекционный эндокардит» в настоящее время вытеснил ранее использовавшиеся термины «бактериальный эндокардит», «затяжной септический эндокардит», так как лучше отражает причину заболевания, вызываемого самыми различными микроорганизмами — бактериальными агентами, риккетсиями, вирусами и грибами.
Наиболее часто заболевают ИЭ лица в возрасте 20 — 50 лет, несколько чаще мужчины, чем женщины. Однако особенностью «современного» ИЭ является высокая частота заболевания в пожилом и старческом возрасте (более 20 % всех случаев). Другая особенность ИЭ в настоящее время — увеличение числа больных с первичной формой болезни (более 50 %), появление новых клинических вариантов течения, значительное изменение характера возбудителя.
Этиология. Среди вызывающих ИЭ возбудителей наиболее часто встречается кокковая флора — стрептококки (зеленящий стрептококк ранее встречался в 90 % случаев), а также стафилококки (золотистый, белый), энтерококк. Значительно реже причиной болезни является грамотрицательная флора — кишечная палочка, синегнойная палочка, протей, клебсиелла. В последние годы важную роль стали играть патогенные грибы, протей, сарцины, бруцеллы, вирусы. У ряда больных истинный возбудитель заболевания не обнаруживается — частота отрицательного результата посева крови колеблется в пределах 20 — 50 %. Обнаружение возбудителя зависит от многих факторов: качества бактериологического исследования, длительности предшествующей антибактериальной терапии, характера возбудителя. Источники инфекции и бактериемии при ИЭ самые различные.
• Операции в полости рта.
• Операции и диагностические процедуры в мочеполовой сфере.
• «Малые» кожные инфекции.
• Оперативное вмешательство на сердечно-сосудистой системе (в том
числе протезирование клапанов).
• Длительное пребывание катетера в вене.
• Частые внутривенные вливания и эндоскопические методы исследо
вания.
• Хронический гемодиализ (артериовенозный шунт).
• Наркомания (внутривенное введение наркотиков).
ИЭ может развиться на интактных клапанах — так называемый первичный эндокардит, а также на фоне предсуществующих (врожденных и приобретенных) изменений сердца и его клапанного аппарата — так называемый вторичный ИЭ. К числу этих изменений можно отнести пороки сердца (врожденные и приобретенные), пролапс митрального клапана, ар-териовенозные аневризмы, постинфарктные аневризмы, шунты при хроническом гемодиализе, состояние после операции на сердце и крупных сосудах (включая протезирование клапанов, комиссуротомию, искусственные сосудистые шунты).
Патогенез. Механизм развития заболевания сложен и изучен недостаточно, однако основные моменты развития ИЭ не вызывают сомнения (схема 10). При наличии в организме очага инфекции под влиянием различных эндогенных и экзогенных факторов, изменяющих реактивность и имунный статус организма, развивается бактериемия.
Микроорганизмы из крови попадают на клапаны сердца, где создают в дальнейшем «вторичный» очаг инфекции. Фиксации и размножению микроорганизмов на эндокарде с формированием вторичного септического очага способствуют дополнительные факторы. По-видимому, имеют значение предшествующее изменение ткани и поверхности клапана, наличие на нем тромботических масс, возникающих под влиянием прямого повреждающего действия струи крови, движущейся с большой скоростью или под
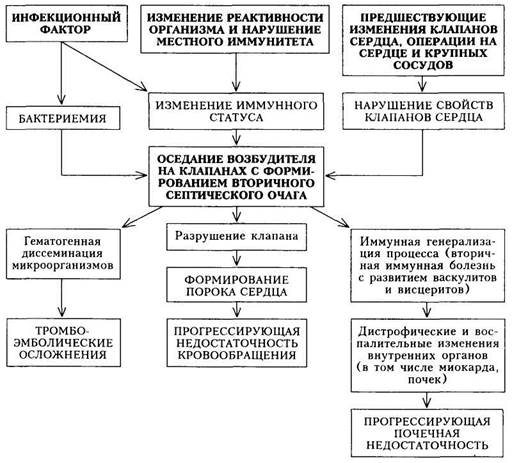 |
| Схема 10. Патогенез инфекционного эндокардита |
большим давлением (в условиях имеющегося порока сердца). Деформация клапанов вследствие возникновения большого градиента давления, узости отверстия и изменения скорости кровотока создает условия, способствующие внедрению инфекционных агентов в эндокард с образованием инфекционного очага.
При поражении ранее интактного клапана происходят изменения, нарушающие нормальные свойства отдельных участков этого клапана в виде отечности, экссудативных или пролиферативных процессов («интерстици-альный вальвулит» — доклиническая фаза). Подобная ситуация возможна и при повреждении интимы крупных сосудов.
В клинической картине заболевания принято выделять две группы симптомов, обусловленных различными патогенетическими механизмами.
Симптомы, спровоцированные инфекционно-токсическим воздействием, протекают с интоксикацией различной степени выраженности и с повышением температуры. Рост бактерий сопровождается формированием вегетации с разрушением клапанов (развитие порока сердца). Происходит также генерализация процесса за счет гематогенного распространения ин-
фекции. Отрыв кусочков клапанных микробных вегетации способствует заносу инфицированных эмболов в различные участки сосудистого русла и усугубляет септические проявления. Одновременно эмболы, попадая с током крови в различные органы, вызывают развитие тромбоэмболичес-ких осложнений, проявляющихся симптомами инфаркта почки, миокарда, селезенки, сосудов глаз, кожи и т.п.
Симптомы, обусловленные иммуновоспалительными механизмами, связаны с иммунной генерализацией процесса. Микроорганизмы, фиксированные на клапанах, вызывают длительную аутосенсибилизацию и ги-перергическое повреждение органов и тканей организма. В этой стадии выявляются циркулирующие в крови и фиксированные в тканях (сердце, почки, печень, сосуды) иммунные комплексы. Иммунные и аутоиммунные нарушения обусловливают развитие васкулитов и висцеритов (иммуно-комплексный нефрит, миокардит, гепатит, капиллярит и т.д.). В ряде случаев иммунные нарушения, называемые вторичными, могут развиваться с самого начала болезни, по существу в продромальный период.
При дальнейшем прогрессировании болезни могут развиваться дистрофические изменения органов с их функциональной недостаточностью (наибольшее значение имеют сердечная и почечная недостаточность, часто приводящая к смерти больных).
Классификация. В настоящее время отсутствует общепринятая классификация болезни. Тем не менее следует выделять клинико-морфологи-ческие формы (первичный, вторичный с указанием фона, на котором развился ИЭ), варианты течения (острый, подострый, затяжной), степень активности патологического процесса и функциональное состояние органов и систем.
Острый ИЭ (быстропрогрессирующий) встречается, как правило, у лиц, ранее не имевших поражения сердца, и клинически проявляется картиной общего сепсиса. Острый вариант ИЭ длится не более 1 — 1,5 мес, но при современных методах лечения иногда удается перевести его в подострый.
Подострый ИЭ обычно длится 3-4 мес, после чего (при проведении достаточно упорной терапии) может наступить ремиссия. В последующем возможны рецидивы болезни. Это наиболее частый вариант болезни.
Затяжной ИЭ длится многие месяцы с периодами обострения и ремиссий. При благоприятном течении клинические проявления неяркие, лабораторные показатели и нарушения общего состояния незначительные. Заболевание обычно вызывается маловирулентными возбудителями (чаще стрептококк) и обычно хорошо поддается лечению. Неблагоприятный вариант характеризуется вялым течением без ярких клинических проявлений, но с тяжелыми осложнениями и плохим прогнозом (больные погибают от прогрессирующей сердечной недостаточности, нарастающей септической интоксикации).
Клиническая картина. Проявления ИЭ весьма разнообразны и могут быть представлены в виде ряда синдромов.
• Синдром воспалительных изменений и септицемии (лихорадка, озноб, геморрагические высыпания, изменение острофазовых показателей крови: лейкоцитоз со сдвигом влево, увеличение СОЭ, появление СРВ, повышение содержания фибриногена, ссг-глобулинов, положительная гемокультура).
• Интоксикационный синдром (общая слабость, выраженная потли
вость, головные боли, миалгии и артралгии, снижение аппетита,
бледность кожных покровов с желтушным оттенком).
• Синдром клапанных поражений (формирование порока серд
ца, чаще аортального или митрального прежде не измененных
клапанов или присоединение этих пороков к ранее существовав
шим).
• Синдром «лабораторных» иммунных нарушений (наличие цирку
лирующих в крови иммунных комплексов, фиксированных иммуно-
комплексных депозитов в почках, миокарде, сосудах; гипергамма-
глобулинемия; появление ревматоидного фактора; выявление про-
тивотканевых антител).
• Синдром тромбоэмболических осложнений (очаговый нефрит, ин
фаркт миокарда, селезенки, кишечника, тромбоэмболии в мозг, сет
чатку глаза, сосуды нижних конечностей и т.д.).
• Синдром иммунных поражений органов и систем (диффузный гло-
мерулонефрит, миокардит, гепатит, васкулит и т.д.).
Степень выраженности указанных синдромов различна. Она определяется не только стадией, но и характером течения ИЭ, на который влияет вид возбудителя. Стафилококковый эндокардит характеризуется высокой активностью процесса, тяжелым общим состоянием, гектической лихорадкой, развитием гнойных осложнений. Грибковые эндокардиты, как правило, сопровождаются эмболической окклюзией крупных артерий, особенно нижних конечностей. Типичная картина заболевания характерна для ИЭ, вызванного зеленящим стрептококком.
На I этапе диагностического поиска жалобы обусловлены инфекцией и интоксикацией, тромбоэмболическими осложнениями, поражением сердца, вовлечением в патологический процесс других органов и систем.
Наиболее существенным для последующего диагноза следует считать одновременное наличие жалоб, указывающих на инфекционный процесс и поражение сердца.
В анамнезе обычно выявляются указания на перенесенный в прошлом ревматизм, наличие приобретенного или врожденного порока сердца, а также эпизоды «немотивированной» длительной лихорадки или субфебрилитета. Начало заболевания часто связано с острой инфекцией или обострением хронической инфекции, а также с рядом врачебных манипуляций (экстракция зубов, аборты, тонзиллэктомия, катетеризация мочевого пузыря, сосудов, операции на сердце и т.д.). Особенно характерно сочетание повышения температуры тела с ознобами и потливостью. Степень повышения температуры тела может быть различной: при остром течении отмечается повышение до 39 °С, тогда как при подостром и затяжном течении температура может быть субфебрильной. Вместе с тем у больных, длительно болеющих и имеющих сердечную или почечную недостаточность, при рецидивах болезни и несомненной активности процесса температура тела может быть нормальной.
Кроме того, можно выявить жалобы, обусловленные и сердечной недостаточностью (на фоне длительно существовавшего порока сердца), а также жалобы, связанные с тромбоэмболическими осложнениями (в особенности тромбоэмболии мелких мезентериальных сосудов, почечных артерий и селезенки).
В анамнезе больных могут быть эпизоды длительного лечения антибиотиками (это бывает при рецидиве ИЭ у больных, ранее уже подвергавшихся лечению).
В случае типичного течения болезни уже на этом этапе можно заподозрить ИЭ. У ряда больных на I этапе причина заболевания остается неясной и может быть установлена в дальнейшем лишь с учетом результатов последующих этапов диагностического поиска.
На II этапе диагностического поиска наибольшее значение для постановки правильного диагноза имеет обнаружение:
1) поражения клапанов сердца (появление патогномоничных для ИЭ
симптомов аортальной или митральной недостаточности; изменение аус-
культативной картины ранее существовавших пороков сердца; появление
«дополнительных» шумов);
2) поражения кожи и слизистых оболочек: цвет кожных покровов,
напоминающий «кофе с молоком», геморрагии, положительные симптомы
Гехта (щипка) и Кончаловского Румпеля Лееде (жгута), а также узел
ки Ослера — болезненные гиперемированные плотные узелки на ладон
ной поверхности и кончиках пальцев, признак Лукина —Либмана (пятна
Лукина) — геморрагия на переходной складке конъюнктивы. Весьма ти
пичным симптомом ИЭ является похудание, иногда значительное (на 15 —
20 кг);
3) увеличения селезенки и печени (спленомегалия часто наблюдается
при ИЭ и почти никогда при ревматизме).
Пальцы в виде барабанных палочек — симптом, не имеющий в настоящее время большого диагностического значения, так как он встречается чрезвычайно редко. Тем не менее наличие его — лишний довод в пользу постановки диагноза ИЭ.
При пороке сердца (в особенности при «вторичных» ИЭ) можно обнаружить признаки недостаточности кровообращения. Другая причина их появления — развитие миокардита, что проявляется глухостью сердечных тонов, систолическим шумом относительной недостаточности митрального клапана и дилатацией полостей.
В редких случаях развивается перикардит (нерезкий шум трения плевры, обусловленный фибринозными наложениями на перикарде).
При физикальном обследовании можно выявить повышение артериального давления, указывающее на развитие диффузного гломерулонеф-рита. У части больных определяются нарушения центральной нервной системы (ЦНС) (парезы, гиперкинезы, патологические рефлексы и т.д.) как проявление васкулитов или эмболии в мозговые сосуды. При исследовании органов дыхания можно выявить инфарктную пневмонию.
С учетом выявленных симптомов на этом этапе диагностического поиска диагноз ИЭ представляется весьма вероятным, особенно при характерном анамнезе. У лиц, не имеющих характерного анамнеза, выявленных симптомов также бывает достаточно, чтобы заподозрить ИЭ.
На II этапе наиболее частой диагностической ошибкой является оценка того или иного синдрома в качестве проявлений самостоятельного заболевания: например, при выраженных признаках поражения печени ставят диагноз гепатита и пр. Естественно, это возможно при недостаточном учете всей клинической картины и отсутствии связи ведущего синдрома с другими проявлениями болезни.
На III этапе диагностического поиска проводят исследования, подтверждающие предварительный диагноз ИЭ и позволяющие сформулировать окончательный развернутый диагноз.
Л абораторно-инстру ментальные исследования предусматривают:
1) повторные попытки обнаружения возбудителя болезни при многократных посевах крови; 2) подтверждение и(или) выявление воспалительного характера патологического процесса (выявление острофазовых показателей); 3) выявление иммунных сдвигов; 4) уточнение (или выявление) характера поражений различных органов и систем; 5) получение прямых диагностических признаков бактериального поражения эндокарда.
• Получение положительной гемокультуры — наиболее важный диа
гностический признак ИЭ. Для подтверждения диагноза их требу
ется не менее 2 — 3. Единичная положительная гемокультура долж
на интерпретироваться с большой осторожностью вследствие воз
можности случайного загрязнения. Большое значение имеют техни
ка забора и посева крови, время посева (желательно на высоте ли
хорадки), использование обогащенных сред. Отрицательная гемо
культура не исключает ИЭ. Переоценивать роль посевов крови
нельзя, так как имеет значение только положительный результат в
сопоставлении с клинической картиной.
• В клиническом анализе крови наиболее важным для диагности
ки является повышение СОЭ до 50 мм/ч и более. В начале
ИЭ выявляется лейкоцитоз со сдвигом лейкоцитарной формулы
влево; далее могут обнаруживаться лейкопения и гипохромная ане
мия.
Диагностическое значение придается обнаружению гистиоцитов в крови, взятой из мочки уха. Содержание их более 6 в поле зрения может свидетельствовать в пользу ИЭ.
При биохимическом анализе крови выявляется увеличение содержания фибриногена, аг-глобулинов и резкое увеличение уровня у-глобули-нов — до 30 — 40 относительных процентов. Как правило, оказываются положительными осадочные пробы (формоловая и тимоловая).
• Кроме гипергаммаглобулинемии, показателями иммунных сдвигов
являются обнаружение циркулирующих иммунных комплексов,
снижение титра комплемента, появление ревматоидного (антигло-
булинового) фактора, усиление реакции бластной трансформации
лимфоцитов с ФГА (фитогемагглютинин) и бактериальными анти
генами, выявление противотканевых антител. Как правило, при ИЭ
в отличие от ревматизма титры анти-О-стрептолизина и антигиалу-
ронидазы нормальные.
• Анализ мочи позволяет выявить гломерулонефрит, проявляющийся
протеинурией, цилиндрурией и гематурией. При высокой протеину-
рии можно предположить развитие амилоидоза (редко встречаю
щееся осложнение ИЭ). Повышение содержания билирубина,
трансаминаз указывает на поражение печени.
Рентгенологическое, электро- и фонокардиографическое исследования помогают уточнить характер клапанного поражения сердца.
♦ Прямой диагностический признак ИЭ ■-■ наличие вегетации на кла
панах сердца — можно обнаружить при эхокардиографии, исполь
зуя два метода: обследование в М-режиме и при В-сканировании.
Таким образом, на заключительном этапе диагностического поиска диагноз ИЭ может быть поставлен с уверенностью у большинства больных, особенно в иммуновоспалительной стадии. В некоторых случаях постановки окончательного диагноза необходимо динамическое наблюдение.
Диагностика. Распознавание ИЭ при развитой клинической картине заболевания не представляет существенных трудностей. Выделяют клинические (основные и дополнительные) и параклинические признаки [Бут-кевич О.М., 1993].
Клинические признаки основные:
♦ лихорадка выше 38 "С с ознобом;
♦ шум в сердце;
♦ спленомегалия.
Клинические признаки дополнительные:
♦ тромбоэмболии;
♦ кожные васкулиты;
♦ гломерулонефрит.
Параклинические признаки:
♦ вегетации на клапанах;
♦ анемия;
♦ положительный результат посева крови;
♦ СОЭ более 30 мм/ч;
♦ повышение активности щелочной фосфатазы нейтрофилов.
Диагноз вероятен: два основных клинических признака (один из них — шум в сердце) и один дополнительный (даже при отсутствии подтверждения его параклиническими признаками).
Диагноз достоверен: два основных клинических и один дополнительный, а также не менее двух параклинических.
Трудности диагностики обусловлены стертым и атипичным течением ИЭ. Если вторичный септический очаг локализуется не в сердце, а в интиме крупных артерий, то исчезает такой важный диагностический признак, как формирование порока сердца. С учетом этого необходимо оценивать комплекс других диагностически значимых симптомов ИЭ.
Определенные сложности возникают в диагностике на ранних этапах, особенно при первичном ИЭ, начало которого очень напоминает другие заболевания.
Следует помнить о разнообразных вариантах начала ИЭ.
♦ «Типичное» постепенное начало заболевания (субфебрильНая тем
пература тела, слабость, недомогание, головная боль, артралгии).
В таких случаях ИЭ следует дифференцировать от ревматизма; при
развитии аортальной недостаточности — от висцерального сифилиса.
♦ Начало болезни по типу «острого инфекционного заболевания»:
высокая температура тела с проливным потом и ознобом. Следует
проводить дифференциальную диагностику с гриппом, брюшным
тифом, малярией и другими инфекциями.
• Болезнь начинается с развития тромбоэмболии (наиболее часто в
мозг, селезенку, почки). ИЭ необходимо дифференцировать от ин
сульта. Наиболее часто ИЭ проявляется тромбоэмболиями в мозг у
пожилых людей. Дифференциальная диагностика проводится с по
чечной коликой при эмболии в почки.
• При появлении симптомов острого гломерулонефрита в начале бо
лезни (гематурия, протеинурия, отеки, гипертензия) необходим
учет диагностически значимых проявлений ИЭ (положительная ге-
мокультура и пр.).
• «Гематологическая маска» ИЭ, проявляющаяся анемией, увеличе
нием селезенки, требует дифференциальной диагностики с целым
рядом болезней системы крови.
Формулировка развернутого клинического диагноза включает:
1) клинико-морфологическую форму ИЭ (первичный или вторичный);
2) этиологию (если удается повторно получить положительную гемокуль-
туру); 3) степень активности патологического процесса; 4) характер кла
панного поражения; 5) наиболее важные органные поражения с указанием
выраженности функциональных расстройств (сердечная, почечная недо
статочность, анемия и пр.); 6) осложнения (тромбоэмболии и пр.).
Лечение. При лечении больных ИЭ следует руководствоваться рядом правил: 1) терапия ИЭ должна быть, по возможности, этиотропной, направленной против конкретного возбудителя (это важное, но не абсолютное правило); 2) лечение ИЭ должно быть продолжительным (при стрептококковой инфекции не менее 4 нед, при стафилококковой — 6 нед, при грамотрицательной флоре — не менее 8 нед); 3) при неустановленной этиологии заболевания антибиотикотерапию проводят в течение нескольких месяцев (методом проб и ошибок), подбирая эффективный препарат; 4) хирургическое лечение имеет определенные показания; его проводят на некоторых этапах болезни.
Для лечения ИЭ в любых возрастных группах следует в первую очередь использовать антибиотики, оказывающие бактерицидное действие на микроорганизмы. Препаратом первоначального выбора по-прежнему является пенициллин. Он малотоксичен, что позволяет применять его длительно в относительно высоких дозировках. Суточная доза пенициллина до 20 000 000 ЕД вводится внутривенно и внутримышечно. Могут применяться и более высокие дозы пенициллина — до 50 000 000 ЕД и выше. Однако следует помнить, что у больных пожилого и старческого возраста при лечении пенициллином и другими антибиотиками в высоких дозах часто наблюдается кардиотоксический эффект: появление или усиление сердечной недостаточности, боли в области сердца, тахикардия. При уменьшении дозы или смене препарата эти явления быстро проходят.
При ИЭ нестрептококковой этиологии ив случаях, когда возбудитель неизвестен, целесообразно применять комбинированную терапию: пенициллин чаще всего комбинируют с аминогликозидами (гентамицином). Гентамицин применяют в дозах 240 — 320 мг/сут (3 — 5 мг на 1 кг массы тела) в виде курсового лечения: препарат вводят в течение 8 дней, затем 5 — 7 дней перерыв, повторное введение препарата в течение 8 дней, снова перерыв, при необходимости проводят третий курс. Цель прерывистого лечения — предупреждение нефротоксического, гепа-тотоксического действия препарата. У больных пожилого и старческого
возраста суточная доза не должна превышать 240 мг. Вместо гентамицина может быть применен препарат этой же группы — сизомицин (2 мг на 1 кг массы больного). Все препараты этой группы противопоказаны при почечной недостаточности и заболеваниях слухового нерва. Тем не менее комбинация пенициллина с аминогликозидами является одной из наиболее эффективных при лечении ИЭ.
При ИЭ стафилококковой этиологии весьма эффективны полусинтетические пенициллины, устойчивые к ферменту пеницил-линазе, продуцируемой стафилококком. Наиболее часто используют окса-циллин (10 — 20 г/сут), а также ампициллин, ампиокс (10—16 г/сут). Эти препараты сочетают с гентамицином. При отсутствии эффекта от лечения следует назначать антибиотики цефалоспоринового ряда: клафоран 6 —8 г внутривенно или внутримышечно равными дозами каждые 6 —8 ч (6 нед) в сочетании с сульфатом амикацина (1 — 1,5 г внутримышечно равными дозами каждые 8— 12 ч в течение 14 дней с интервалом 14 дней); це-фалотин (цефалотина натриевая соль) 8—12 г внутривенно или внутримышечно равными дозами каждые 6 ч (6 нед).
При энтерококковой инфекции — пенициллин 20 000 000 — 30 000 000 ЕД внутривенно или внутримышечно каждые 4 ч (6 нед) в сочетании со стрептомицином по 1 г внутримышечно равными дозами каждые 12 ч (4 нед). При недостаточном эффекте от данной комбинации препаратов назначают ампициллин по 8—12 г внутримышечно равными дозами каждые 6 ч (6 нед) с гентамицином в обычных дозах.
Лечение грибкового ИЭ проводится амфотерицином (30-55 мг/сут). Курс — не менее 40 — 50 дней. В качестве антибиотиков резерва используют вибрамицин, рондомицин, фузидин (2 — 3 г/сут).
К основным антибиотикам, применяемым при ИЭ, относится также рифампицин (применяется в дозе 600—1200 мг в капсулах и внутривенно), действующий на стафилококки и стрептококки. Оказывает сенсибилизирующее действие, поэтому всегда лучше проводить один длительный курс лечения, чем повторные короткие курсы. Чаще применяется как резервный препарат при неэффективности других антибиотиков. Отмена антибиотиков производится сразу, без постепенного уменьшения дозы. После отмены антибактериальных средств при хорошем самочувствии и благополучных лабораторных показателях больной наблюдается в стационаре еще 7—10 дней для исключения развития ранних рецидивов. Если в процессе лечения развивается резистентность микроорганизмов к проводимой терапии (что проявляется возвратом симптомов: вновь повышается температура тела, появляются ознобы, слабость, СОЭ снова повышается), то следует резко повысить дозу применяемых антибиотиков либо сменить препарат.
Следует отметить, что факторами, обусловливающими резистентность к проводимой антибиотикотерапии, являются позднее начало лечения (в связи с трудностями диагностики); особая вирулентность микрофлоры; наличие микробных ассоциаций (патологический процесс вызывается не одним микроорганизмом); пожилой возраст больных; поражение нескольких клапанов одновременно; эндокардит трехстворчатого клапана; ИЭ, развивающийся у больных, имеющих протезы клапанов или подвергающихся гемодиализу.
Глюкокортикоиды применяются в настоящее время для лечения ИЭ нечасто. Они показаны при резко выраженных имунных сдвигах: высоком
уровне циркулирующих иммунных комплексов в крови, концентрации иммуноглобулинов М и А, васкулите, артрите, миокардите, а также в случае высокой аллергической чувствительности к антибиотикам. Назначают обычно небольшие дозы (15 — 20 мг преднизолона в сутки). Лечение кор-тикостероидами необходимо проводить обязательно в сочетании с антибиотиками и заканчивать его за 1 нед до отмены антибиотиков.
У больных с клиническими признаками миокардита на фоне антибактериальной терапии могут применяться нестероидные противовоспалительные средства — индометацин (75—100 мг/сут). Эффективность их в общем ниже, чем кортикостероидов, но применение их при ИЭ менее опасно в отношении развития нагноительных осложнений, поэтому у некоторых больных применение неспецифических противовоспалительных средств предпочтительнее.
Из препаратов иммунотерапии применяют антистафилококковую плазму в сочетании с антибактериальной терапией (5 вливаний на курс), что может обеспечить при стафилококковом ИЭ наступление стойкой ремиссии, которую иногда не удается получить при применении одних антибиотиков.
В случае необходимости назначают симптоматическое лечение: при сердечной недостаточности — сердечные гликозиды и мочегонные средства; при тромбоэмболии — фибринолитики и антикоагулянты, хирургическое удаление эмбола; при анемии — препараты железа, при кахексии — анаболические стероиды; при повышении артериального давления (АД) гипотензивные препараты и т.д.
В последние годы применяется хирургическое лечение ИЭ. Показания: рефрактерная сердечная недостаточность в сочетании с ИЭ, устойчивым к антибиотикотерапии; инфицирование протезов клапанов; значительные вегетации на клапанах; полная резистентность к терапии; абсцессы миокарда. Операция заключается в замене пораженного клапана протезом (при непрерывной антибиотикотерапии). Летальность при неотложной замене аортального клапана довольно высока (около 30 %), тогда как при плановой операции она значительно ниже (9 %).
Исходы и эволюция ИЭ. Ближайшие исходы: 1) полное выздоровление (с формированием порока сердца или, что более редко, без него); 2) смерть на ранних этапах болезни от прогрессирования инфекции (10 %); 3) летальные эмболии (10 — 20 %); 4) переход в хроническое течение, возможны рецидивы болезни. При этом различают ранние и поздние рецидивы. Наиболее опасны ранние рецидивы, возникающие в течение первых 1 — 3 мес (отмечаются в 10—15 % случаев); поздние рецидивы возникают в более продолжительные сроки, обычно после ремиссии патологического процесса. Отдаленные исходы: 1) смерть при прогрессировании сердечной недостаточности (60 — 65 %); 2) формирование хронического нефрита и смерть от прогрессирующей почечной недостаточности (10 — 15%).
Прогноз. Раннее начало лечения антибиотиками в адекватных дозах может полностью подавить воспалительный процесс. Так, выздоровление от ИЭ, вызванного зеленящим стрептококком, отмечается у 80 — 90 % больных. Однако при других возбудителях прогноз хуже. Так, при стафилококковом и особенно грибковом ИЭ летальность достигает 70 — 90 %, поэтому, если говорить об отдаленных результатах лечения, то полное выздоровление отмечается лишь у V3 больных. Прогноз при аортальной ло-
кализации ИЭ хуже, нежели при митральной. Ближайший и отдаленный прогноз при врожденных пороках лучше, чем при приобретенных.
Профилактика. У больных пороками сердца и другими заболеваниями, которые могут осложняться ИЭ, необходима тщательная санация инфекционных очагов, раннее и энергичное лечение любой интеркуррент-ной инфекции. Следует профилактически использовать лечение антибиотиками короткими курсами у лиц с повышенным риском развития ИЭ (экстракция зубов, снятие зубных камней, тонзиллэктомия, удаление катетера после урологических операций и пр.). За 30 мин — 1 ч до манипуляций вводят 1 000 000 ЕД пенициллина или 2 г ампициллина (оксацил-лина); в этих дозах антибиотики вводят еще 2 — 3 дня.
 2015-05-10
2015-05-10 2217
2217
