Масса одной молекулы (μ - молярная масса, m - масса вещества, N - количество молекул, NА - постоянная Авогадро): 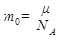 ;
; 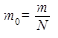
Последовательность молекул, образованных элементами 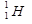 ,
, 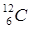 ,
, 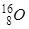 , в порядке увеличения молярной массы:
, в порядке увеличения молярной массы:
1)H2 2)CH4 3)H2O 4)C2H2 5)O2 6)CO2
Молярная масса m определяется соотношением (mо - масса одной молекулы газа, N - общее количество молекул газа, NA - число Авогадро)... 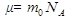
Единица измерения молярной массы вещества в СИ кг·моль-1
Формулы количества молей вещества (N - количество молекул, m - масса вещества, m - молярная масса, N A - число Авогадро): 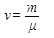 ;
; 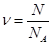 1
1
Один моль в СИ является единицей измерения количества вещества
Количество вещества - это количество молекул
Количество молекул N вещества массой m равно (m -молярная масса, NA - число Авогадро) 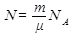
Количество молекул в одном моле вещества называется числом Авогадро
Соответствие между физическими величинами и их размерностями:
Плотность кг·м-3
Концентрация м-3
количество вещества моль
Количество молекул в единице объема вещества - это концентрация молекул
Масса единицы объема вещества - это плотность вещества
Тепловое движение молекул газа, при котором все направления движения молекул равновероятны называют хаотическим
Связь температуры t0 шкалы Цельсия и абсолютной температуры Т 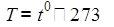
Изменение температуры на 100 С соответствует изменению абсолютной температуры на 100 (К).
Абсолютная температура - это количественная мера энергии молекулы
Единица измерения давления - один Паскаль - в СИ равна 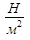
Соответствие между физическими величинами и их единицами в СИ
Давление Па
Объем м3
молярная масса кг/моль
Давление газа на стенки сосуда зависит от: концентрации молекул газатемпературы газа
В процессе теплопроводности происходит перенос энергии
Явление, при котором происходит перенос массы вещества - это диффузия
Градиент концентрации молекул имеет место в явлении диффузии
Поток импульса имеет место в явлении вязкости
Единица измерения универсальной газовой постоянной R = 8,31 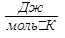 в СИ.
в СИ.
Внутренняя энергия идеального газа (i - число степеней свободы, ν - количество вещества, R - газовая постоянная, Т - абсолютная температура):
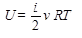
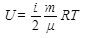
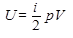
Максимальную внутреннюю энергию идеальный газ имеет в состоянии, обозначенном на диаграмме PV точкой 3
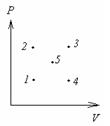
Соответствие формулы работы идеального газа названию процесса:
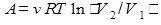 изотермический
изотермический
А=0 изохорный
А=рDV изобарный
Наибольшую работу идеальный газ совершает при переходе из состояния А в состояние 2
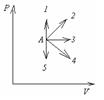
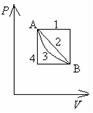
Наибольшую работу газ совершает при переходе из состояния А в состояние В через последовательность состояний, обозначенную цифрой 1
Соответствие между физическими величинами и их единицами измерения количество теплоты Дж
удельная теплоемкость Дж×кг-1×К-1
удельная теплота плавления Дж×кг-1
Количество теплоты - это энергия, переданная газу в процессе теплообмена
Процесс обмена внутренними энергиями соприкасающихся тел, не сопровождающийся совершением работы, называется теплообменом
Отношение 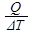 является (Q - теплота, переданная телу, ΔТ - изменение температуры тела) теплоемкостью тела
является (Q - теплота, переданная телу, ΔТ - изменение температуры тела) теплоемкостью тела
Единица удельной теплоемкости вещества в СИ...
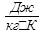
Величина, равная количеству теплоты, которое необходимо, чтобы повысить температуру тела на один кельвин, называется теплоемкостью
Количество теплоты, переданной газу, расходуется на совершение газом работы и на изменение его: температуры внутренней энергии
Формула первого начала термодинамики 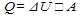
Изменение внутренней энергии 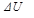 системы (Q - количество теплоты, переданное системе, А работа внешних сил)
системы (Q - количество теплоты, переданное системе, А работа внешних сил) 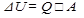
Внутренняя энергия газа, совершившего работу 500 Дж при сообщении ему 900 Дж теплоты увеличилась на 400 Дж
Необратимыми являются процессы: диффузиивязкого течения
В изолированных системах при любых обратимых процессах энтропия не изменяется
В изолированных системах при любых необратимых процессах энтропия возрастает
Невозможно построить вечный двигатель второго рода - это второй закон термодинамики
Невозможен процесс самопроизвольной передачи энергии от холодного тела к горячему – это второй закон термодинамики
Циклически действующий двигатель, совершающий работу за счет получаемого извне тепла, называется тепловой машиной.
Минимальное количество тепловых резервуаров, с которыми рабочее тело тепловой машины обменивается теплом, равно 2
В цикле Карно реализуются процессы: адиабатическийизотермический
Последовательностьгазовых процессов в цикле Карно (начальный объем минимальный, начальное давление максимальное):
1) изотермическое расширение 2) адиабатическое расширение 3) изотермическое сжатие 4) адиабатическое сжатие
КПД идеальной тепловой машины (Qx - теплота, отданная холодильнику, Qн - теплота, полученная от нагревателя, А - работа машины):
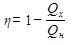
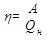
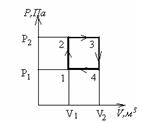
Работа, совершаемая тепловой машиной за один цикл, изображенный на рисунке, равна...
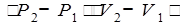
Максимальный КПД идеального теплового двигателя, температура холодильника которого 270С, а температура нагревателя на 1000С больше, равен 25 %.
КПД тепловой машины окажется наибольшим, если круговой процесс в машине совершить через последовательность равновесных процессов.
Идеальным называется газ, у которого потенциальная энергия взаимодействия молекул равна нулю
Состояние системы, при котором все параметры состояния имеют определенные постоянные значения - это равновесное состояние
Давление идеального газа p (n - концентрация молекул газа, Т - абсолютная температура) 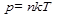
Нагревание идеального газа в закрытом сосудеприводит к увеличению средней скорости и средней кинетической энергии молекул газа.
Основное уравнение молекулярно-кинетической теории идеального газа: 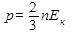
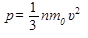
Соответствие между физическими величинами и их обозначениями в формуле давления идеального газа р=nkT:
р давление
n концентрация молекул
T температура газа
Уравнение состояния идеального газа (уравнение Менделеева-Клапейрона) 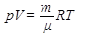
Количество молекул N идеального газа в объеме V при давлении р и температуре T (k - постоянная Больцмана, NA - число Авогадро, R -газовая постоянная) 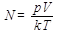
Плотность идеального газа (р - давление, Т - абсолютная температура, μ - молярная масса, R - универсальная газовая постоянная) 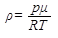
Последовательность молекул газов в порядке увеличения плотности газов при одинаковых давлении и температуре (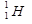 ,
, 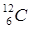 ,
, 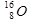 )...
)...
1)CO2 2)O2 3)C2H2 4)CH4 5)H2
Уравнение изохорического процесса 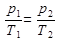
Давление газа при возрастании температуры в 2 раза в изохорическом процессе увеличится в 2 раза
Процесс, совершаемый идеальным газом при постоянном объеме, называется изохорическим
Процесс 1-2, изображенный на ТР - диаграмме для идеального газа (m = const) изохорический
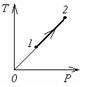
В процессе, показанном на диаграмме TР, при постоянной массе газа остается неизменным объем

Объем данной массы идеального газа при переходе из состояния 1 в состояние 2 сначала не изменялся, затем уменьшался
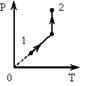
Соотношение объемов трех состояний идеального газа, обозначенных точками 1, 2и3 на диаграмме РT (m - const) 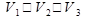
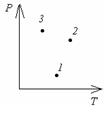
Процессу идеального газа, изображенному в координатных осях PT, соответствует график процесса в координатах РV под номером 2
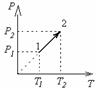
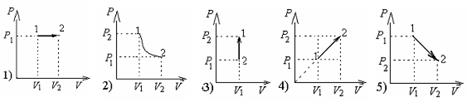
При изохорическом процессе переданная газу теплота равна изменению его внутренней энергии.
Молярная теплоемкость при постоянном объеме равна (i - число степеней свободы, 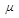 -молярная масса, R - универсальная газовая постоянная)
-молярная масса, R - универсальная газовая постоянная) 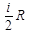
Удельная теплоемкость при постоянном объеме (i - число степеней свободы, 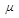 -молярная масса, R - универсальная газовая постоянная)
-молярная масса, R - универсальная газовая постоянная) 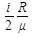
Уравнение изобарического процесса 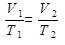
Объем идеального газа при возрастании температуры в 2 раза в изобарическом процессе увеличится в 2 раза
При изобарном охлаждении данной массы газа: уменьшается объемуменьшается внутренняя энергия
Процесс, совершаемый идеальным газом при постоянном давлении, называется изобарным
Изобарический процесс изображен на графиках, обозначенных номерами 1 и 3
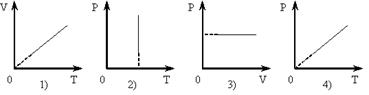
В процессе перехода идеального газа из состояния 1 в состояние 2 может:
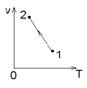 уменьшаться давление при постоянной массе
уменьшаться давление при постоянной массе
 2015-07-14
2015-07-14 1209
1209








